Les chercheurs du MIT ont identifié un problème qui tend à limiter les processus chimiques de transformation du dioxyde de carbone en carburant ou en d'autres produits chimiques utiles - et des moyens de résoudre ce problème. Crédit :Varanasi Lab
Si les chercheurs pouvaient trouver un moyen de convertir chimiquement le dioxyde de carbone en carburant ou en d'autres produits, ils pourraient réduire considérablement les émissions de gaz à effet de serre. Mais bon nombre de ces processus qui semblaient prometteurs en laboratoire n'ont pas fonctionné comme prévu dans des formats à grande échelle qui conviendraient à une utilisation avec une centrale électrique ou d'autres sources d'émissions.
Aujourd'hui, des chercheurs du MIT ont identifié, quantifié et modélisé l'une des principales raisons des mauvaises performances de ces systèmes de conversion. Le coupable s'avère être un épuisement local du gaz carbonique juste à côté des électrodes utilisées pour catalyser la conversion. Le problème peut être atténué, a découvert l'équipe, en coupant et en remettant simplement le courant à des intervalles spécifiques, ce qui laisse le temps au gaz de remonter jusqu'aux niveaux nécessaires à côté de l'électrode.
Les résultats, qui pourraient stimuler les progrès dans le développement d'une variété de matériaux et de conceptions pour les systèmes de conversion électrochimique du dioxyde de carbone, ont été publiés aujourd'hui dans la revue Langmuir , dans un article du postdoctorant du MIT Álvaro Moreno Soto, de l'étudiant diplômé Jack Lake et du professeur de génie mécanique Kripa Varanasi.
"L'atténuation du dioxyde de carbone est, je pense, l'un des défis importants de notre époque", déclare Varanasi. Alors qu'une grande partie de la recherche dans le domaine s'est concentrée sur la capture et la séquestration du carbone, dans lesquelles le gaz est pompé dans une sorte de réservoir souterrain profond ou converti en un solide inerte tel que le calcaire, une autre voie prometteuse a été de convertir le gaz en d'autres carbone composés tels que le méthane ou l'éthanol, à utiliser comme carburant, ou l'éthylène, qui sert de précurseur à des polymères utiles.
Il existe plusieurs façons d'effectuer de telles conversions, y compris les procédés électrochimiques, thermocatalytiques, photothermiques ou photochimiques. "Chacun d'entre eux a des problèmes ou des défis", dit Varanasi. Les processus thermiques nécessitent une température très élevée et ne produisent pas de produits chimiques de très grande valeur, ce qui est également un défi avec les processus activés par la lumière, dit-il. "L'efficacité est toujours en jeu, toujours un problème."
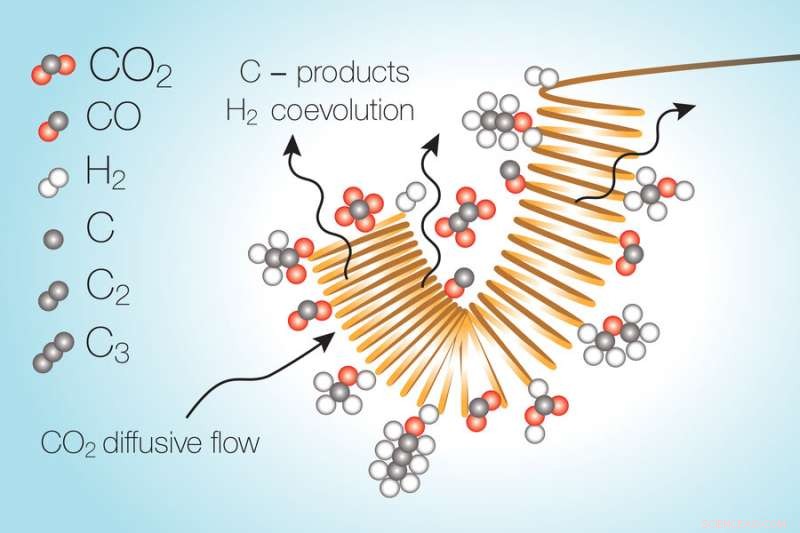
L'équipe s'est concentrée sur les approches électrochimiques, dans le but d'obtenir des "produits à teneur plus élevée en carbone" - des composés qui contiennent plus d'atomes de carbone et ont tendance à être des carburants de plus grande valeur en raison de leur énergie par poids ou volume. Dans ces réactions, le plus grand défi a été de freiner les réactions concurrentes qui peuvent avoir lieu en même temps, en particulier la division des molécules d'eau en oxygène et hydrogène.
Les réactions ont lieu lorsqu'un flux d'électrolyte liquide contenant le dioxyde de carbone dissous passe sur une surface catalytique métallique chargée électriquement. Mais au fur et à mesure que le dioxyde de carbone est converti, il laisse derrière lui une région dans le flux d'électrolyte où il a essentiellement été utilisé, et ainsi la réaction dans cette zone appauvrie se tourne plutôt vers la séparation de l'eau. Cette réaction indésirable consomme de l'énergie et réduit considérablement l'efficacité globale du processus de conversion, ont découvert les chercheurs.
"Il y a un certain nombre de groupes qui travaillent là-dessus, et un certain nombre de catalyseurs qui sont là-bas", dit Varanasi. "Dans tout cela, je pense que la co-évolution de l'hydrogène devient un goulot d'étranglement."
Une façon de contrecarrer cet épuisement, ont-ils découvert, peut être obtenue par un système pulsé - un cycle consistant simplement à couper la tension, à arrêter la réaction et à donner au dioxyde de carbone le temps de se propager dans la zone appauvrie et d'atteindre à nouveau des niveaux utilisables, et puis reprendre la réaction.
Souvent, disent les chercheurs, les groupes ont trouvé des matériaux catalyseurs prometteurs mais n'ont pas effectué leurs tests de laboratoire assez longtemps pour observer ces effets d'épuisement, et ont donc été frustrés en essayant d'étendre leurs systèmes. De plus, la concentration de dioxyde de carbone à côté du catalyseur dicte les produits qui sont fabriqués. Par conséquent, l'épuisement peut également modifier la gamme de produits fabriqués et rendre le processus peu fiable. "Si vous voulez être en mesure de créer un système qui fonctionne à l'échelle industrielle, vous devez être capable de faire fonctionner les choses sur une longue période de temps", explique Varanasi, "et vous ne devez pas avoir ce genre d'effets qui réduisent le l'efficacité ou la fiabilité du processus."
L'équipe a étudié trois matériaux catalyseurs différents, dont le cuivre, et "nous nous sommes vraiment concentrés sur la compréhension et la capacité de quantifier les effets d'épuisement", a déclaré Lake. Au cours du processus, ils ont pu développer un moyen simple et fiable de surveiller l'efficacité du processus de conversion en temps réel, en mesurant les niveaux de pH changeants, une mesure de l'acidité, dans l'électrolyte du système.
Dans leurs tests, ils ont utilisé des outils analytiques plus sophistiqués pour caractériser les produits de réaction, y compris la chromatographie en phase gazeuse pour l'analyse des produits gazeux et la caractérisation par résonance magnétique nucléaire pour les produits liquides du système. Mais leur analyse a montré que la simple mesure du pH de l'électrolyte à côté de l'électrode pendant le fonctionnement pouvait fournir une mesure suffisante de l'efficacité de la réaction au fur et à mesure de sa progression.
Cette capacité à surveiller facilement la réaction en temps réel pourrait finalement conduire à un système optimisé par des méthodes d'apprentissage automatique, contrôlant le taux de production des composés souhaités grâce à une rétroaction continue, déclare Moreno Soto.
Maintenant que le processus est compris et quantifié, d'autres approches pour atténuer l'épuisement du dioxyde de carbone pourraient être développées, selon les chercheurs, et pourraient facilement être testées à l'aide de leurs méthodes.
Ce travail montre, dit Lake, que "quel que soit votre matériau catalyseur" dans un tel système électrocatalytique, "vous serez affecté par ce problème". Et maintenant, en utilisant le modèle qu'ils ont développé, il est possible de déterminer exactement quel type de fenêtre temporelle doit être évalué pour avoir une idée précise de l'efficacité globale du matériau et quel type d'opérations système pourrait maximiser son efficacité.