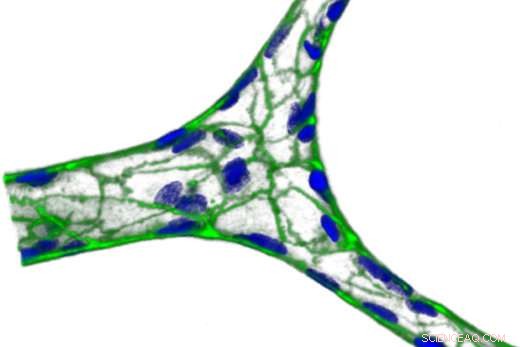
Un vaisseau sanguin miniature, formé sur un hydrogel d'agarose/gélatine. Le vert représente la VE-cadhérine, une protéine qui colle les cellules ensemble, et le bleu est les noyaux. Crédits :Yongzhi Qiu
Dans des maladies telles que le paludisme et la drépanocytose, les globules rouges se décomposent, avec des effets nocifs sur le reste du corps - en particulier la paroi des petits vaisseaux sanguins.
Les ingénieurs biomédicaux ont établi un système modèle pour étudier ces problèmes, qui peut également être utilisé dans d'autres maladies cardiovasculaires. Le système construit un réseau de vaisseaux sanguins artificiels, à base de matériaux "hydrogels" familiers qui se dissolvent à la chaleur :gélatine et agarose, un sucre dérivé d'algues.
Les résultats ont été récemment publiés par Nature Génie Biomédical .
"L'innovation technologique clé ici est que notre hydrogel peut maintenir la croissance de ces vaisseaux pendant des semaines, voire des mois, ce qui est beaucoup plus long que les approches standard, " dit l'auteur principal Wilbur Lam, MARYLAND, doctorat « Avec ce système, nous pouvons étudier non seulement comment les vaisseaux réagissent aux aspects de la maladie, mais aussi à quel point les vaisseaux guériront au fil du temps une fois ces insultes supprimées. »
Lam est professeur adjoint au département de pédiatrie de la faculté de médecine de l'Université Emory et au département de génie biomédical Wallace H. Coulter de Georgia Tech et de l'Université Emory.
Travailler avec Lam, instructeur Yongzhi Qiu, doctorat et ses collègues ont construit un dispositif microfluidique à base d'hydrogel, avec des vaisseaux ramifiés d'environ 20 micromètres de diamètre. Le dispositif peut alors être recouvert de cellules endothéliales, qui tapissent les vaisseaux sanguins, et connecté à une pompe. Un avantage d'utiliser des hydrogels, les auteurs écrivent, est que les hydrogels ne sont pas aussi rigides que les polymères solides, et ainsi répondre d'une manière plus physiologiquement pertinente aux changements de débit de fluide.
Une fois entièrement assemblé, les cellules endothéliales affaiblissent leurs barrières en réponse à des molécules inflammatoires telles que le TNF-alpha puis guérissent par la suite.
Les chercheurs ont également testé les réponses à l'hème, un composant de l'hémoglobine formé lorsque les globules rouges s'ouvrent, et ils ont testé les effets des globules rouges sujets à l'occlusion provenant de patients drépanocytaires et des globules rouges infectés par des parasites Plasmodium.
Le système modèle pourrait être utilisé pour disséquer davantage les effets des globules rouges par rapport à d'autres cellules et molécules inflammatoires, et pour rechercher des médicaments qui pourraient prévenir les dommages aux vaisseaux sanguins, disent les chercheurs.