Les photocatalyseurs hautement réducteurs ou oxydants constituent un défi fondamental en photochimie. Seuls quelques complexes de métaux de transition contenant des ions métalliques abondants sur Terre ont jusqu’à présent évolué vers des oxydants à l’état excité, notamment le chrome, le fer et le cobalt. Tous ces photocatalyseurs nécessitent une lumière de haute énergie pour leur excitation et leur pouvoir oxydant n’a pas encore été pleinement exploité. De plus, les métaux précieux et donc chers sont les ingrédients décisifs dans la plupart des cas.
Une équipe de chercheurs dirigée par le professeur Katja Heinze de l'Université Johannes Gutenberg de Mayence (JGU) a développé un nouveau système moléculaire basé sur l'élément manganèse. Le manganèse, contrairement aux métaux précieux, est le troisième métal le plus abondant après le fer et le titane et est donc largement disponible et très bon marché. L'étude est publiée dans la revue Nature Chemistry .
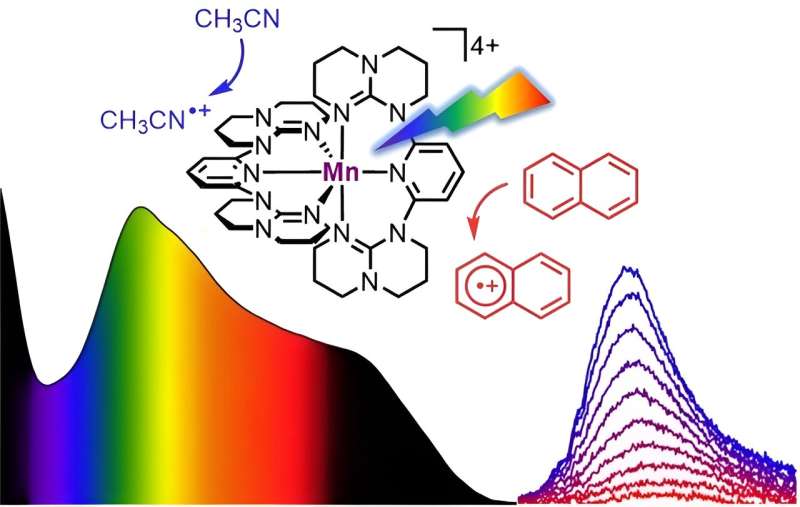
L'équipe du professeur Katja Heinze a conçu un complexe de manganèse soluble qui absorbe toute la lumière visible du bleu au rouge, c'est-à-dire dans une longueur d'onde de 400 à 700 nanomètres, et une partie de la lumière proche infrarouge jusqu'à 850 nanomètres. Cette absorption panchromatique du complexe rappelle la couleur sombre du Braunstein ou du dioxyde de manganèse, qui est un minéral naturel.
Contrairement au minéral Braunstein, le nouveau « Braunstein moléculaire » émet après excitation avec une lumière visible ou NIR-I d'une longueur d'onde de 850 nanomètres une lumière NIR-II d'une longueur d'onde de 1 435 nanomètres. "Il s'agit d'une observation inhabituelle pour un système moléculaire basé sur le manganèse dans son état d'oxydation +IV. Même avec des métaux nobles, les émissions dans cette région énergétique sont essentiellement sans précédent", a déclaré le professeur Katja Heinze.
Encore plus intrigante au-delà de cette luminescence NIR-II provenant d’un système moléculaire au manganèse est l’observation selon laquelle, après photoexcitation, le « Braunstein moléculaire » peut oxyder divers substrats organiques. Cela inclut des molécules aromatiques extrêmement difficiles avec des potentiels d'oxydation très élevés telles que le naphtalène, le toluène ou le benzène.
"Même des solvants très stables peuvent être attaqués par le superphotooxydant lorsqu'ils sont excités par la lumière LED", a déclaré le Dr Nathan East, qui a préparé le nouveau complexe et réalisé toutes les expériences de photolyse au cours de son doctorat. dans le groupe du professeur Katja Heinze.
Les techniques spectroscopiques ultrarapides utilisant des impulsions laser avec une résolution temporelle inférieure à la picoseconde ont révélé une réactivité inhabituelle à l'état excité et deux états photoactifs différents :un état de haute énergie de très courte durée mais extrêmement oxydant et un état de basse énergie modérément oxydant de plus longue durée. Le premier peut attaquer les molécules de solvant qui sont déjà proches du complexe avant l'excitation lumineuse, tandis que le second état excité existe suffisamment longtemps pour attaquer les substrats aromatiques après une collision diffusionnelle.
"C'est ce qu'on appelle l'extinction statique et dynamique des états excités", a expliqué le Dr Robert Naumann, scientifique principal spécialisé en spectroscopie résolue en temps au sein du groupe du professeur Katja Heinze.
"Une image détaillée des processus photoinduits a émergé lorsque nous avons modélisé les états excités impliqués par des calculs de chimie quantique à la lumière des résultats spectroscopiques", a déclaré Heinze.
"Ces calculs avancés et longs n'ont été possibles qu'en utilisant la puissance de calcul des supercalculateurs MOGON et ELWETRITSCH en Rhénanie-Palatinat", a déclaré le Dr Christoph Förster, scientifique principal du groupe de Katja Heinze, fortement impliqué dans le domaine quantique. étude chimique.
À l’avenir, les scientifiques pourraient être en mesure de développer de nouvelles réactions stimulantes induites par la lumière en utilisant le manganèse, un métal commun et abondant. Cela remplacera non seulement les composés rares et plus coûteux du ruthénium et de l'iridium, qui sont encore aujourd'hui les plus fréquemment utilisés, mais permettra même de créer des classes de réactions et de substrats qui ne sont pas disponibles avec les composés classiques.
"Grâce à notre propre système laser ultrarapide nouvellement installé, à la puissance de calcul de superordinateurs hautes performances et à la créativité et aux compétences de nos doctorants, nous continuerons à poursuivre nos efforts pour développer une photochimie plus durable", a déclaré le professeur. Katja Heinze.
Plus d'informations : Nathan R. East et al, Photoréactivité oxydative à deux états d'un complexe de manganèse (IV) utilisant la lumière proche infrarouge, Nature Chemistry (2024). DOI :10.1038/s41557-024-01446-8
Fourni par l'Université Johannes Gutenberg de Mayence