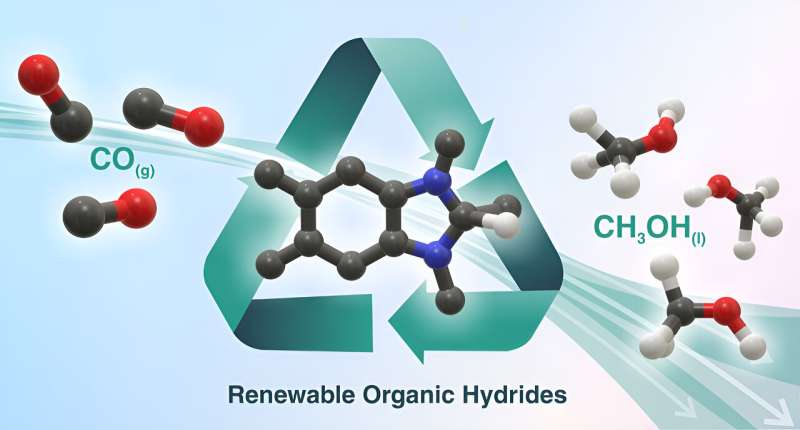
Des scientifiques du Laboratoire national de Brookhaven du Département américain de l'énergie (DOE) et de l'Université de Caroline du Nord à Chapel Hill (UNC) ont démontré la conversion sélective du dioxyde de carbone (CO2 ) en méthanol en utilisant une stratégie de réaction en cascade. Le processus en deux parties est alimenté par la lumière du soleil, se déroule à température ambiante et à pression ambiante, et utilise un réactif organique recyclable similaire à un catalyseur présent dans la photosynthèse naturelle.
"Notre approche constitue une étape importante vers la recherche d'un moyen efficace de convertir le CO2 , un puissant gaz à effet de serre qui pose un défi important pour l'humanité, en un carburant liquide facilement stockable et transportable", a déclaré Javier Concepcion, chimiste principal du Brookhaven Lab, auteur principal de l'étude.
La recherche a été menée dans le cadre du Centre pour les approches hybrides de l’énergie solaire aux combustibles liquides (CHASE), un pôle d’innovation énergétique basé à l’UNC. L'étude est publiée en couverture du Journal of the American Chemical Society. .
La conversion à température ambiante du CO2 dans les carburants liquides est une quête qui dure depuis des décennies. De telles stratégies pourraient contribuer à atteindre des cycles énergétiques neutres en carbone, en particulier si la conversion est alimentée par la lumière du soleil. Le carbone émis sous forme de CO2 en brûlant des molécules de carburant à carbone unique telles que le méthanol, elles pourraient essentiellement être recyclées pour fabriquer un nouveau carburant sans ajouter de nouveau carbone dans l'atmosphère.
Méthanol (CH3 OH) est une cible particulièrement attractive car il s’agit d’un liquide facilement transportable et stockable. En plus de son utilité comme carburant, le méthanol sert de matière première clé dans l’industrie chimique pour fabriquer des molécules plus complexes. De plus, comme le méthanol ne contient qu'un seul atome de carbone, comme le CO2 , cela évite la nécessité de créer des liaisons carbone-carbone, qui nécessitent des processus énergivores.
Cependant, les étapes clés impliquées dans les réactions nécessaires pour générer de manière sélective et efficace des combustibles liquides solaires comme le méthanol restent mal comprises.
"Conversion du CO2 au méthanol est très difficile à réaliser en une seule étape. Sur le plan énergétique, cela équivaut à gravir une très haute montagne", a déclaré Concepcion. "Même si la vallée de l'autre côté est à une altitude plus basse, y arriver nécessite beaucoup d'énergie."
Au lieu d'essayer de relever le défi en une seule « ascension », l'équipe Brookhaven/UNC a utilisé une stratégie en cascade (en plusieurs étapes) qui passe par plusieurs intermédiaires plus faciles à atteindre.
"Imaginez escalader plusieurs petites montagnes au lieu d'une grande, et le faire à travers plusieurs vallées", a déclaré Concepion.

Les vallées représentent les intermédiaires de réaction. Mais même atteindre ces vallées peut s’avérer difficile, car il nécessite un échange progressif d’électrons et de protons entre diverses molécules. Pour diminuer les besoins énergétiques de ces échanges, les chimistes utilisent des molécules appelées catalyseurs.
"Les catalyseurs permettent d'atteindre la vallée suivante à travers des 'tunnels' qui nécessitent moins d'énergie que l'escalade par-dessus la montagne", a déclaré Concepcion.
Pour cette étude, l’équipe a exploré les réactions utilisant une classe de catalyseurs appelés dihydrobenzimidazoles. Ce sont des hydrures organiques, des molécules qui possèdent deux électrons supplémentaires et un proton à « donner » à d'autres molécules. Ils sont peu coûteux, leurs propriétés peuvent être facilement manipulées et des études antérieures ont montré qu'ils peuvent être recyclés, une condition nécessaire pour un processus catalytique.
Ces molécules ont une structure et une fonction similaires aux cofacteurs organiques responsables du transport et de la fourniture d'énergie sous forme d'électrons et de protons pendant la photosynthèse naturelle.
"La photosynthèse elle-même est une cascade de nombreuses étapes de réaction qui convertissent le CO2 atmosphérique en , l'eau et l'énergie lumineuse en énergie chimique sous forme de glucides, à savoir des sucres, qui peuvent ensuite être métabolisés pour alimenter l'activité des organismes vivants. Notre approche consistant à utiliser des hydrures organiques biomimétiques pour catalyser le méthanol en tant que carburant liquide peut donc être considérée comme une approche artificielle de la photosynthèse", a déclaré Renato Sampaio, co-auteur principal de l'UNC.
Dans l'étude, les chimistes ont brisé la conversion du CO2 en méthanol en deux étapes :réduction photochimique du CO2 en monoxyde de carbone (CO), suivi de transferts séquentiels d'hydrure des dihydrobenzimidazoles pour convertir le CO en méthanol.
Leurs travaux décrivent les détails de la deuxième étape, alors que la réaction se déroule à travers une série d'intermédiaires, notamment un monoxyde de carbone lié au ruthénium (Ru-CO 2+ ), un ruthénium formyle (Ru-CHO + ), un groupement hydroxyméthyle de ruthénium (Ru-CH2 OH + ), et enfin, la libération de méthanol induite par la lumière.
Alors que les deux premières étapes de ce schéma sont des « réactions sombres », la troisième étape qui aboutit à du méthanol libre est initiée par l'absorption de la lumière par l'hydroxyméthyle de ruthénium (Ru-CH2 OH + ) complexe. Le mécanisme proposé par lequel cela se produit passe par un transfert d'électrons à l'état excité entre le Ru-CH2 OH + et une molécule d'hydrure organique suivie rapidement d'un transfert de protons broyé qui aboutit à la génération de méthanol en solution.
« La nature « one-pot » et sélective de cette réaction entraîne la génération de concentrations millimolaires (mM) de méthanol – la même plage de concentrations que les matières premières – et évite les complications qui ont entravé les efforts précédents visant à utiliser des catalyseurs inorganiques pour ces réactions", a déclaré Gerald Meyer, co-auteur de l'UNC et directeur de CHASE. "Ce travail peut donc être considéré comme une étape importante dans l'utilisation de catalyseurs à hydrures organiques renouvelables dans la quête de plusieurs décennies de production catalytique de méthanol à température ambiante à partir de CO2. ."
Plus d'informations : Andressa V. Müller et al, Réduction du CO en méthanol avec des hydrures organiques recyclables, Journal of the American Chemical Society (2024). DOI :10.1021/jacs.3c14605
Fourni par le Laboratoire national de Brookhaven