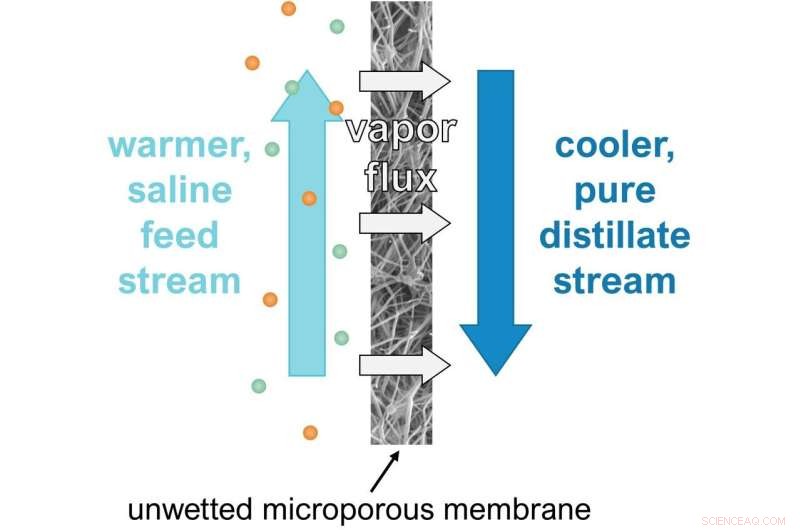
Le flux d'eau chaude à haute salinité se trouve d'un côté de la membrane et un flux d'eau pure froide se trouve de l'autre. l'eau réchauffée s'évapore, laissant derrière elle le sel et formant une vapeur, qui se transforme en une forme liquide distillée lorsqu'elle rencontre le courant d'eau froide de l'autre côté de la membrane. Crédit :Allyson McGaughey.
Ayant grandi à Seattle, Allyson McGaughey, Ph.D. de l'USC Viterbi School of Engineering. '21, n'a jamais été confronté à la réalité quotidienne de la sécheresse. Dans le désert de plus en plus chaud et sec de Los Angeles, cependant, la rareté de l'eau a été mise à nu, augmentant l'urgence de trouver des solutions alternatives pour l'eau.
Dans une recherche publiée dans le Journal of Membrane Science , McGaughey, en coordination avec Amy Childress, professeur émérite de l'USC Viterbi Gabilan, a révélé de nouvelles idées sur la meilleure façon de concevoir des processus de purification de l'eau - par exemple, le traitement des eaux usées dans une installation de traitement de l'eau - à l'aide de la distillation membranaire (MD). MD est un processus qui sépare le sel de l'eau à l'aide d'une fine membrane sèche et poreuse. Des différences de température modérées font passer l'eau d'un côté à l'autre.
Pour mieux comprendre cela, pensez à une passoire à spaghetti, mais avec des trous beaucoup, beaucoup plus petits. Un jet d'eau versé à travers la passoire sera "nettoyé" de certains matériaux dans l'eau qui sont trop gros pour passer à travers les trous de la passoire (comme les pores d'une membrane), laissant un jet "propre" de l'autre côté de la passoire. Pourtant, tout ce qui est plus petit que ces trous, comme le sel dissous dans l'eau de nos pâtes, peut toujours passer. Pour purifier encore plus, et si nous pouvions collecter uniquement la vapeur, ou la vapeur d'eau pure ? Maintenant, imaginez une passoire qui ne laisse passer que de la vapeur, et non de l'eau liquide, à travers les trous. Ensuite, même les sels dissous ne peuvent pas passer. En utilisant une membrane très hydrophobe (craignant l'eau) qui fait exactement cela, MD peut être utilisé pour extraire de l'eau pure et dessalée des cours d'eau contaminés.
Selon les chercheurs, le succès de la distillation membranaire repose en grande partie sur des conceptions de membranes capables de réduire ou d'éliminer l'humidité qui s'accumule dans la membrane. Si une membrane devient humide, selon les chercheurs, elle peut perdre son efficacité, compromettant la qualité de l'eau traitée. À cette fin, McGaughey, maintenant boursier postdoctoral à l'Université de Princeton, a étudié la meilleure façon de concevoir des membranes afin qu'elles ne deviennent pas excessivement humides et traitent avec succès l'eau, en éliminant le sel et les contaminants et en créant un écoulement de haute qualité ou pur. /P>
Selon McGaughey, parmi leurs principales conclusions, la réduction de la taille des pores de la membrane ou l'augmentation de l'épaisseur de la membrane elle-même peuvent augmenter la résistance à l'eau et retarder ou empêcher la contamination du flux d'eau purifiée.
Les membranes sont généralement constituées d'un matériau synthétique hydrophobe ou résistant à l'eau avec des pores de 0,1 à 0,5 micromètre de petite taille. McGaughey a déclaré que si d'autres processus sont généralement plus économes en énergie que la distillation membranaire - par exemple, un processus appelé osmose inverse - dans le cas de courants d'eau plus salés, ces processus plus typiques nécessitent une pression considérable pour forcer les molécules d'eau à travers la membrane. . Ainsi, les rendant moins pratiques pour traiter les flux très salés.
En revanche, la distillation membranaire permet de purifier l'eau plus salée plus efficacement qu'avec l'osmose inverse et permet aux scientifiques de purifier les eaux usées plus salées qui sont généralement éliminées car elles ne peuvent pas être efficacement nettoyées par les processus de traitement de l'eau traditionnels.
Le problème, a déclaré McGaughey, est que les membranes qui filtrent les eaux usées peuvent être excessivement humides. "Dans l'osmose inverse, nous utilisons des membranes denses qui ne sont pas poreuses pour que seules les molécules d'eau passent à travers, mais dans la distillation par membrane, il y a des trous dans les membranes qui peuvent permettre la contamination si elles sont mouillées", a-t-elle déclaré.
Optimisation de la distillation membranaire pour augmenter la résistance à l'eau des membranes
Le dessalement est par nature un processus coûteux et énergivore en raison des propriétés chimiques du sel et de l'eau. Le sel se dissout facilement dans l'eau, créant des liens très difficiles à rompre, ont déclaré les chercheurs.
"Si nous avions le choix, nous ne dessaliserions pas du tout", a déclaré McGaughey, "mais nous avons de plus en plus besoin de cette eau."
Avec la distillation par membrane, McGaughey a déclaré qu'un flux salé réchauffé est placé d'un côté d'une membrane sèche et un flux d'eau fraîche et pure est de l'autre. La différence de température entre les deux courants est la force motrice qui déplace l'eau d'un côté à l'autre. Afin de séparer l'eau pure du sel et d'autres contaminants, les molécules d'eau dans le flux salé passent d'un liquide à un gaz vapeur en raison de la chaleur.
À l'intérieur des pores de la membrane sèche, il y a un petit espace d'air qui permet la collecte de vapeur, qui se produit lorsque l'eau salée est réchauffée et s'évapore, traversant la membrane tout en laissant le sel derrière. Parce que l'entrefer est petit, peu de chaleur est nécessaire pour transformer l'eau salée en vapeur, ce qui signifie que vous pouvez utiliser l'énergie solaire pour réchauffer le liquide salé. La vapeur représente l'eau purifiée ou le distillat qui, de l'autre côté de la membrane, est refroidi — par l'eau froide — et revient sous forme liquide.
La résistance de la membrane à l'eau liquide, ou résistance au mouillage, est essentielle pour garantir que le flux de distillat est réellement purifié plutôt que contaminé. Lorsque la membrane est mouillée, l'eau liquide des eaux usées ou du flux salin se mélange au flux d'eau purifiée, créant un résultat de qualité inférieure, voire un résultat d'eau qui ne répondrait pas aux normes de potabilité.
Essayer de comprendre comment une membrane perd sa résistance au mouillage à un niveau fondamental et comment cela peut être évité grâce à l'hydrophobicité du matériau de la membrane et à la taille des pores est essentiel, ont déclaré les chercheurs.
"Nous avons des membranes qui fonctionnent maintenant, mais lorsque vous montez à des salinités extrêmement élevées et que vous obtenez une précipitation de sel sur la surface de la membrane, cela reste un grand défi", a déclaré McGaughey.
Défis émergents de l'approvisionnement en eau
"La gestion des flux de déchets à haute salinité est un défi majeur, par exemple, les flux de déchets industriels", a déclaré McGaughey.
"Cette [distillation membranaire] ne sera jamais plus économe en énergie que l'osmose inverse, mais elle peut utiliser l'énergie solaire thermique ou la chaleur" perdue "de faible qualité, ce qui signifie qu'elle peut compter sur l'énergie verte. Cela signifie moins d'émissions de carbone que l'électricité nous utilisons pour conduire l'osmose inverse et elle peut également atteindre des flux de salinité plus élevés », a-t-elle déclaré.
Au lieu qu'un seul processus soit une solution autonome, McGaughey a déclaré que la distillation membranaire pourrait être un complément à l'osmose inverse, par exemple quelque chose que vous pouvez utiliser en aval (plus loin dans le processus de traitement de l'eau), après un traitement par osmose inverse.
"La distillation membranaire pourrait être utilisée sur le flux d'eau salée rejeté qui sort de l'osmose inverse pour maximiser l'utilisation de l'eau disponible", a-t-elle déclaré.
McGaughey a également déclaré que la distillation par membrane pourrait également avoir des applications dans les régions rurales et non électrifiées.