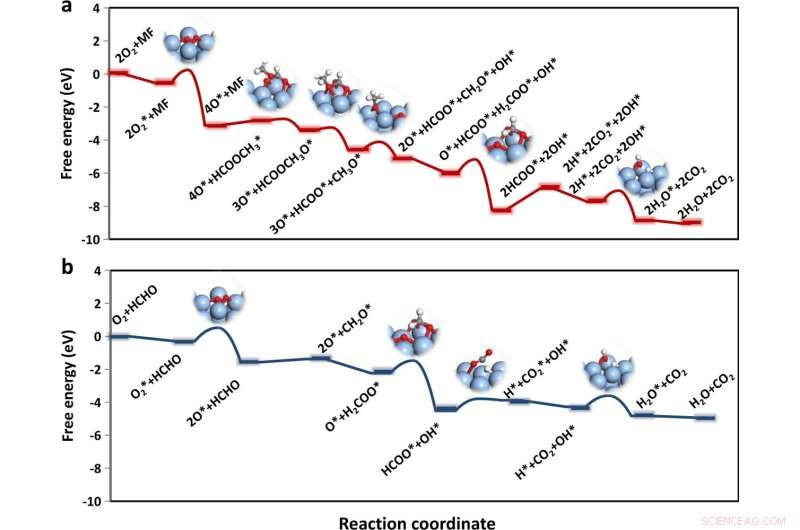
Diagrammes d'énergie libre des processus d'oxydation. a Oxydation MF (ligne rouge) et b HCHO (ligne bleue) sur la surface Ag(100), respectivement. Les structures d'état de transition sont représentées sous forme d'encarts, où Ag, C, O et H sont représentés respectivement en argent, gris, rouge et blanc. Crédit :Nature Communications (2022). DOI :10.1038/s41467-022-29936-8
Un groupe de recherche dirigé par le professeur Xiao Jianping et Assoc. Le professeur Jiao Feng de l'Institut de physique chimique de Dalian (DICP) de l'Académie chinoise des sciences (CAS), en collaboration avec le professeur Qu Zhenping de l'Université de technologie de Dalian, a conçu un catalyseur tandem bifonctionnel zéolithes-argent (Ag) qui pourrait stimule l'oxydation du formaldéhyde à basse température.
Cette étude a été publiée dans Nature Communications le 22 avril.
Les calculs théoriques et les résultats expérimentaux ont montré que l'activité d'oxydation du formaldéhyde était influencée par la séparation entre les deux composants du catalyseur bifonctionnel.
Les chercheurs ont découvert une tendance volcanique pour la séparation entre les nanoparticules de ZSM-5 et d'Ag, ce qui signifie que ce n'est pas "le plus proche, le mieux".
Le formaldéhyde activé par ZSM-5 acide détaché pourrait générer des intermédiaires gazeux de formiate de méthyle, qui était plus facilement oxydé par les composants ultérieurs (Ag). Le composant Ag adsorberait inévitablement les molécules de formaldéhyde n'ayant pas réagi et conduirait ainsi à une activité d'oxydation du formiate de méthyle plus faible lorsque les deux composants étaient trop proches.
L'oxydation du formiate de méthyle sur les composants Ag a obtenu une activité élevée en supprimant la formation de dioxyméthylène (DOM), qui était difficile à oxyder davantage.
Par rapport à celle du catalyseur à l'argent supporté monofonctionnel, la conversion du formaldéhyde a été augmentée de 50 fois (100 % contre 2 %) à 70 degrés Celsius. Des chercheurs révèlent un mécanisme à voies multiples dans la réduction électrochimique du CO2