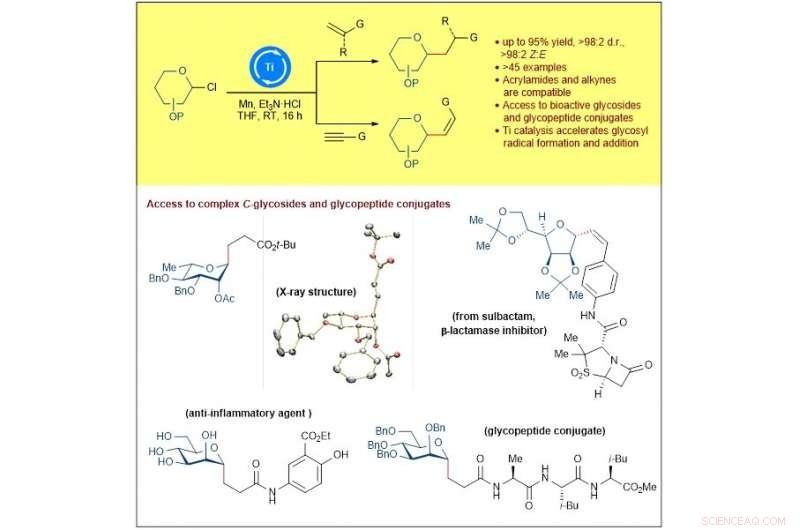
Figure 1 :Schéma montrant le développement d'un régime général de fonctionnalisation par radicaux glycosyle catalysé par le titane qui offre un accès rapide à de précieux C -alkyle et C -alcényl glycosides. Crédit: Chimie
Les chimistes de NUS ont conçu une nouvelle stratégie pour synthétiser des glycosides C-alkyle et C-alcényle importants sur le plan médical grâce à un processus de transformation réductrice catalysée par le titane qui réagit facilement avec les chlorures de glycosyle et divers alcènes ou alcynes activés.
Les glycosides C-alkyliques sont largement présents dans la nature et présentent une myriade d'activités biologiques souhaitables. Par ailleurs, la robustesse des liaisons C-glycosidiques vis-à-vis des enzymes hydrolytiques in vivo permet aux C-alkylglycosides de jouer un rôle crucial dans la conception de candidats pharmaceutiques à base de sucre. En particulier, la synthèse de C-alkyl glycosides conjugués à des acides aminés ou à des dérivés peptidiques offre une plate-forme puissante pour développer des peptidomimétiques à base de sucre. Ces analogues de peptides C-glycosylés sont utiles dans le développement de médicaments et les études biologiques pour étudier le mécanisme de transport hémato-encéphalique impliquant des peptides bioactifs ainsi que le rôle de la glycosylation dans la stabilisation des peptides. Malheureusement, les protocoles non catalytiques existants reposent souvent sur des quantités superstoechiométriques de réactifs qui limitent la praticité, alors que les protocoles catalytiques actuels présentent une portée limitée qui entrave l'applicabilité à la préparation de médicaments et de glycopeptides.
Une équipe de recherche dirigée par le professeur Koh Ming Joo, du Département de chimie, L'Université nationale de Singapour a développé une réaction qui favorise la formation de liaisons carbone-carbone entre les donneurs de chlorure de glycosyle et les alcènes/alcynes électroattracteurs dans des conditions réductrices douces pour donner des glycosides C stéréodéfinis (voir Figure 1). Des études mécanistiques ont révélé que les espèces catalytiques de titane accélèrent la génération d'intermédiaires radicaux glycosyle et leur addition à travers la liaison p. L'utilisation de la source de protons du chlorhydrate de triéthylamine est tout aussi cruciale, qui permet une protonolyse efficace (clivage d'une liaison chimique par des acides) pour renverser le cycle catalytique. D'autres informations ont été obtenues à partir des calculs de la théorie fonctionnelle de la densité (DFT) effectués par le Dr Zhang Xinglong, un collaborateur de l'Institut de Calcul Haute Performance de l'Agence pour la Science, Technologie et recherche (A*STAR).
Le professeur Koh a dit, "Notre nouveau collecteur catalysé au titane n'est pas seulement une avancée dans le domaine de la fonctionnalisation catalytique des radicaux glycosyle, mais contribue également de manière significative à la recherche sur les glucides en fournissant une voie permettant d'accéder à des blocs de construction de glycoside C de grande valeur. »
"Nous attendons de notre protocole développé qu'il facilite les études biologiques et alimente de nouvelles initiatives de chimie médicinale vers le développement de candidats thérapeutiques à base de glyco. En outre, les connaissances mécaniques dérivées de nos travaux sont susceptibles d'inspirer de futurs efforts dans la conception de nouvelles transformations stéréosélectives pour accéder à d'autres classes importantes de composés glucidiques, " a ajouté le professeur Koh.
L'équipe de recherche prévoit d'utiliser ce travail pour la synthèse d'une bibliothèque de C-glycosides pour des tests biologiques potentiels.