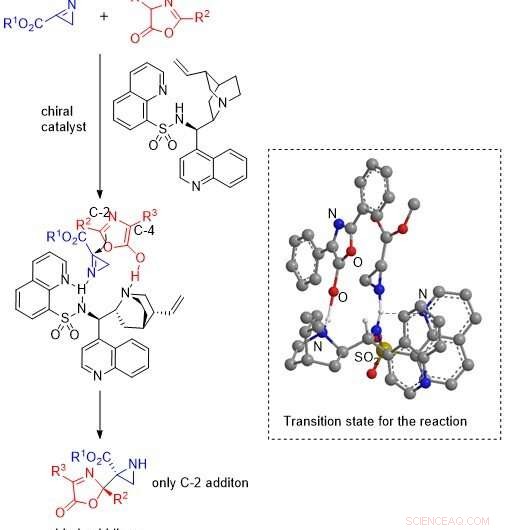
Produire des aziridines avec un rendement élevé et une pureté élevée en utilisant un nouveau catalyseur. Des scientifiques japonais ont récemment proposé un état de transition possible pour la réaction entre les aziridines et les oxazolones en présence d'un catalyseur sulfonamide alcaloïde de quinquina, produire des composés aziridine-oxazolone souhaitables avec des rendements élevés et une énantiosélectivité ou pureté. Crédit :Shuichi Nakamura de NITech
À moins que vous n'ayez étudié la chimie à l'université, il est peu probable que vous ayez rencontré le nom d'aziridine. Composé organique de formule moléculaire, C
Une de ces techniques qui a récemment attiré l'attention du point de vue de la synthèse pharmaceutique implique l'utilisation d'oxazolones, des composés chimiques de formule moléculaire C.
Dans une nouvelle étude publiée récemment dans Lettres organiques , Le professeur Nakamura avec ses collègues de NITech et de l'Université d'Osaka, Japon, exploré cette question et, dans une percée significative, ont réussi à obtenir des composés aziridine-oxazolone avec des rendements élevés (99 %) ainsi qu'une énantiosélectivité ou une pureté élevée (98 %). En outre, l'équipe a utilisé un catalyseur original qu'ils ont développé pour catalyser les réactions qu'ils ont étudiées.
L'équipe a commencé par chauffer des -azideacrylates à 150°C dans un solvant organique tétrahydrofurane (THF) pour préparer des 2H-azirines, puis les a fait réagir avec des oxazolones en présence de divers organocatalyseurs pour produire différents composés aziridine-oxazolone. En particulier, l'équipe a examiné l'effet du catalyseur cinchonine et de divers groupes hétéroarènecarbonyle et hétéroarènesulfonyle dans des organocatalyseurs dérivés d'alcaloïdes de quinquina et a découvert que les réactions utilisant des catalyseurs avec un groupe 2-pyridinesulfonyle ou un groupe 8-quinoléinesulfonyle donnaient à la fois un rendement élevé (81-99% ) ainsi qu'une énantiopure élevée (93-98%). En outre, les scientifiques ont observé que la réaction entre une 2H-azirine contenant un groupe ester éthylique et une oxazolone avec un 3, Le groupe 5-diméthoxyphényle en présence du catalyseur avec le groupe 8-quinoléinesulfonyle a également donné des rendements élevés (98-99 %) ainsi qu'une énantiopure (97-98 %).
L'équipe est ensuite passée à l'exploration de la réaction entre la 2H-azirine avec un groupe ester éthylique et une plus grande variété d'oxazolones en présence du catalyseur avec un groupe 8-quinoléinesulfonyle. Dans toutes les réactions, ils ont observé des rendements élevés (77-99%) et des énantiopures (94-99%) sauf un pour le cas d'une oxazolone portant un groupe benzyle et le catalyseur avec un groupe 2-pyridylsulfonyle qui n'a produit qu'un rendement modéré ( 61%) et pureté (86%). De plus, ils ont pu convertir les aziridines obtenues en divers autres énantiomères sans aucune perte de pureté.
Finalement, l'équipe a proposé un mécanisme catalytique et un état de transition pour la réaction des 2H-azirines avec les oxazolones dans lequel le catalyseur active à la fois l'oxazolone et la 2H-azirine, qui réagissent alors pour donner un produit d'addition qui, à son tour, donne l'aziridine avec régénération du catalyseur.
Bien que le mécanisme détaillé n'ait pas encore été clarifié, les scientifiques sont enthousiasmés par leurs découvertes et attendent avec impatience l'application de la méthode en médecine et en pharmacologie. « Il a le potentiel de fournir aux gens de nouveaux médicaments et de créer de nouveaux médicaments ainsi que des candidats médicaments qui sont actuellement difficiles à synthétiser. De plus, le catalyseur utilisé dans cette étude peut être utilisé pour de nombreuses autres réactions de synthèse stéréo-sélectives, " observe un Pr Nakamura optimiste.
Des conséquences fascinantes à envisager à coup sûr !