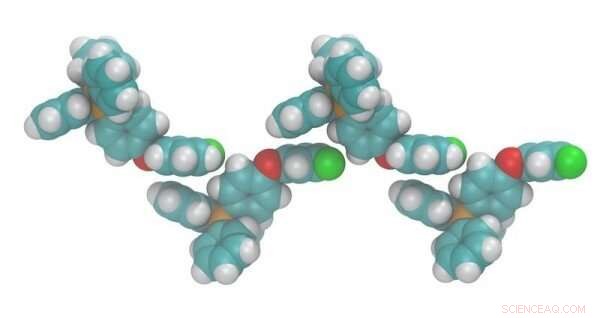
Simulation d'un sel fluoré démontrant l'alignement des cations. L'ajout d'atomes de fluor électronégatifs (vert) conduit à un alignement avec les centres de phosphore électropositifs (orange) dans la phase solide provoquant des interactions qui abaissent le point de fusion. Crédit :Brooks Rabideau, Université du Sud de l'Alabama, Génie chimique et biomoléculaire et Société royale de chimie
Bien que les charges opposées s'attirent toujours, ils n'interagissent pas toujours aussi étroitement que possible. Dans une nouvelle étude, les chercheurs ont utilisé une combinaison de simulations moléculaires et d'expériences pour démontrer les effets d'une modification subtile de la structure des cations chargés positivement dans des composés constitués d'ions. Ces changements encouragent les cations à s'aligner les uns avec les autres dans la phase solide de la matière. Cela diminue certains types d'interactions potentielles entre les cations et les anions chargés négativement dans la phase solide. Cet alignement des cations diminue également le point de fusion du composé ionique, souvent de manière significative.
De nombreux procédés chimiques nécessitent des liquides comme solvants pour les réactions chimiques, lubrifiants, fluides caloporteurs. Les liquides se vaporisent souvent au cours du processus. Cela peut créer des émissions dangereuses. Les composés ioniques liquides (liquides ioniques) offrent une solution à ce problème car ils ont une très faible volatilité, ce qui signifie qu'ils sont moins susceptibles de se vaporiser. Certains liquides ioniques sont stables à haute température, mais leurs points de fusion peuvent être trop élevés pour une utilisation pratique. Les résultats de ces travaux fournissent aux scientifiques un nouvel ensemble d'outils pour concevoir des composés ioniques avec des points de fusion plus bas. Ces résultats permettront aux scientifiques de concevoir des composés ioniques à utiliser sur une plus large gamme de températures et d'applications.
Les liquides ioniques sont des sels liquides à la température à laquelle ils sont utilisés. Ces liquides ont une variété d'utilisations potentielles dans des processus sans danger pour l'environnement. En particulier, les liquides ioniques thermiquement stables sont prometteurs en tant que solvants à haute température et fluides caloporteurs. Cependant, ces liquides ioniques peuvent avoir des points de fusion bien au-dessus de la température ambiante. Cela limite leur aptitude au traitement à des températures plus basses. Ainsi, comprendre comment abaisser le point de fusion de ces composés élargira leur utilisation potentielle et permettra aux technologies qui en dépendent.
Les scientifiques savent que les changements structurels, en particulier ceux conférant une asymétrie importante, diminuer les points de fusion d'une grande variété de composés. Ces modifications structurelles ne sont pas possibles tout en conservant des composés thermiquement robustes, car de nombreuses structures chimiques courantes ont une faible stabilité thermique. Les chercheurs ont montré dans la présente étude que des changements structurels subtils qui augmentent également le moment dipolaire du cation peuvent abaisser considérablement les points de fusion. La simulation informatique fournit un aperçu au niveau moléculaire et démontre que l'augmentation du moment dipolaire provoque l'alignement des cations les uns avec les autres dans la phase solide. Cela entrave à son tour les interactions anion/cation et augmente l'enthalpie en phase solide (une mesure de la chaleur ou du travail dans le système). Cette augmentation de l'enthalpie en phase solide diminue l'enthalpie de fusion entraînant des points de fusion plus bas. Cette étude fournit une règle de conception pour abaisser le point de fusion de liquides ioniques structurellement similaires en modifiant leur moment dipolaire.