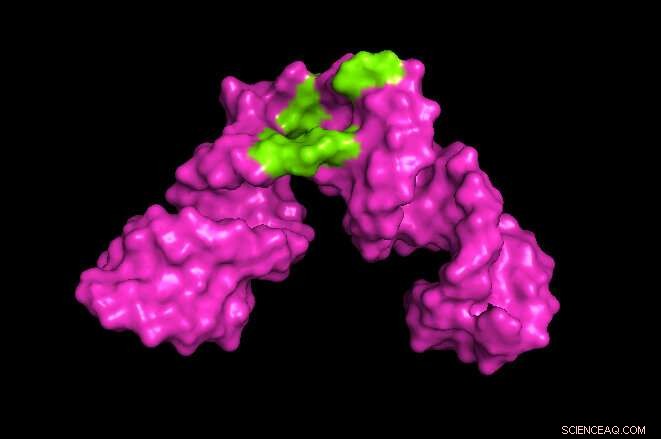
Des chercheurs de l'Université du Maryland ont développé une méthode pour étendre la portée de la spectroscopie par résonance magnétique nucléaire (RMN). Dans l'exemple ci-dessus, les chercheurs ont pu créer une image 3D révélant le site sur un morceau d'ARN de l'hépatite où de petites molécules telles qu'un médicament pourraient se lier (en vert). Crédit :Kwaku Dayie/Université du Maryland
Des scientifiques de l'Université du Maryland ont développé une méthode pour déterminer les structures de grosses molécules d'ARN à haute résolution. La méthode surmonte un défi qui a limité l'analyse et l'imagerie 3-D de l'ARN aux seules petites molécules et morceaux d'ARN au cours des 50 dernières années.
La nouvelle méthode, qui élargit le champ d'application de la spectroscopie par résonance magnétique nucléaire (RMN), permettra aux chercheurs de comprendre la forme et la structure des molécules d'ARN et d'apprendre comment elles interagissent avec d'autres molécules. Les informations fournies par cette technologie pourraient conduire à des traitements thérapeutiques ciblés par ARN pour la maladie. Le document de recherche sur ce travail a été publié dans la revue Avancées scientifiques le 7 octobre 2020.
"Le champ de la spectroscopie de résonance magnétique nucléaire a été bloqué en regardant des choses qui sont petites, disons 35 blocs de construction d'ARN ou nucléotides. Mais la plupart des choses intéressantes qui sont biologiquement et médicalement pertinentes sont beaucoup plus importantes, 100 nucléotides ou plus, " dit Kwaku Dayie, professeur de chimie et de biochimie à l'UMD et auteur principal de l'article. "Donc, être capable de briser l'embouteillage et de regarder les choses qui sont grandes est très excitant. Cela nous permettra de jeter un coup d'œil à ces molécules et de voir ce qui se passe d'une manière que nous n'avons pas pu faire auparavant. »
En spectroscopie RMN, les scientifiques dirigent des ondes radio vers une molécule, excitant les atomes et "éclairant" la molécule. En mesurant les changements du champ magnétique autour des atomes excités - la résonance magnétique nucléaire - les scientifiques peuvent reconstituer des caractéristiques telles que la forme, structure et mouvement de la molécule. Les données que cela produit peuvent ensuite être utilisées pour générer des images, un peu comme les images IRM vues en médecine.
Ordinairement, Les signaux RMN des nombreux atomes d'une molécule biologique tels que l'ARN se chevauchent, rendant l'analyse très difficile. Cependant, dans les années 1970, les scientifiques ont appris à concevoir biochimiquement des molécules d'ARN pour mieux fonctionner avec la RMN en remplaçant les atomes d'hydrogène par des atomes de fluor magnétiquement actifs. Dans des molécules d'ARN relativement petites constituées de 35 nucléotides ou moins, les atomes de fluor s'allument facilement lorsqu'ils sont touchés par des ondes radio et restent excités suffisamment longtemps pour une analyse à haute résolution. Mais à mesure que les molécules d'ARN grossissent, les atomes de fluor ne s'allument que brièvement, puis perdent rapidement leur signal. Cela a empêché l'analyse 3D à haute résolution de molécules d'ARN plus grosses.
Des travaux antérieurs réalisés par d'autres avaient montré que le fluor continuait à produire un signal fort lorsqu'il se trouvait à côté d'un atome de carbone contenant six protons et sept neutrons (C-13). Donc, Dayie et son équipe ont développé une méthode relativement simple pour changer le C-12 naturel dans l'ARN (qui a 6 protons et 6 neutrons) en C-13 et installer un atome de fluor (F-19) juste à côté.
Dayie et son équipe ont d'abord démontré que leur méthode pouvait produire des données et des images équivalentes aux méthodes actuelles en l'appliquant à des morceaux d'ARN du VIH contenant 30 nucléotides, qui avait été précédemment imagé. Ils ont ensuite appliqué leur méthode à des morceaux d'ARN de l'hépatite B contenant 61 nucléotides, soit près du double de la taille de la spectroscopie RMN précédente possible pour l'ARN.
Leur méthode a permis aux chercheurs d'identifier des sites sur l'ARN de l'hépatite B où de petites molécules se lient et interagissent avec l'ARN. Cela pourrait être utile pour comprendre l'effet de médicaments thérapeutiques potentiels. La prochaine étape pour les chercheurs est d'analyser des molécules d'ARN encore plus grosses.
"Ce travail nous permet d'élargir ce qui peut être mis en évidence, " a dit Dayie. " Nos calculs nous disent que, en théorie, nous pouvons regarder de très grandes choses, comme une partie du ribosome, qui est la machine moléculaire qui synthétise les protéines à l'intérieur des cellules."
En comprenant la forme et la structure d'une molécule, les scientifiques peuvent mieux comprendre sa fonction et comment il interagit avec son environnement. Quoi de plus, cette technologie permettra aux scientifiques de voir la structure 3D au fur et à mesure qu'elle change, parce que les molécules d'ARN en particulier changent fréquemment de forme. Ces connaissances sont essentielles pour développer des thérapies qui ciblent étroitement les molécules spécifiques à la maladie sans affecter les fonctions cellulaires saines.
"L'espoir est que si les chercheurs connaissent les coins et recoins d'une molécule dysfonctionnelle, alors ils peuvent concevoir des médicaments qui remplissent les coins et recoins pour le mettre hors service, " dit Dayie. " Et si nous pouvons suivre ces molécules alors qu'elles changent de forme et de structure, alors leur réponse aux médicaments potentiels sera un peu plus prévisible, et la conception de médicaments efficaces peut être plus efficace. »