Combler le vide dans la synthèse d'ammoniac :le rôle des lacunes d'azote dans les catalyseurs
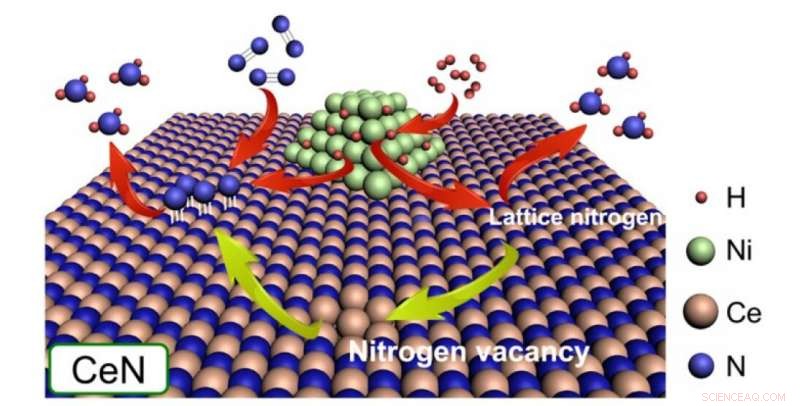
Les particules de nickel dissocient H2 pour fournir des atomes H soit aux atomes N du réseau cristallin CeN lui-même, soit aux atomes N saillants des molécules N2 remplissant une lacune d'azote. Dans cette étude, il a été constaté que CeN sans Ni peut également dissocier les molécules H2. Crédit : 2020 Société chimique américaine
Des scientifiques de l'Institut de technologie de Tokyo (Tokyo Tech) explorent comment les lacunes d'azote dans les catalyseurs participent à la synthèse de l'ammoniac, un produit chimique essentiel dans l'industrie des engrais. Ils ont élaboré une règle générale pour la conception intelligente de catalyseurs à base de nitrure en fonction de leur énergie de formation de lacunes d'azote et ont créé un catalyseur hautement performant pour la synthèse d'ammoniac à l'aide de cérium, un métal de transition abondant.
Ammoniac (NH 3 ) est un produit chimique naturellement présent dans l'environnement, mais son utilisation généralisée en tant qu'ingrédient important dans divers procédés de fabrication en a fait l'un des produits chimiques les plus produits. Il est essentiel dans la production d'engrais et contribue à augmenter le rendement de diverses cultures. En raison de sa forte demande, bien plus de 150 millions de tonnes de NH 3 sont produits chaque année. Sans surprise, les chimistes ont activement recherché des moyens écologiques et économes en énergie de synthétiser le NH 3 .
La manière conventionnelle de produire du NH 3 est en utilisant directement de l'azote (N 2 ) et l'hydrogène (H 2 ) des gaz. Mais, rompre le lien fort entre les atomes N est un défi. C'est là que les catalyseurs (matériaux qui facilitent les réactions nécessaires) entrent en jeu. Malheureusement, le catalyseur le plus performant d'aujourd'hui pour NH 3 la synthèse nécessite du ruthénium, un métal rare et cher. Dans un effort pour trouver des alternatives, scientifiques de Tokyo Tech, dont le Dr Tian-Nan Ye, Professeur Masaaki Kitano, et le professeur Hideo Hosono, ont récemment essayé de découvrir exactement ce qui fait un bon catalyseur pour briser N 2 et la production de NH 3 .
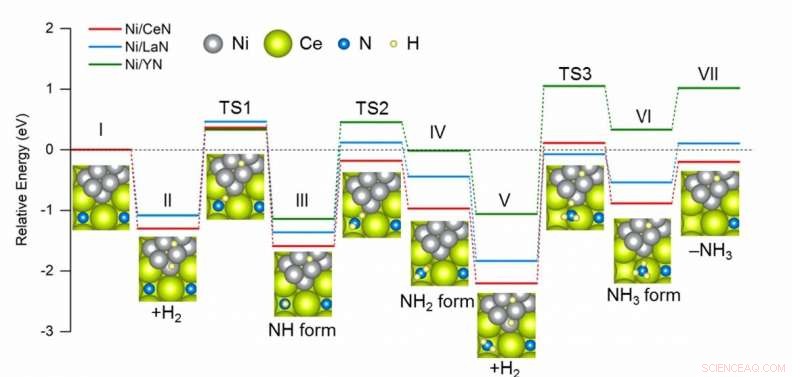
Diagramme comparatif de l'énergie nécessaire à chaque étape lors de la synthèse de NH3 à l'aide de différents catalyseurs. Ni/CeN a le profil énergétique le plus favorable pour la formation de nouvelles lacunes d'azote, ce qui se traduit par de meilleures performances catalytiques. Crédit : 2020 Société chimique américaine
Dans un précédent article publié dans La nature , Hosono et ses collègues avaient présenté une nouvelle stratégie pour produire NH 3 qui impliquait l'utilisation de nitrure de lanthane (LaN) couplé à des nanoparticules de nickel (Ni). La contribution clé de cette étude a été la réalisation que les lacunes d'azote jouent un rôle important dans le processus catalytique, ce qui leur a permis de concevoir un catalyseur à base de La avec des performances comparables à celles à base de ruthénium. Dans une étude récente, publié dans le Journal de l'American Chemical Society , l'équipe de recherche a poussé ses découvertes encore plus loin et a exploré si l'énergie requise pour produire ces lacunes d'azote est ce qui définit finalement la performance des catalyseurs pendant NH 3 production.
Les lacunes d'azote à la surface du catalyseur peuvent facilement capturer N 2 et affaiblir sa liaison N-N, après quoi les atomes se sont dissociés de H 2 au niveau du Ni, les nanoparticules sautent sur l'atome de N en saillie pour produire du NH 3 . En outre, les atomes H dissociés peuvent également former NH 3 en utilisant directement des atomes de N du réseau cristallin du catalyseur lui-même, créant ainsi de nouvelles lacunes d'azote dans le processus. Suite au succès de leur précédent catalyseur Ni/LaN, dans cette étude, ils ont créé et comparé des catalyseurs similaires avec différentes énergies de formation de lacunes d'azote (ENV).
Parmi les catalyseurs testés, Le nitrure de cérium chargé en Ni (CeN) a présenté les meilleures performances catalytiques en raison de son ENV relativement faible. La performance des autres matériaux testés était également directement liée à leur ENV respective. Enthousiasmé par les résultats, Remarques du professeur Hosono, "Nous pouvons maintenant proposer une règle générale pour la conception de catalyseurs à base de nitrure pour NH 3 synthèse, dans laquelle leur ENV domine leurs performances catalytiques. l'activité catalytique du Ni/CeN était comparable à celle des catalyseurs à base de ruthénium, représentant une alternative potentielle écologique composée de matériaux plus abondants.
Quoi de plus, l'équipe a également noté que le chargement de Ni sur CeN n'était même pas nécessaire ; les lacunes d'azote dans CeN peuvent également déclencher la dissociation de H 2 molécules. "Il a été démontré que le CeN en lui-même et avec une charge de Ni produisait les catalyseurs les plus efficaces et les plus stables pour la synthèse de l'ammoniac parmi les différents catalyseurs de nitrure que nous avons étudiés, " explique Ye. L'équipe espère que les connaissances acquises grâce à cette étude pourraient également être utiles dans des applications autres que la synthèse d'ammoniac. Kitano conclut :« La compréhension du rôle des nitrures peut faire la lumière sur la conception et le développement de catalyseurs efficaces à base de métaux de transition pour d'autres processus chimiques. »

