
Un exemple de petit, électrode à circulation que les chercheurs de Duke utilisaient pour produire plus d'hydrogène à partir de l'électrolyse avec un sou pour l'échelle. Crédit :Wiley Lab, université de Duke
Électrolyse, faire passer un courant dans l'eau pour la briser en hydrogène et oxygène gazeux, pourrait être un moyen pratique de stocker l'énergie excédentaire provenant de l'énergie éolienne ou solaire. L'hydrogène peut être stocké et utilisé comme carburant plus tard, quand le soleil est couché ou que les vents sont calmes.
Malheureusement, sans une sorte de stockage d'énergie abordable comme celui-ci, des milliards de watts d'énergie renouvelable sont gaspillés chaque année.
Pour que l'hydrogène soit la solution au problème du stockage, l'électrolyse par division de l'eau devrait être beaucoup plus abordable et efficace, dit Ben Wiley, professeur de chimie à l'Université Duke. Et lui et son équipe ont quelques idées sur la façon d'y parvenir.
Wiley et son laboratoire ont récemment testé trois nouveaux matériaux qui pourraient être utilisés comme matériau poreux, électrode à circulation pour améliorer l'efficacité de l'électrolyse. Leur objectif était d'augmenter la surface de l'électrode pour les réactions, en évitant de piéger les bulles de gaz produites.
"Le taux maximum de production d'hydrogène est limité par les bulles bloquant l'électrode, empêchant littéralement l'eau d'atteindre la surface et de se diviser, " dit Wiley.
Dans un article paru le 25 mai dans Matériaux énergétiques avancés , ils ont comparé trois configurations différentes d'une électrode poreuse à travers laquelle l'eau alcaline peut s'écouler au fur et à mesure que la réaction se produit.
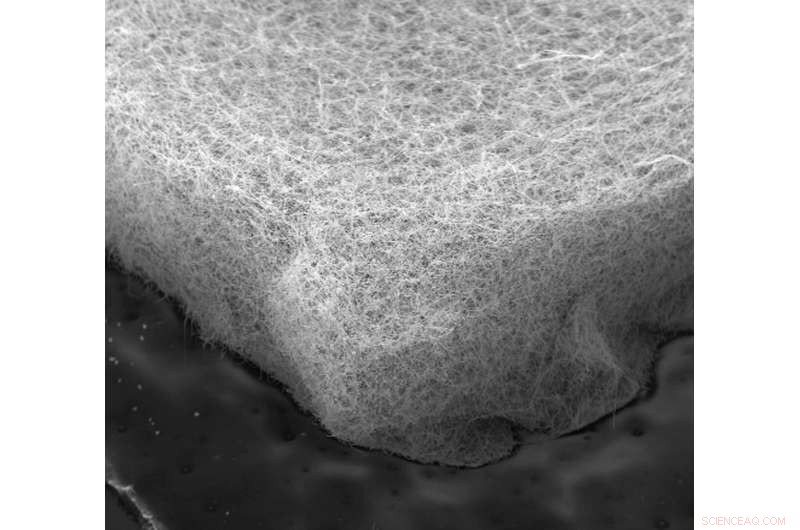
Une vue microscopique du feutre de nickel qui a optimisé la surface et la libération des bulles en produisant de l'hydrogène à partir de l'électrolyse. Crédit :Wiley Lab, université de Duke
Ils ont fabriqué trois types d'électrodes à flux continu, chacun un carré de 4 millimètres de matériau semblable à une éponge, juste un millimètre d'épaisseur. L'un était fait d'une mousse de nickel, l'un était un « feutre » fait de microfibres de nickel, et le troisième était un feutre fait de nanofils de nickel-cuivre.
Courant pulsé à travers les électrodes pendant cinq minutes, cinq minutes de repos, ils ont découvert que le feutre composé de nanofils de nickel-cuivre produisait initialement de l'hydrogène plus efficacement car il avait une plus grande surface que les deux autres matériaux. Mais dans les 30 secondes, son efficacité a plongé car le matériau s'est obstrué par des bulles.
L'électrode en mousse de nickel était la meilleure pour laisser s'échapper les bulles, mais il avait une surface sensiblement plus faible que les deux autres électrodes, le rendant moins productif.
Le sweet spot s'est avéré être un feutre de microfibre de nickel qui produisait plus d'hydrogène que le feutre de nanofil, en dépit d'avoir 25 pour cent moins de surface pour la réaction.
Au cours d'un test de 100 heures, le feutre en microfibres produisait de l'hydrogène à une densité de courant de 25, 000 milliampères par centimètre carré. A ce rythme, il serait 50 fois plus productif que les électrolyseurs alcalins classiques actuellement utilisés pour l'électrolyse de l'eau, les chercheurs ont calculé.

Une vue au microscope électronique du feutre de nickel qui a optimisé la surface et la libération des bulles lorsqu'il a produit de l'hydrogène à partir de l'électrolyse. Crédit :Wiley Lab, université de Duke
Le moyen le moins cher de produire des quantités industrielles d'hydrogène à l'heure actuelle n'est pas de diviser l'eau, mais en brisant le gaz naturel (méthane) avec de la vapeur très chaude - une approche énergivore qui crée 9 à 12 tonnes de C02 pour chaque tonne d'hydrogène qu'il produit, sans compter l'énergie nécessaire pour créer de la vapeur à 1000 degrés Celsius.
Wiley a déclaré que les producteurs commerciaux d'électrolyseurs d'eau pourraient être en mesure d'améliorer la structure de leurs électrodes en fonction de ce que son équipe a appris. S'ils pouvaient augmenter considérablement le taux de production d'hydrogène, le coût de l'hydrogène produit à partir de la séparation de l'eau pourrait baisser, peut-être même assez pour en faire une solution de stockage abordable pour les énergies renouvelables.
Il travaille également avec un groupe d'étudiants du programme Bass Connections de Duke qui explorent la possibilité d'étendre l'électrolyse à flux continu pour produire de l'hydrogène à partir de l'abondante énergie solaire indienne.