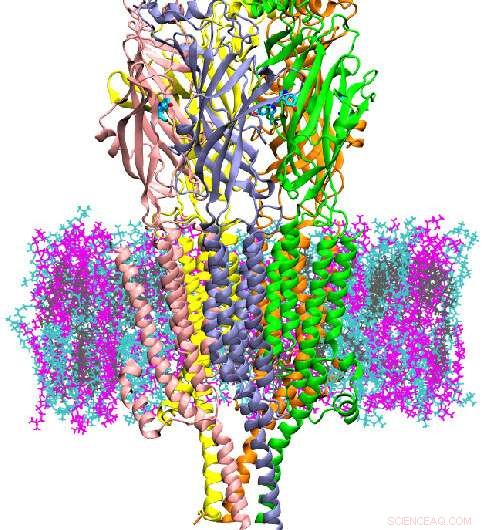
Crédit :A. James Clark School of Engineering, Université du Maryland
Des scientifiques de l'Université du Maryland (UMD) et du National Institute of Standards and Technology (NIST) ont découvert un moyen de détecter le mécanisme moléculaire par lequel 5HT3A, un récepteur de la sérotonine situé au niveau de la synapse neuronale, est activé. Disposer d'un modèle moléculaire de cette activation permettra de tester des inhibiteurs pharmaceutiques en utilisant des modèles informatiques au lieu d'expériences traditionnelles, potentiellement réduire le coût et le temps de dépistage de nouveaux médicaments.
L'étude menée par Jeffery Klauda, professeur de génie chimique et biomoléculaire (ChBE) à l'Université du Maryland (UMD), a été publié dans le Actes de l'Académie nationale des sciences ( PNAS ) aujourd'hui. Nicolas Guros, un assistant de recherche diplômé du ChBE, a été le premier auteur de l'étude et a été co-dirigé par Arvind Balijepalli, un ingénieur en mécanique au NIST.
5HT3A est un type de protéine connue sous le nom de canal ionique, impliqué dans la dépression, l'anxiété et ciblé pour réduire les nausées induites par la chimiothérapie. Il régule le flux d'ions au niveau de la fente post-synaptique des neurones. Les auteurs ont effectué des simulations informatiques de 5HT3A pendant jusqu'à 20 microsecondes, bien plus longtemps que les simulations précédentes effectuées pour
"Si vous pensez à la dynamique moléculaire (MD) comme un microscope moléculaire, cela signifie que nous sommes en mesure d'observer le mécanisme d'activation pendant x10 plus longtemps que par le passé, " a déclaré Guros. " De nouvelles capacités de calcul peuvent fournir le pouvoir d'observer l'activation moléculaire de protéines complexes à des échelles de temps considérablement plus longues. Plus ce délai est long, la meilleure validation que nous pouvons avoir des résultats expérimentaux pour démontrer que les modèles MD sont une méthode robuste pour étudier les protéines et tester les produits pharmaceutiques. »
L'activation et la désensibilisation de protéines comme 5HT3A se produisent en quelques millisecondes, donc tout en étant plus proche de l'échelle de temps réelle, les scientifiques sont encore un peu en retard dans l'observation de l'ensemble du cycle de transport de la protéine. Cette étude, cependant, a pu donner un aperçu des effets de la liaison de la sérotonine sur le développement d'un état préactif de 5HT3A et de la manière dont la diversité des lipides membranaires influence la structure et la fonction des protéines.
Il reste beaucoup d'espace de simulation à explorer avec ces modèles, et cela n'a été rendu possible que ces dernières années grâce aux progrès de la puissance de calcul. Spécifiquement, cette étude a été réalisée à l'aide d'une allocation basée sur une subvention sur le superordinateur Anton2 maintenu par le Pittsburgh Supercomuting Center (PSC) et parrainé par la recherche DE Shaw. Les ressources de calcul traditionnelles de haute performance ne seraient pas capables d'atteindre les échelles de temps de cette étude.
À mesure que la vitesse et la puissance de calcul augmenteront à l'avenir, le groupe espère étudier les effets des produits pharmaceutiques, comme le granisétron ou l'ondansétron, dans le but de modéliser avec précision leurs effets sur la protéine et d'étudier d'autres thérapies ciblées.