
Crédit:UC San Diego Jacobs School of Engineering
Les améliorations apportées à une classe d'électrolyte de batterie introduite pour la première fois en 2017 - les électrolytes à gaz liquéfié - pourraient ouvrir la voie à une avancée à fort impact et recherchée depuis longtemps pour les batteries rechargeables :le remplacement de l'anode en graphite par une anode lithium-métal.
La recherche, publié le 1er juillet 2019 par la revue Joule , s'appuie sur les innovations signalées pour la première fois dans Science en 2017 par le même groupe de recherche de l'Université de Californie à San Diego et la spin-out universitaire South 8 Technologies.
Trouver des moyens rentables de remplacer l'anode en graphite dans les batteries lithium-ion commerciales est d'un grand intérêt car cela pourrait conduire à des batteries plus légères capables de stocker plus de charge, via une augmentation de 50 pour cent de la densité énergétique au niveau cellulaire. L'augmentation de la densité énergétique proviendrait d'une combinaison de facteurs, notamment la capacité spécifique élevée de l'anode lithium-métal, faible potentiel électrochimique, et poids léger (faible densité).
Par conséquent, le passage aux anodes lithium-métal étendrait considérablement l'autonomie des véhicules électriques et réduirait le coût des batteries utilisées pour le stockage en réseau, a expliqué Shirley Meng, professeur de nano-ingénierie à l'UC San Diego, un auteur correspondant sur le nouveau papier dans Joule .
Cependant, faire le changement s'accompagne de défis techniques. Le principal obstacle est que les anodes au lithium métal ne sont pas compatibles avec les électrolytes conventionnels. Deux problèmes de longue date surviennent lorsque ces anodes sont associées à des électrolytes conventionnels :une faible efficacité de cyclage et la croissance de dendrites.
L'approche de Meng et de ses collègues était donc de passer à un électrolyte plus compatible, appelés électrolytes gazeux liquéfiés.
Électrolytes de gaz liquéfiés en action
L'un des aspects alléchants de ces électrolytes gazeux liquéfiés est qu'ils fonctionnent à la fois à température ambiante et à des températures extrêmement basses, jusqu'à moins 60 C. Ces électrolytes sont fabriqués à partir de solvants gazeux liquéfiés - des gaz liquéfiés sous des pressions modérées - qui sont beaucoup plus résistants au gel que les électrolytes liquides standard.
Crédit:UC San Diego Jacobs School of Engineering
Dans l'article 2019 de Joule , les chercheurs rapportent comment, par des études expérimentales et informatiques, ils améliorent leur compréhension de certaines des lacunes de la chimie des électrolytes des gaz liquéfiés. Avec cette connaissance, ils ont pu adapter leurs électrolytes de gaz liquéfiés pour améliorer les performances des paramètres clés des anodes lithium-métal, à la fois à température ambiante et moins 60 C.
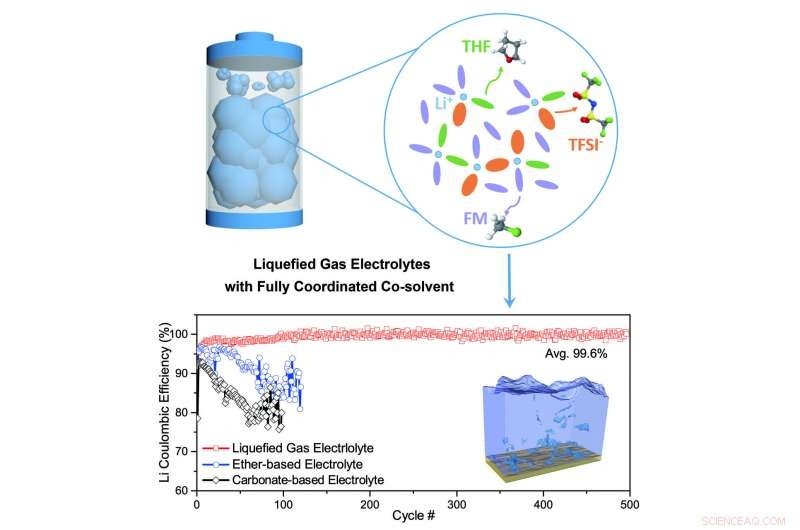
Dans les tests de demi-cellule lithium-métal, l'équipe rapporte que l'efficacité de cyclage de l'anode (efficacité coulombienne) était de 99,6 pour cent pour 500 cycles de charge à température ambiante. Il s'agit d'une augmentation par rapport à l'efficacité de cyclisme de 97,5% signalée dans le 2017 Science papier, et une efficacité de cycle de 85 pour cent pour les anodes au lithium métal avec un électrolyte (liquide) conventionnel.
A moins 60 C, l'équipe a démontré une efficacité de cycle d'anode lithium-métal de 98,4 %. En revanche, la plupart des électrolytes conventionnels ne fonctionnent pas en dessous de moins 20 C.
Les outils de simulation et de caractérisation de l'équipe de l'UC San Diego, beaucoup développés dans le laboratoire de stockage et de conversion d'énergie dirigé par Shirley Meng, permettre aux chercheurs d'expliquer pourquoi les anodes au lithium métal fonctionnent mieux avec des électrolytes gazeux liquéfiés. Au moins une partie de la réponse a à voir avec la façon dont les particules de lithium se déposent sur la surface de l'anode métallique.
Les chercheurs rapportent le dépôt lisse et compact de particules de lithium sur des anodes lithium-métal lors de l'utilisation d'électrolytes gazeux liquéfiés. En revanche, lorsque des électrolytes conventionnels sont utilisés, des dendrites en forme d'aiguille se forment sur l'anode de lithium métallique. Ces dendrites peuvent dégrader l'efficacité, provoquer des courts-circuits, et conduire à de graves menaces pour la sécurité.
Une mesure de la densité du dépôt des particules de lithium sur les surfaces des anodes est la porosité. Plus la porosité est faible, mieux c'est. L'équipe de recherche rapporte en Joule que la porosité du dépôt de particules de lithium sur une anode métallique est de 0,90 % à température ambiante en utilisant des électrolytes gazeux liquéfiés à température ambiante. La porosité en présence d'électrolytes conventionnels grimpe à 16,8 pour cent.
La course au bon électrolyte
Il y a actuellement un gros effort pour trouver ou améliorer des électrolytes compatibles avec l'anode métal lithium et compétitifs en termes de coût, sécurité, et plage de température. Les groupes de recherche se sont principalement intéressés aux solvants très concentrés (liquides) ou aux électrolytes solides, mais il n'y a actuellement pas de solution miracle.
"En tant que membre de la communauté de recherche sur les batteries, Je suis convaincu que nous allons développer les électrolytes dont nous avons besoin pour les anodes lithium-métal. J'espère que cette recherche inspirera plus de groupes de recherche à se pencher sérieusement sur les électrolytes de gaz liquéfiés, " a déclaré Meng.
Meng est également l'auteur correspondant d'un article connexe dans le numéro de mai 2019 de Tendances en chimie "Problèmes clés entravant une anode lithium-métal pratique."