
Crédit :pexels/CC0
Le développement et l'amélioration des produits pharmaceutiques jouent un rôle central dans la bataille en cours contre les maladies humaines. La synthèse organique est le domaine qui permet ces développements car elle offre la boîte à outils pour diversifier les structures chimiques. Le groupe de Nuno Maulide, récemment nommé Scientifique de l'année 2018 en Autriche, en collaboration avec le groupe de Harald Sitte, a maintenant rapporté une méthode facile pour le remplacement de l'hydrogène par du fluor dans des molécules médicamenteuses importantes. Cette nouvelle découverte permet d'affiner les produits pharmaceutiques existants (et potentiellement nouveaux) afin de les doter de propriétés pharmacologiques améliorées. Les résultats ont été récemment publiés dans la célèbre revue Chimie de la nature .
La grande majorité des produits pharmaceutiques employés dans le traitement des maladies humaines sont de nature organique, ce qui signifie que le composant actif est une molécule (ou une combinaison de plusieurs molécules) constituée d'atomes de carbone et d'hydrogène. Ce trait est commun à toute matière vivante, comme protéines, sucres, les graisses et l'ADN sont également basés sur de tels squelettes hydrocarbonés, ne différant que par l'arrangement et leur substitution par une quantité relativement faible d'autres éléments possibles (principalement l'oxygène, azote, soufre et phosphore). "Nos corps ne sont rien d'autre qu'un grand assemblage de milliards de carbone fabriqué, ou en d'autres termes, molécules organiques", dit Nuno Maulide, récemment nommé Scientifique de l'année 2018 en Autriche et professeur à l'Université de Vienne. En raison de cette similitude, les produits pharmaceutiques biologiques sont parfaitement adaptés pour interagir avec le corps humain, par exemple en se liant à des récepteurs déclenchant ou inhibant ainsi une fonction souhaitée ou non souhaitée.
Trouver la clé qui correspond le mieux à la serrure
La conception d'une molécule pharmaceutique ciblant une interaction spécifique avec une structure réceptrice est souvent conceptualisée par l'analogie d'un verrou et d'une clé. "Le récepteur (par exemple une enzyme) a une structure unique (verrou) et nécessite donc une structure unique (clé) avec laquelle interagir. En raison de la nécessité d'un ajustement exact, l'intégrité structurelle du composé pharmaceutique est la clé (jeu de mots!) Pour assurer sa bioactivité bénéfique", explique Harald Sitte, Professeur à l'Université de médecine de Vienne et co-auteur de l'étude.
Crédit :Université de Vienne
Essayant d'échapper au nettoyage
Cependant, tout comme les nutriments sont métabolisés par le corps, les produits pharmaceutiques qui pénètrent dans le corps (constitués des mêmes constituants essentiels, carbone, hydrogène, …) sont également dégradés par les mêmes enzymes qui métabolisent et éliminent nos constituants alimentaires. « Ce type de machine de nettoyage est indispensable à notre organisme pour se protéger; les molécules indésirables et pouvant avoir des effets négatifs doivent être éliminées rapidement. Malheureusement, une telle machinerie est souvent aveugle et les produits pharmaceutiques seront également métabolisés dès qu'ils entreront en contact avec le corps", explique Christopher Teskey, PostDoc dans le groupe Maulide et co-premier auteur de l'étude. Cela peut altérer la structure des produits pharmaceutiques et donc également supprimer leurs propriétés bénéfiques. "Une grande partie de cette dégradation se produit précisément à la jonction des atomes de carbone et d'hydrogène (liaisons C-H), qui peuvent être brisés ou modifiés pour former de nouveaux composés qui peuvent être plus facilement éliminés du corps par excrétion. Les liaisons C-H sont par nature des liaisons plutôt faibles, ce qui signifie que l'oxydation peut avoir lieu facilement", explique Pauline Adler, ancien PostDoc du groupe Maulide et autre co-premier auteur de l'étude. "C'est finalement une course pour échapper au nettoyage ! Plus un médicament bénéfique peut échapper à cette chasse au chat et à la souris avec les enzymes du métabolisme, plus longtemps son effet bénéfique peut être ressenti dans le corps", plaisante Maulide.
Une solution astucieuse :échanger H avec F peut être un 2-en-1
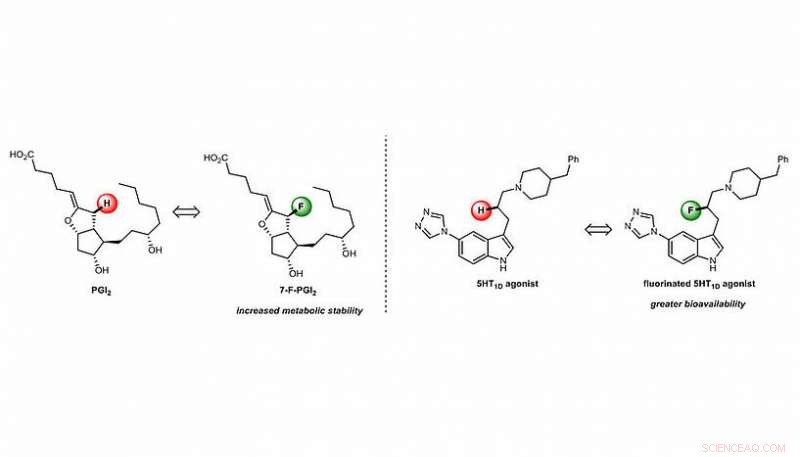
Il est donc évident que, si les points faibles structurels des molécules médicamenteuses pouvaient être éliminés ou atténués, leur stabilité métabolique pourrait être considérablement augmentée. Les chimistes ont découvert il y a quelques années que le remplacement stratégique de liaisons C-H particulièrement faibles par des liaisons C-F beaucoup plus fortes peut être une approche très enrichissante dans cette direction. Alors que l'hydrogène et le fluor sont distinctement différents à certains égards, leurs tailles sont comparables, et le remplacement de H par F peut donc souvent être supposé n'avoir qu'un effet minime sur la structure de la clé (pharmaceutique). "Encore plus alors, en raison de ces propriétés électroniques différentes, un atome de fluor stratégiquement placé peut potentiellement établir des interactions supplémentaires avec sa cible (lock), améliorant ainsi l'activité souhaitée", explique Maulide. "De plus, l'introduction de fluor dans une molécule médicamenteuse peut altérer ses propriétés de manière à ce qu'il puisse être plus facilement absorbé par l'organisme (augmentation de la biodisponibilité), augmentant encore une fois la quantité de médicament qui peut trouver et interagir avec son récepteur. Cela peut vraiment être une situation 2 en 1 !", pose Daniel Kaiser, ancien doctorat étudiant du groupe Maulide et co-auteur de l'étude (Figure 1).
Crédit :Université de Vienne
Le défi de remplacer H par F :si seulement vous pouviez utiliser du dentifrice
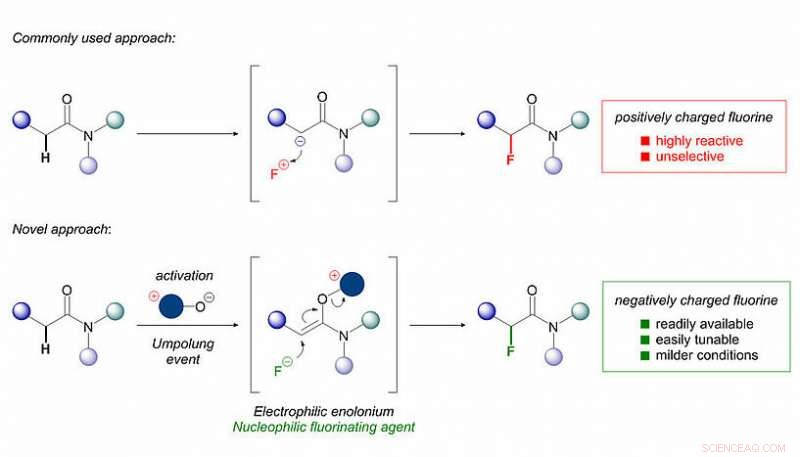
Alors que l'introduction du fluor peut avoir ce large éventail d'effets bénéfiques sur un produit pharmaceutique, son placement sur des molécules organiques est souvent loin d'être anodin. Les méthodes de fluoration les plus courantes impliquent des réactifs corrosifs et parfois toxiques. Ces réactifs sont à base d'atomes de fluor chargés positivement (F+), qui sont beaucoup plus chers et difficiles à manipuler que leurs homologues fluorés chargés négativement (F-) communs et bon marché (l'anion fluorure lui-même est communément connu, par exemple, comme constituant du dentifrice).
Une solution simple et la première démonstration
Le groupe de recherche du Pr. Nuno Maulide (Institut de Chimie Organique, Université de Vienne) a maintenant découvert une méthode facile et sélective pour l'introduction d'atomes de fluor dans des molécules organiques en utilisant l'anion fluorure largement disponible (F–). "La plupart des chimistes ont cherché à introduire le fluor en utilisant des molécules organiques polarisées négativement qui peuvent réagir avec un réactif F+. Nous avons simplement fait le contraire :inverser la polarité de la molécule organique afin que nous puissions utiliser le même fluorure que vous avez dans le dentifrice !", s'enthousiasme Maulide. Surtout, cette approche utilise des matières premières bon marché, is operationally simple and delivers high yields of the products in short amounts of time.
Credit:University of Vienna
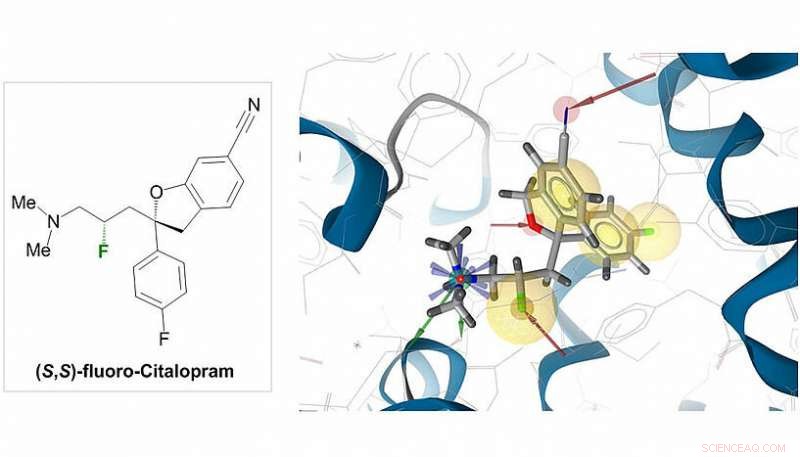
In the published work, several fluorinated analogues of common bioactive agents were easily synthesised, most prominently fluoro-Citalopram. "The parent molecule Citalopram is a blockbuster antidepressant used in the treatment of clinical depression. It interacts with the serotonin transporter (SERT) and raises the synaptic concentration of serotonin to alleviate the depressive symptoms", explains Sitte. In collaboration with the group of Prof. Harald Sitte (MedUni Vienna), Prof. Maulide and his team were able to establish that the activity of Citalopram is retained upon insertion of a fluorine atom. Significativement, while the activity is retained (despite the structural change), other pharmacological factors, such as metabolic stability and bioavailability, are expected to improve as a consequence of fluorination. The teams therefore believe that fluoro-Citalopram could present a viable alternative to the non-fluorinated analogue.
Chemistry opens the door
"Having a method to exchange H with F under such simple conditions is but the beginning. We can now imagine doing this exchange in a range of other pharmaceuticals and study the properties of the resulting, new analogues. Since the exchange of H with F is also a technique that can be of relevance to the materials industry, you can understand why we are excited about this work", explains Maulide. "This is a great example of the power of Chemistry:because we are able to manipulate the structure of matter at a molecular level with atomic precision, we can open doors that would otherwise remain closed to the imagination", closes Maulide.