Crédit :Wiley
Avec son grand nombre de formes de vie différentes, la mer est une source largement inexplorée de produits naturels qui pourraient être des points de départ pour de nouveaux produits pharmaceutiques, tels que les médicaments antitumoraux trabectédine et lurbinectine. Parce que seules de petites quantités peuvent être obtenues à partir d'organismes marins, une production synthétique est nécessaire. Dans la revue Angewandte Chemie , les scientifiques ont introduit une nouvelle, voie de synthèse efficace pour ces deux médicaments. Une étape clé est l'activation contrôlée par la lumière d'une liaison carbone-hydrogène.
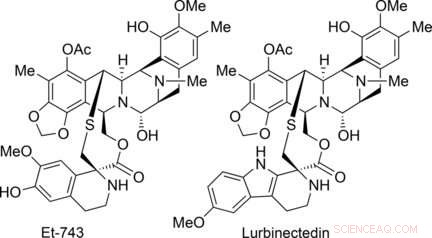
La trabectédine (également appelée ectéinascédine) provient de l'espèce d'ascidie de mer Ecteinascidia turbinata et est le premier produit naturel marin à être utilisé en clinique comme médicament pour le traitement du sarcome avancé des tissus mous. La lurbinectine a une structure légèrement modifiée et est actuellement en études cliniques de phase III pour le traitement de certains cancers du poumon et du sein. Une tonne d'ascidies est nécessaire pour acquérir environ un gramme de trabectédine. Une voie de synthèse viable et efficace pour fabriquer ce médicament et des médicaments apparentés en quantités suffisantes est donc nécessaire de toute urgence. Cependant, La trabectédine s'est jusqu'à présent avérée être l'une des molécules cibles les plus difficiles dans la synthèse de produits naturels. Différentes voies de synthèse ont été proposées mais aucune n'est réellement viable. Les méthodes actuelles sont très complexes, nécessitent des réactifs coûteux et peu courants, et offrent des rendements insatisfaisants.
Des chercheurs travaillant avec Dawei Ma à l'Institut de chimie organique de Shanghai (Chine) ont maintenant décrit une voie synthétique de novo plus efficace et viable pour la trabectédine et la lurbinectine. De novo, également appelée synthèse totale, signifie que le produit naturel est entièrement synthétisé à partir de petits, matières premières communes.
La synthèse commence avec l'acide aminé S-tyrosine et se compose de 26 étapes individuelles. D'abord, plusieurs étapes sont utilisées pour produire un intermédiaire, qui agit comme matériau de départ pour la production séparée des deux moitiés de la molécule cible - Trabectédine ou Lurbinectine. Ceux-ci sont ensuite liés ensemble dans une étape de réaction ultérieure.
L'étape clé de la synthèse est l'activation contrôlée par la lumière d'une liaison carbone-hydrogène normalement non réactive (activation C-H à distance). Un mécanisme de réarrangement radical conduit à une fermeture de cycle dans laquelle un groupe quinone est converti en un 1, unité 3-benzodioxole, qui est un composant structurel présent dans de nombreux produits naturels. La réaction était particulièrement efficace sous irradiation avec de la lumière bleue dans le solvant tétrahydrofurane.
Les scientifiques espèrent que leur voie de synthèse offre une méthode pratique et économique pour la production de trabectédine et de lurbinectine, enfin fournir un approvisionnement adéquat de ces médicaments antitumoraux marins complexes.