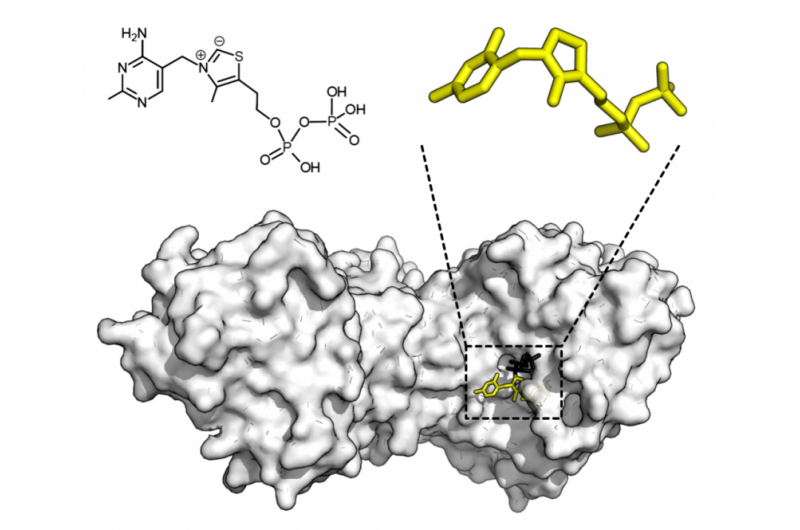
Structure chimique du pyrophosphate de thiamine et structure protéique de la transcétolase. Cofacteur thiamine pyrophosphate en jaune et substrat xylulose 5-phosphate en noir. Crédit :Thomas Shafee/Wikipédia
Des chercheurs des départements de chimie et d'ingénierie de l'Université d'Oxford ont trouvé un moyen général de prédire l'activité enzymatique. Les enzymes sont les catalyseurs protéiques qui remplissent la plupart des fonctions clés de la biologie. Publié dans Nature Chimie Biologie , la nouvelle approche d'IA des chercheurs est basée sur la séquence de l'enzyme, ainsi que le criblage d'un « ensemble d'apprentissage » défini de substrats et les bons paramètres chimiques pour les définir.
Les enzymes sont la cible de nombreux médicaments. Si les scientifiques peuvent prédire leurs fonctions, ils peuvent ensuite inhiber ces fonctions avec de petites molécules, dans certains cas pour traiter une maladie. Cette recherche sera essentielle pour créer une image holistique qui fournira une compréhension plus complète et plus complète de la biologie et de la santé.
Les chercheurs se sont attaqués à toute une famille d'enzymes d'une espèce végétale. Ils ont combiné l'expression à haut débit des enzymes des gènes correspondants, puis criblé leur activité enzymatique par quantitatif, spectroscopie de masse sans marqueur. Une simple analyse de la séquence primaire de l'enzyme ne donne aucun modèle réel de prédiction d'activité, mais lorsqu'il est combiné avec les techniques d'IA du Machine Learning Group de l'Université d'Oxford, les descripteurs chimiques standard peuvent dériver un système fortement prédictif.
Ben Davis, Le professeur de chimie à l'Université d'Oxford dit :"L'essentiel est qu'au lieu d'être une "boîte noire", cette méthode redonne au chimiste/biologiste des prédictions réussies et les raisons de ces prédictions qui ont une signification chimique et biologique. Cela nous a à son tour permis de déterminer quelles enzymes peuvent être utilisées. en synthèse, prédire l'activité d'enzymes d'espèces très différentes (même des bactéries) et trouver comment concevoir des enzymes d'une nouvelle manière sur la base de suggestions que nous n'aurions pas prédites."
Il ajoute :« Nous considérons qu'il s'agit d'un moteur de découverte très puissant. Il offrira des possibilités intrigantes pour les tests d'hypothèses. Compte tenu du récent prix Nobel de chimie dans l'évolution des enzymes en éprouvette, L'IA appliquée aux enzymes pour une meilleure compréhension pourrait s'avérer être une prochaine frontière très puissante."
Stephen Roberts, professeur d'apprentissage automatique en ingénierie de l'information à l'Université d'Oxford déclare :« Nous vivons à une époque de big data et de big models, mais pas nécessairement de grande connaissance ou perspicacité. En effet, la nature de nombreux complexes, les modèles performants masquent les détails du succès, conduisant à des solutions « boîte noire » qui manquent d'interprétabilité immédiate. En contraste frappant, la méthode scientifique construit l'extraction d'insights dans son noyau. Dans cette recherche, nous avons montré que les modèles qui offrent transparence et perspicacité sont toujours capables de conduire des avancées scientifiques. »
Cette avancée majeure permet de prédire avec succès l'activité des catalyseurs protéiques, ce qui a des implications dans un large éventail de domaines, y compris la recherche médicale. C'est un domaine nettement plus difficile que la modélisation de catalyseurs à petites molécules qui a été jusqu'à présent le summum de l'apprentissage automatique/de la chimie.