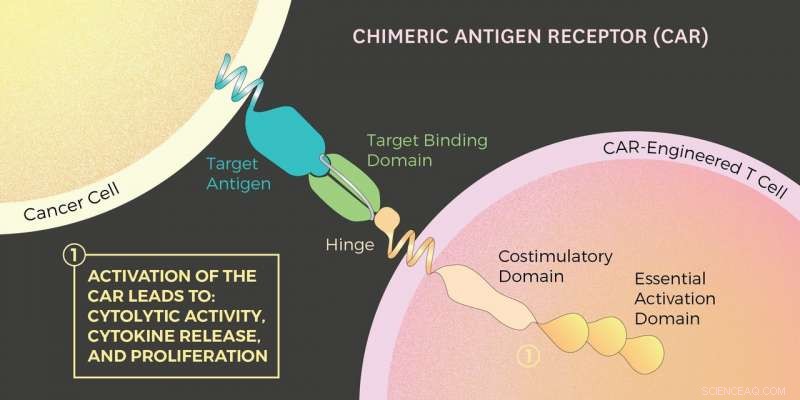
Illustration du récepteur d'antigène chimérique (CAR). Crédit :Madelin Lum/USC Viterbi School of Engineering
Le cancer reste la deuxième cause de décès aux États-Unis. Cette année, on estime que 1,7 million de nouveaux cas seront diagnostiqués, avec près de 610, 000 personnes devraient mourir de la maladie, selon l'Institut national du cancer.
Heureusement, plusieurs traitements récents contre le cancer sont très prometteurs. Parmi eux se trouve la thérapie cellulaire T par récepteur d'antigène chimérique (CAR), que l'American Society of Clinical Oncology a récemment nommé « l'avance de l'année 2018 ». Trois chercheurs de l'USC Viterbi School of Engineering—Professeur adjoint Stacey Finley, Le professeur Pin Wang et le professeur adjoint Nick Graham viennent de publier un article dans Journal biophysique qui éclaire le fonctionnement de ce nouveau traitement, des informations qui pourraient un jour aboutir à de meilleures thérapies contre le cancer avec moins d'effets secondaires.
"Nous essayons de creuser dans les mécanismes moléculaires, " dit Graham, professeur adjoint de génie chimique et de science des matériaux. "En comprenant le fonctionnement des cellules CAR T, nous pourrions essayer d'en concevoir de meilleurs."
Lorsque le système immunitaire fonctionne normalement, les cellules immunitaires se déplacent dans le corps et recherchent des agents pathogènes qui ne leur appartiennent pas et les tuent. Cependant, les cellules cancéreuses peuvent se masquer, ce qui rend la tâche plus difficile pour les bonnes cellules, comme les cellules T, pour les tuer.
Avec la thérapie cellulaire CAR T, les cellules T d'une personne sont retirées, génétiquement modifié avec des protéines, puis réinjecté au patient. Les cellules CAR T qui en résultent sont bien meilleures pour lutter contre les cellules cancéreuses. C'est parce que ces cellules CAR T modifiées ont un récepteur protéique modifié, la voiture, qui peuvent se lier aux cellules cancéreuses. Lorsque cela se produit, un signal du CAR indique à la cellule T de commencer à détruire le cancer en sécrétant les substances chimiques perforine et granzyme.
Thérapies cellulaires CAR T
Plus tôt cette année, la Food and Drug Administration des États-Unis a approuvé la première thérapie cellulaire CAR T pour le traitement de certaines personnes atteintes de leucémie avancée et d'une forme de lymphome, les deux cancers du sang. Les premiers résultats se sont révélés très prometteurs. Cependant, dans les premiers tests, les thérapies cellulaires CAR-T se sont jusqu'à présent avérées beaucoup moins efficaces contre le sein, poumon, cancer de la prostate et autres tumeurs solides. En outre, certaines personnes suivant une thérapie cellulaire CAR T ont ressenti des effets secondaires importants; quelques-uns sont même morts.
Le trio de chercheurs de l'USC espère que leurs travaux amélioreront considérablement les thérapies cellulaires CAR T en découvrant le processus compliqué par lequel les CAR activent les cellules combattant le cancer. Spécifiquement, ils examinent un processus appelé phosphorylation, qui est une réaction chimique qui se produit lorsque le récepteur CAR se heurte à une cellule cancéreuse et envoie un signal à la cellule T pour attaquer les mauvaises cellules.
"Je pense que ce qui est le plus excitant, c'est que nous ajoutons vraiment au terrain une compréhension des sites de la RCA qui deviennent phosphorylés, à quelle vitesse cela se produit et la quantité de phosphorylation de chaque site, " dit Finley, le Gordon S. Marshall Early Career Chair et professeur adjoint de génie biomédical, génie chimique et science des matériaux et sciences biologiques.
A travers leurs recherches, Finley, Wang et Graham ont appris quand et combien de phosphorylation se produit sur les six sites de la RCA, lequel, dans une analogie imparfaite, pourraient être imaginés comme des « hubs d'amarrage, " selon les mots de Graham.
En outre, ils ont découvert qu'il n'existe pas de "gardien", ce qui signifie qu'aucun site CAR ne doit être phosphorylé avant les autres. Jusqu'à maintenant, les chercheurs n'avaient qu'une idée générale du processus de phosphorylation, rendant difficile la bio-ingénierie des cellules CAR T qui pourraient lutter avec succès contre des seins complexes et compliqués, cancer du poumon et autres tumeurs solides.
De meilleures CAR pour lutter contre le cancer
Aller de l'avant, Finley, Wang et Graham espèrent tirer parti de leurs découvertes pour concevoir des RAC plus efficaces contre le cancer avec moins d'effets secondaires. Cela pourrait signifier que la phosphorylation ait lieu plus rapidement et plus intensément sur certains sites CAR, en fonction de la complexité des cellules cancéreuses ciblées. Alternativement, les chercheurs de l'USC pourraient concevoir des CAR pour qu'ils phosphorylent moins, empêchant ainsi les cellules T qui combattent le cancer et d'autres de devenir trop agressives et de tuer les cellules saines, un problème qui a surgi avec les premiers traitements du cancer à cellules CAR T.
Déjà, Finley a construit des modèles quantitatifs très prometteurs.
« Une fois que nous aurons ces outils et modèles quantitatifs, nous devrions être en mesure de les appliquer à une variété de conceptions différentes de RAC, " dit Finley, dont le groupe de recherche possède une expertise en modèles mathématiques. "Peut-être pourriez-vous utiliser un modèle, avant de faire une expérience, pour voir si ce nouveau design fonctionnerait. Au lieu d'avoir à faire autant d'expériences fastidieuses en laboratoire, vous pourriez créer un modèle mathématique prédictif pour sélectionner le meilleur design."
Ajouté Wang, le Zohrab A. Kaprielian Fellow in Engineering et professeur de génie chimique et de science des matériaux, et génie biomédical :« Si vous voulez rendre les cellules T plus puissantes, la question est de savoir comment concevoir au mieux la RCA. C'est le but de notre recherche, Je pense."