Crédit :Wiley
Les réactions couplées de transfert d'oxygène et de transfert d'électrons qui utilisent des cofacteurs sont des réactions enzymatiques d'une importance cruciale pour toutes les formes de vie, des bactéries aux vertébrés. Dans le Journal européen de chimie inorganique , les scientifiques ont introduit un modèle pour l'enzyme sulfite oxydase. Il est basé sur un complexe de molybdène dont les ligands spéciaux peuvent être oxydés pour permettre le couplage du transfert d'oxygène à un substrat avec un transfert d'électrons intramoléculaire. Les intermédiaires contenant des ions molybdène(V) jouent un rôle essentiel.
De nombreuses enzymes ne fonctionnent pas seules; ils nécessitent des cofacteurs, des composants non protéiques qui jouent un rôle dans le transfert d'électrons. Ceux-ci impliquent souvent des ions métalliques, comme le fer dans les cytochromes ou l'oligo-élément molybdène, qui se trouve dans les molybdène oxotransférases, enzymes qui transfèrent les atomes d'oxygène aux substrats. Un représentant important de ce dernier est la sulfite oxydase, qui oxyde le sulfite toxique pour faire du sulfate. Le transfert d'oxygène implique un changement de l'état d'oxydation du molybdène de tétravalent (MoIV) à pentavalent (MoV). Les électrons impliqués sont éliminés au moyen de cytochromes et utilisés pour la production d'ATP. Le molybdène pentavalent (MoV) semble être un intermédiaire dans la réaction.
Des chercheurs travaillant avec Katja Heinze à l'Université de Mayence ont maintenant développé une approche conceptuelle pour stabiliser et caractériser spectroscopiquement les intermédiaires prédits dans les réactions des oxotransférases contenant du Mo en utilisant des systèmes modèles. Ils utilisent une méthode qui est également utilisée dans le contrôle des catalyseurs :ils attachent un « commutateur » moléculaire avec un état d'oxydation contrôlable.
Les chercheurs ont choisi d'utiliser le couple redox ferrocène/ferrocénium, dans lequel un atome de fer est pris en sandwich entre deux chargés négativement, aromatique, cycles de carbone à cinq chaînons. L'ion fer peut basculer entre un état avec une double charge positive (FeII, ferrocène) et un triplement chargé positivement, état oxydé (FeIII, ferrocénium). Ceci est analogue aux cofacteurs cytochromes naturels, qui peut également contenir FeII ou FeIII. Les chercheurs ont attaché deux de ces « commutateurs » ferrocène/ferrocénium à un complexe de molybdène comme modèle pour le centre actif d'une sulfite oxydase. Le molybdène est à l'état d'oxydation VI et possède deux atomes d'oxygène liés par des doubles liaisons. La réaction avec un phosphane organique (une molécule de phosphore-hydrocarbure) comme substrat modèle accepteur d'oxygène se produit à des vitesses variables, en fonction des charges sur les "commutateurs", car le statut redox des substituants ferrocényle module les barrières énergétiques pour certains intermédiaires. Il en résulte une variété d'adduits entre le complexe Mo et le phosphane.
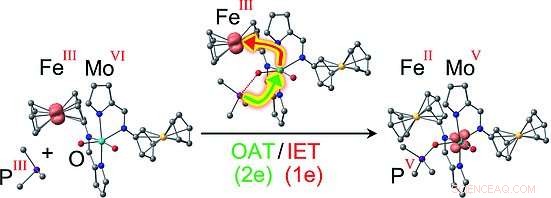
Les versions les plus intéressantes sont celles avec deux ions FeIII ou un FeII et un ion FeIII :Dans ces cas, le mécanisme n'est plus un simple transfert d'un atome d'oxygène au substrat, comme pour la version FeII/FeII. Au lieu de cela, il est couplé à un transfert d'électrons intramoléculaire, peut-être conceptuellement similaire à celui des sulfites oxydases naturelles. Au cours de la réaction de transfert d'oxygène, un électron est transféré du molybdène à l'un des ions FeIII, résultant en une distribution de charge de FeII FeIII MoV ou FeII FeII MoV. Pour cette dernière version, les chercheurs ont pu utiliser la spectroscopie par résonance de spin électronique pour détecter sans ambiguïté l'intermédiaire MoV FeII FeII MoV avec le substrat oxydé (le produit) encore lié à celui-ci. Le couplage du transfert d'oxygène à un transfert d'électrons intermoléculaire abaisse la barrière d'activation pour cette étape réactionnelle et stabilise simultanément l'intermédiaire MoV, comme prévu par les modèles informatiques.
Les chercheurs proposent d'utiliser ce nouveau système comme modèle pour les étapes de transfert d'atomes d'oxygène et de transfert d'électrons intramoléculaires dans les sulfites oxydases, et espèrent utiliser ce nouveau concept pour développer des analogues pour d'autres réactions enzymatiques avec transfert d'électrons couplé. À l'avenir, il semble également possible d'étendre ce concept à des réactions catalytiques commutables qui n'ont pas de prototype naturel.