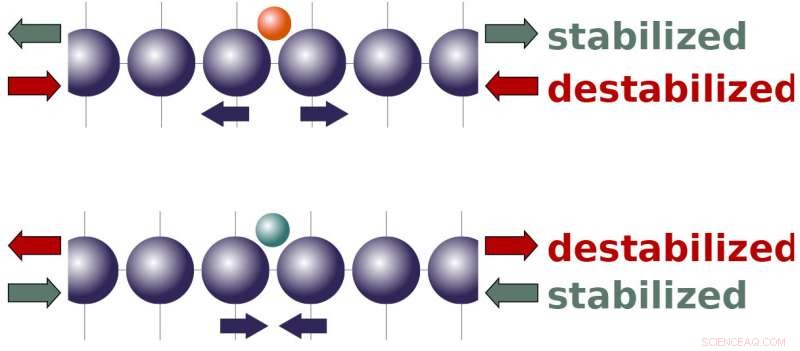
Des chercheurs de l'Université Brown ont montré que les effets de la contrainte externe sur un catalyseur dépendent de la contrainte interne exercée par les réactifs chimiques. Ce nouveau cadre théorique pourrait être utile pour optimiser les catalyseurs pour différentes réactions. Crédit :laboratoire Peterson / Université Brown
Des chercheurs de l'Université Brown ont développé une nouvelle théorie pour expliquer pourquoi l'étirement ou la compression des catalyseurs métalliques peut les rendre plus performants. La théorie, décrit dans le journal Catalyse naturelle , pourrait ouvrir de nouvelles possibilités de conception pour de nouveaux catalyseurs dotés de nouvelles capacités.
Les catalyseurs sont des substances qui accélèrent les réactions chimiques. La grande majorité de la catalyse industrielle implique des surfaces solides, souvent des métaux, qui catalysent des réactions dans des liquides ou des gaz. Un pot catalytique sur une voiture, par exemple, utilise des catalyseurs métalliques pour éliminer les toxines des gaz d'échappement. Il existe également un intérêt à utiliser des catalyseurs métalliques pour convertir le dioxyde de carbone en carburants, fabriquer des engrais à partir de l'azote atmosphérique et entraîner des réactions dans des voitures à pile à combustible.
La recherche de ces dernières années a montré que l'application d'une contrainte aux catalyseurs métalliques - soit en compression soit en tension - peut dans certains cas modifier leur comportement.
« La souche est un sujet très brûlant en catalyse en ce moment, " a déclaré Andrew Peterson, professeur adjoint à la Brown's School of Engineering et co-auteur de la recherche. "Nous commençons à voir des choses se produire sous pression qui ne s'expliquent pas facilement par la théorie traditionnelle du fonctionnement des catalyseurs. Cela nous a fait réfléchir à un cadre alternatif pour cette question."
Un catalyseur métallique fonctionne en provoquant la liaison des réactifs à sa surface, un processus connu sous le nom d'adsorption. L'adsorption rompt les liaisons chimiques des molécules réactives, permettant à différentes étapes d'une réaction chimique de se dérouler à la surface du métal. Une fois les étapes de réaction terminées, le produit final est libéré du catalyseur par le processus inverse, appelé désorption.
La propriété clé d'un catalyseur est sa réactivité, ce qui signifie à quel point il lie étroitement les molécules chimiques à sa surface. Les catalyseurs doivent être quelque peu réactifs pour que la liaison se produise, mais pas trop réactif. Trop de réactivité fait que le catalyseur retient trop étroitement les molécules, ce qui peut gêner certaines étapes de la réaction ou faire en sorte que les produits finaux ne puissent pas se désorber.
Il a été démontré ces dernières années que l'application d'une contrainte sur un catalyseur peut ajuster sa réactivité, et il existe une théorie bien établie sur son fonctionnement. En général, la théorie prédit que la contrainte de traction devrait augmenter la réactivité, tandis que la compression devrait le réduire. Cependant, Peterson et son groupe ont continué à rencontrer des systèmes qui ne s'expliquent pas facilement par la théorie.
Cela a amené les chercheurs à réfléchir à une nouvelle façon de voir le problème. La théorie traditionnelle décrit les choses au niveau des électrons et des bandes d'électrons. La nouvelle théorie fait un zoom arrière, en se concentrant plutôt sur la mécanique de la façon dont les molécules interagissent avec le réseau atomique d'un catalyseur.
Peterson et son équipe ont montré que les molécules liées à la surface d'un catalyseur auront tendance soit à séparer les atomes du réseau, soit à les rapprocher, en fonction des caractéristiques des molécules et des sites de liaison. Les différentes forces produites par les molécules ont des implications intéressantes sur la façon dont la contrainte externe devrait affecter la réactivité d'un catalyseur. Cela suggère que la tension, qui étire le réseau atomique d'un catalyseur, devrait rendre un catalyseur plus réactif aux molécules qui veulent naturellement séparer le réseau. À la fois, la tension devrait diminuer la réactivité pour les molécules qui veulent rassembler le réseau. La compression, c'est-à-dire la compression du réseau, a un effet inverse.
La nouvelle théorie aide non seulement à expliquer des résultats auparavant déroutants, il fait de nouvelles prédictions importantes. Spécifiquement, il prédit un moyen de briser les relations d'échelle traditionnelles entre les catalyseurs et les différents types de molécules.
"Les relations d'échelle signifient que, dans des circonstances normales, lorsque vous augmentez la réactivité d'un catalyseur pour un produit chimique, il augmente également la réactivité pour d'autres produits chimiques, " Peterson a dit. " De même, si vous diminuez la réactivité pour un produit chimique, vous le diminuez pour les autres."
Ces relations d'échelle entraînent des compromis gênants lors de la tentative d'optimisation d'un catalyseur. Obtenir la réactivité parfaite pour un produit chimique pourrait amener un autre produit chimique à se lier trop étroitement (ou trop lâchement), potentiellement inhiber certaines étapes d'une réaction. Mais cette nouvelle théorie suggère que la contrainte peut briser ces relations d'échelle, permettant à un catalyseur de lier simultanément un produit chimique plus étroitement et un autre plus lâchement, en fonction de l'interaction naturelle du produit chimique avec le réseau atomique du catalyseur et de la manière dont le champ de contrainte est conçu sur la surface du catalyseur.
« Maintenant, vous pouvez commencer à réfléchir à un réglage très fin des catalyseurs pour qu'ils fonctionnent mieux à travers les différentes étapes de réaction, " Peterson a déclaré. "Cela pourrait considérablement améliorer les performances d'un catalyseur, selon les produits chimiques impliqués.
L'équipe de Peterson a commencé à constituer une base de données de produits chimiques de réaction courants et de leurs interactions avec différentes surfaces de catalyseur. Cette base de données pourrait servir de guide pour trouver des réactions qui pourraient bénéficier de la tension et de la rupture des relations d'échelle.
En attendant, Peterson espère que le travail qu'ils ont fait jusqu'à présent fournira à cette communauté de catalyse une nouvelle façon de penser à la contrainte.
"Nous essayons de donner un cadre qui permet de comprendre plus intuitivement comment la contrainte fonctionne en catalyse, " a déclaré Peterson. " Alors que les gens conçoivent de nouveaux catalyseurs, ils peuvent penser à des moyens de mieux exploiter ces effets de contrainte."