
Un type modifié de la protéine Eos peut devenir fluorescent lorsqu'il est illuminé par une lumière laser bleue et rouge. Fond :deux protéines du cytosquelette en bleu et rouge. La protéine visible en rouge a été marquée avec le nouveau type Eos modifié. (Montage :Mohr MA et al. Angewandte Chemie 2017. Copyright Wiley-VCH. Reproduit avec permission)
Les scientifiques ont identifié le mécanisme qui permet aux protéines fluorescentes de changer de couleur en deux phases. Ils jettent ainsi les bases de nouvelles applications en microscopie et en analyses fonctionnelles en recherche biologique.
Tout a commencé avec une observation que les scientifiques de l'ETH ont faite il y a environ deux ans avec une protéine fluorescente spéciale isolée des coraux, Dendra 2, qui émet une fluorescence verte. La lumière peut être utilisée pour modifier sa structure moléculaire afin qu'elle passe au rouge. Les chercheurs ont découvert une nouvelle façon d'induire ce changement de couleur :il est brièvement excité par une impulsion de lumière laser bleue, puis illuminé immédiatement par une lumière proche infrarouge. Les applications de ce commutateur de couleur à deux phases incluent la microscopie à fluorescence.
Une équipe internationale de chercheurs dirigée par Periklis Pantazis, du Département de science et ingénierie des biosystèmes (D-BSSE) de l'ETH Zurich à Bâle, a maintenant expliqué ce mécanisme de commutation de couleur à deux phases. Les scientifiques appellent cela une "conversion amorcée". Les nouvelles connaissances permettent aux chercheurs de modifier d'autres protéines sensibles à la lumière afin qu'elles puissent également être excitées en deux phases.
Les chercheurs de l'ETH Zurich, l'Institut de technologie de Karlsruhe, et le Janelia Research Campus à Ashburn, Virginie, examiné de près les protéines activées par la lumière bleue et réussi à montrer que ces protéines entrent dans un état excité durant plusieurs millisecondes. "C'est relativement long, " explique Pantazis. " D'autres phénomènes de fluorescence sont beaucoup plus courts. "
Les scientifiques ont également démontré que cet état est un cas d'un phénomène connu de la chimie quantique, un "état triplet". Après environ cinq millisecondes, la protéine fluorescente Dendra 2 revient à son état fondamental. La conversion amorcée ne se produit que si la deuxième phase - l'éclairage avec une lumière proche infrarouge - se produit dans la fenêtre temporelle triplet.
Séquences d'acides aminés modifiées
La durée de l'état triplet dépend fortement de la stabilité de la protéine fluorescente. Cette, à son tour, dépend de la séquence exacte des éléments constitutifs des protéines (acides aminés), c'est pourquoi les scientifiques ont modifié la séquence d'acides aminés de Dendra 2 à plusieurs endroits. Puis, ils ont fait de même avec une autre protéine fluorescente, Éos. Jusqu'à maintenant, cette protéine n'a pas pu être excitée en deux phases. Il est documenté dans la littérature scientifique que ces emplacements sont essentiels pour l'état triplet.
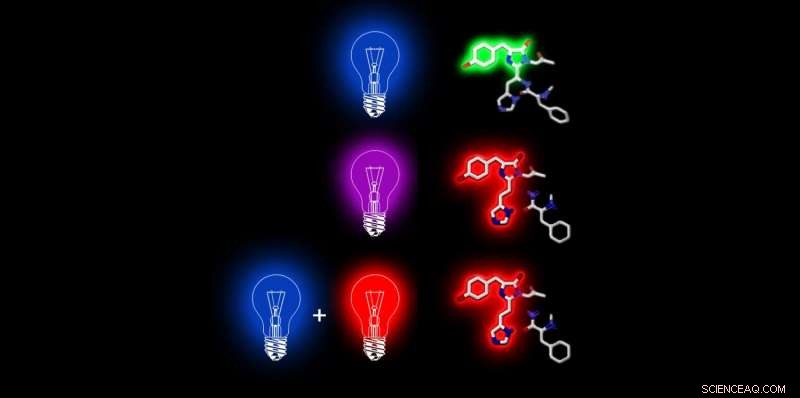
Lorsque Dendra 2 (à droite avec son composé chimique fluorescent) est éclairé par une lumière laser bleue, il émet une fluorescence verte. Avec la lumière violette, il modifie sa structure chimique de sorte qu'il ne peut qu'être fluorescent en rouge. Ce changement de structure chimique se produit également lorsqu'il est brièvement éclairé avec du bleu et immédiatement après avec de la lumière rouge (ou avec une lumière laser bleue et rouge simultanément). Crédit :ETH Zurich
Les scientifiques ont mesuré la durée de l'état triplet avec toutes les nouvelles protéines. Cet état a été étendu de manière significative dans plusieurs des protéines testées. Les scientifiques ont également pu modifier la protéine Eos afin qu'elle puisse également être activée en deux phases. Ils ont réussi à le faire avec six autres protéines qui n'avaient jamais été activées en deux phases auparavant. « Les protéines modifiées n'ont pas seulement été rendues commutables en deux phases pour la première fois ; elles sont également plus stables et donc fluorescentes plus intensément, " dit Manuel Mohr, doctorant dans le groupe Pantazis et auteur principal de l'étude.
Les scientifiques ont fait la découverte originale avec un laser qui n'est pas conventionnellement disponible, qui utilise la lumière dans le proche infrarouge. Aujourd'hui, cependant, les scientifiques ont démontré que l'effet peut également être obtenu en utilisant les mêmes lasers rouges conventionnels que l'on trouve dans chaque microscope à fluorescence. En d'autres termes, la conversion amorcée est possible avec n'importe quel microscope à fluorescence.
La conversion amorcée peut être utilisée en microscopie afin de marquer un point étroitement défini dans un échantillon de tissu. Pour ce faire, les scientifiques dirigent un faisceau laser bleu et rouge dans le tissu afin que les faisceaux se croisent en un seul point. La conversion amorcée se produit uniquement à cette intersection. "Because neither blue nor red laser light have a toxic effect, the method is ideal for living organisms, " says Pantazis. Applications with other microscopy techniques may also be possible, including super-resolution microscopy, which has been around for several years now.
Brain mapping and gene sequencing
"We now know how to modify photoconvertible proteins to make them switch in two phases, " says Pantazis. The ETH scientists are working together with protein experts to modify other fluorescent proteins used in microscopy in the same way.
The researchers recently modified proteins so that they can be split off from a gene-activating messenger in a way that allows them to be light-activated with two colours. Par exemple, they could illuminate tissue with a blue and red beam intersecting at a single point, making it possible to activate specific genes in a single cell of the tissue. Proteins that detect calcium can be modified in this way, également, and could potentially be used for 3-D brain mapping.
Biologists can ultimately use the new technique for other functional analyses in 3-D. ETH Zurich has already issued several licences for the patent, including to a start-up that plans to develop a DNA sequencing technique using a 3-D matrix.