
Ils ont joué un rôle clé dans la démonstration du comportement inhabituel du carbone :Tim Schleif (à gauche) et Joel Mieres Perez (à droite). Crédit : RUB, Marquard
Des chimistes de la Ruhr-Universität Bochum ont trouvé des preuves que les atomes de carbone ne se comportent pas seulement comme des particules mais aussi comme des ondes. Cette propriété de mécanique quantique est bien connue pour les particules légères telles que les électrons ou les atomes d'hydrogène. Cependant, les chercheurs n'ont que rarement observé la dualité onde-particule pour les atomes lourds, comme le carbone. L'équipe dirigée par le professeur Dr Wolfram Sander et Tim Schleif de la Chaire de chimie organique II avec le professeur Dr Weston Thatcher Borden, Université du nord du Texas, rapports dans la revue Angewandte Chemie .
"Notre résultat est l'un des rares exemples montrant que les atomes de carbone peuvent afficher des effets quantiques, " dit Sander. Plus précisément, les chercheurs ont observé que les atomes de carbone peuvent créer un tunnel. Ils franchissent ainsi une barrière énergétique, bien qu'ils ne possèdent pas assez d'énergie pour le faire.
Rarement observé pour les particules lourdes
Wolfram Sander explique le paradoxe :« C'est comme si un tigre sortait de sa cage sans sauter par-dessus la clôture, ce qui est beaucoup trop élevé pour lui. Mais il s'en sort quand même." Ce n'est possible que s'il se comporte comme une vague, mais pas s'il se comporte comme une particule. La probabilité qu'un objet puisse creuser un tunnel dépend de sa masse. Le phénomène peut, par exemple, être observé beaucoup plus facilement pour les électrons légers que pour les atomes de carbone relativement lourds.
Les chercheurs ont étudié la réaction tunnel en utilisant le réarrangement Cope, une réaction chimique connue depuis près de 80 ans. La matière première de la réaction, un composé hydrocarboné, est identique à la molécule du produit. Le même composé chimique existe donc avant et après la réaction. Cependant, les liaisons entre les atomes de carbone changent au cours du processus.
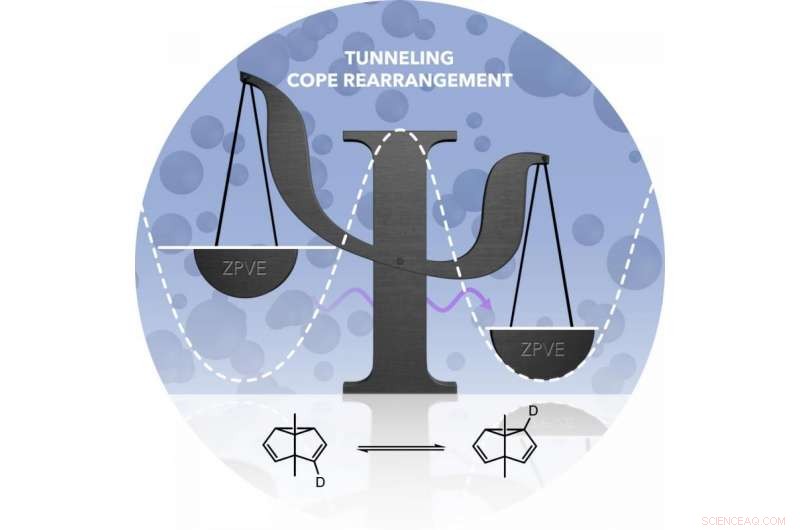
Le réarrangement Cope donne un produit identique au matériau de départ. Cependant, les deux formes ont des énergies différentes. La barrière énergétique pour le réarrangement (symbolisée par la ligne pointillée) ne peut pas être surmontée à basse température. Ce n'est que lorsque l'atome de carbone se comporte comme une onde (flèche violette) qu'il peut contourner la barrière. Crédit :Markus Henkel
Dans leur expérience, les chercheurs basés à Bochum ont marqué l'un des atomes de carbone dans la molécule :ils ont remplacé l'atome d'hydrogène qui lui était lié par l'isotope d'hydrogène deutérium, une version plus lourde de l'hydrogène. Les molécules avant et après le réarrangement de Cope différaient en termes de distribution du deutérium. En raison de ces différentes répartitions, les deux formes moléculaires avaient des énergies légèrement différentes.
La réaction ne devrait pas réellement avoir lieu
À température ambiante, cette différence a peu d'effet; en raison de l'abondante offre d'énergie thermique dans les environs, les deux formes se produisent également fréquemment. Cependant, à des températures très basses inférieures à dix Kelvin, une forme de molécule est nettement préférée en raison de la différence d'énergie. Lors du passage de la température ambiante à des températures extrêmement basses, l'équilibre doit passer d'une répartition égale des deux formes à une répartition inégale.
Cette transition ne peut, cependant, se produisent de manière classique - puisque, lors du réarrangement d'une forme à l'autre, une barrière énergétique doit être surmontée, bien que la molécule elle-même n'ait pas l'énergie pour cela et que l'environnement froid soit également incapable de la fournir. Bien que le nouvel équilibre ne doive pas se produire de manière classique, les chercheurs ont néanmoins pu le démontrer dans l'expérience. Leur conclusion :le réarrangement de Cope à des températures extrêmement basses ne peut s'expliquer que par un effet tunnel. Ils ont ainsi fourni des preuves expérimentales d'une prédiction faite par Weston Borden il y a plus de cinq ans sur la base d'études théoriques.
Les solvants influencent la capacité à creuser un tunnel
A la Ruhr-Universität, Wolfram Sander entreprend des recherches dans le pôle d'excellence Ruhr Explores Solvation, où il s'intéresse aux interactions des solvants et des molécules dissoutes. "Il est connu que les solvants influencent la capacité de tunnel, " dit le chimiste. " Cependant, jusqu'à présent, on n'a pas compris comment ils font cela."