
Crédit :Aarhus University Förster Resonance Energy Transfer (FRET) combine la lumière laser et des caméras ultra-sensibles qui envoient des signaux dans une molécule individuelle. Ce signal se propage à l'autre molécule de couleur sur la pompe, qui commence à transmettre la lumière d'une autre couleur. Le groupe se concentre sur la relation entre les différentes couleurs, qui est enregistré dans un microscope optique spécialement construit. Ces mesures fournissent des informations sur les mouvements de la pompe. Crédit :Mateusz Dyla
Pour la première fois, les chercheurs ont observé les pompes à ions qui activent le transport cellulaire et les systèmes de signalisation. Cela garantit le fonctionnement des mécanismes biomoléculaires.
Chaque pompe à calcium ne mesure que quelques nanomètres dans chaque direction, et réside dans les membranes cellulaires. Mais malgré sa petite taille, c'est essentiel à la vie. Cette pompe est la raison pour laquelle nos muscles peuvent se contracter, et que les neurones peuvent envoyer des signaux. Si la petite pompe a cessé de fonctionner, les cellules cesseraient de communiquer. C'est pourquoi les cellules utilisent une grande partie de leur énergie - environ un quart du carburant du corps, connu sous le nom d'ATP - pour maintenir les pompes en marche.
Il y a beaucoup de choses que nous ignorons encore sur la structure et la fonction de cette pompe vitale. La connaissance de la pompe est essentielle pour comprendre l'équilibre énergétique et d'autres fonctions importantes du corps.
Un groupe de recherche danois vient de publier une nouvelle étude qui montre pour la première fois comment la pompe fonctionne au niveau d'une seule molécule, et comment il garantit que les ions sont pompés dans la bonne direction. En d'autres termes, comment la pompe fonctionne comme une rue moléculaire à sens unique. La découverte vient d'être publiée dans la prestigieuse revue La nature .
"Ce travail représente la prochaine étape d'une quête profonde et importante pour comprendre la structure et la fonction atomiques de la pompe. Nous sommes maintenant un pas de plus vers la compréhension de la façon dont les pompes à ions assurent les fonctions des cellules. Nous avons caractérisé comment elles pompent les ions hors de la cellule à un niveau de détail sans précédent. L'importance d'une telle connaissance de base des processus biophysiques ne peut être que sous-estimée. Elle aura une grande influence sur notre compréhension des processus de la vie et, à l'heure, sur le traitement des maladies, " déclare le professeur Poul Nissen. Le professeur Nissen est l'un des plus grands experts mondiaux de cette famille de pompes et co-auteur de l'article.
Le filet de sécurité moléculaire
Dans une certaine mesure, l'histoire a commencé dans les années 50, lorsque le professeur Jens Christian Skou a fait son travail de pionnier à l'université d'Aarhus, qui a découvert les fonctions de pompage dans nos cellules. La pompe à calcium est une proche cousine de la pompe sodium-potassium sur laquelle Skou a travaillé, et ils utilisent un mécanisme de pompage similaire. Les travaux de Skou lui ont valu un prix Nobel de chimie en 1997. Depuis, de nombreux chercheurs ont étudié le mécanisme et la fonction de ces pompes, dont beaucoup au Center for Membrane Pumps in Cells and Disease - PUMPkin - à l'Université d'Aarhus.
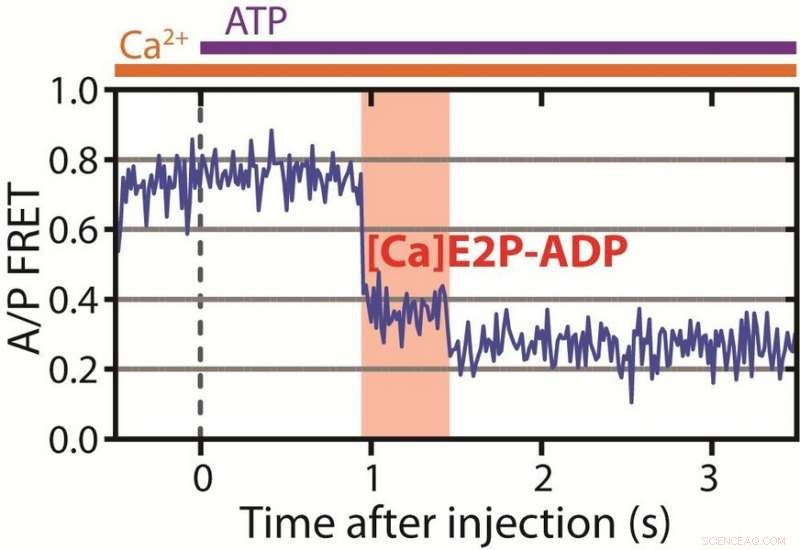
Illustré ici est la chronologie de la fonction de pompe, qui est maintenant révélé en haute résolution temporelle. La courbe montre la relation entre les couleurs fluorescentes mesurées émises par les colorants liés à la pompe. A gauche, la pompe est ouverte vers l'intérieur de la cellule et a lié des ions calcium et absorbé la molécule d'ATP - en d'autres termes, il est "chargé". La prochaine étape est la nouvelle, résultat clé :dans le champ rouge, la pompe est dans l'état fermé jusqu'alors inconnu, où il a enfermé les ions à envoyer hors de la cellule. La dernière étape illustrée montre que la pompe s'est ouverte et a libéré des ions calcium dans l'environnement. D'ici, il ne peut pas revenir à l'état en surbrillance. Crédit :Daniel Terry/Dyla
Un aperçu clé de la nouvelle publication concerne la nature à sens unique du transport d'ions. Précédemment, il a été supposé que la nature unidirectionnelle de la pompe résultait du clivage de la molécule riche en énergie ATP. L'hypothèse était que lorsque l'ATP était clivé, la pompe n'a pas pu faire marche arrière et reformer l'ATP. Cela s'est avéré incorrect.
"Nous avons identifié un nouvel état fermé dans le cycle de pompage, dans laquelle la pompe ne peut entrer que si l'ion calcium provient des fluides intracellulaires et que la pompe a clivé l'ATP. Il ne peut pas atteindre cet état si l'ion provient de l'environnement de la cellule. Lorsque le calcium est libéré de cet état, c'est le « point de non-retour ». C'est le mécanisme qui explique que la pompe fonctionne comme une pompe et pas seulement comme un canal passif. Cet aperçu vraiment unique est basé sur des expériences très avancées. Ces expériences nous permettent de voir directement la pompe faire son travail pour la première fois, " déclare le boursier postdoctoral Mateusz Dyla, le premier auteur du nouveau document.
La pompe à calcium a besoin d'énergie, qu'il obtient en clivant une molécule d'ATP. L'énergie libérée est convertie en travail de la pompe. Cela explique comment de grands gradients de concentration s'accumulent entre l'intérieur et l'extérieur de la cellule. La différence de concentration peut être supérieure à 10, 000 fois, et cette grande différence est essentielle à la communication entre les cellules comme dans la signalisation nerveuse.
Fumée et miroirs
La raison pour laquelle les expériences sont si complexes est assez claire. La pompe est si petite qu'elle ne peut pas être visualisée directement au microscope optique. Jusque là, et avec beaucoup de difficulté, les chercheurs ont créé des modèles moléculaires d'états stables de la pompe en utilisant une technique connue sous le nom de cristallographie aux rayons X. C'est l'équivalent d'un film en stop-motion. Les scientifiques ont qualifié en plaisantant leur visualisation du mouvement de la pompe entre ces états de « Pump Fiction ». La nouvelle étude, qui a duré cinq ans, déplace la visualisation du stop motion aux images en direct des mouvements fonctionnels de la pompe. L'amélioration technique des techniques microscopiques a permis d'observer le nouvel état.
La technique est connue sous le nom de spectroscopie de fluorescence à molécule unique, et utilise un phénomène connu sous le nom de transfert d'énergie de résonance de Förster, en bref FRET. Ici, une lumière laser intense et des caméras ultra-sensibles sont combinées pour permettre l'observation directe d'une seule molécule à travers la minuscule quantité de lumière émise par chaque molécule.
Le groupe de recherche a profité d'une pompe à calcium de la bactérie Listeria, qui a été préparé pour les études grâce à l'ingénierie des protéines. L'ingénierie de la protéine à elle seule a pris plusieurs années.
Dans les expériences FRET, deux molécules de colorant sont attachées à la protéine, qui est ensuite éclairé par une lumière laser. Un colorant, le donateur, absorbe la lumière laser et soit l'émet avec une couleur caractéristique, ou bien transfère l'énergie à l'autre colorant, l'accepteur. Celui-ci émettra alors de la lumière d'une autre couleur. De la lumière sera ainsi émise par les deux colorants, et les scientifiques peuvent mesurer la distance entre les deux colorants en mesurant la quantité de lumière émise par chaque couleur. Parce que les colorants ont été soigneusement insérés dans deux positions spécifiques dans la pompe, ces changements de distance suivent les mouvements de pompage de la pompe.
La technique de la molécule unique a permis les nouvelles découvertes, comme expliqué par le camarade Magnus Kjærgaard, Institut d'études avancées d'Aarhus (AIAS), qui a également contribué à la découverte.
"Nous sommes passés de 'Pump Fiction' à 'Pump Live'. Auparavant, nous avons toujours enregistré les signaux de plusieurs molécules en même temps, qui brouille les mouvements. En utilisant les techniques de FRET monomoléculaire, nous pouvons nous concentrer sur une molécule à la fois, ce qui nous permet d'observer directement les changements structurels. Cela nous fournit une vidéo de la pompe en action avec moins d'espaces. Notre film Pump Fiction a d'abord reçu son nom parce que nous savions que les transitions entre les différents états du cycle étaient fictives, et qu'il pourrait y avoir des informations supplémentaires cachées dans les écarts entre les états connus. Nous l'avons maintenant démontré en abondance, et en même temps a révélé de nouvelles informations essentielles sur le fonctionnement de la pompe, " il dit.
En plus d'ajouter à notre connaissance des processus de base de la vie, la compréhension de ces pompes peut également avoir des applications pratiques. Des mutations dans les pompes peuvent provoquer des défauts dans les cellules du cerveau, et cela peut provoquer des troubles neurologiques tels que la migraine, paralysie temporaire ou troubles neurodégénératifs.
Les mécanismes de ces pompes ioniques sont donc essentiels pour comprendre les erreurs de la pompe, notamment en vue de développer de nouveaux médicaments ciblant la pompe.
"Nous n'avons pas encore atteint le stade où nous pouvons transférer nos recherches sur les pompes à ions dans le traitement de la maladie. Cependant, les nouvelles connaissances ont conduit à des idées qui peuvent être utilisées pour développer le traitement des défauts de la signalisation neuronale, par exemple. Mais c'est un travail pour l'avenir. À l'heure actuelle, il y a tout lieu de célébrer la révélation des détails intimes de l'une des enzymes les plus importantes de la vie. Le travail s'est appuyé sur de grandes collaborations ici à l'université, et avec des chercheurs aux États-Unis. Nous avons déjà commencé de nouvelles collaborations passionnantes qui nous permettront de franchir les prochaines étapes, ", explique le professeur Poul Nissen.