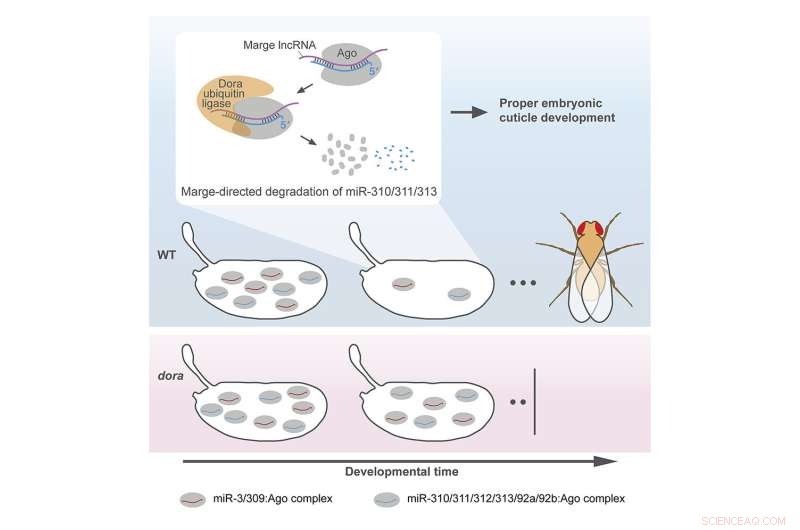
Résumé graphique. Crédit :Cellule moléculaire (2022). DOI :10.1016/j.molcel.2022.08.029
Dans une étude du laboratoire de David Bartel, membre du Whitehead Institute, des chercheurs ont identifié des séquences génétiques pouvant entraîner la dégradation de régulateurs cellulaires appelés microARN chez la mouche des fruits Drosophila melanogaster. Les résultats ont été publiés le 22 septembre dans Molecular Cell .
"Il s'agit d'une étude passionnante qui ouvre la voie à une compréhension plus approfondie de la voie de dégradation des microARN", déclare Bartel, qui est également professeur de biologie au Massachusetts Institute of Technology et chercheur au Howard Hughes Medical Institute. "La découverte de ces séquences "déclencheuses" nous permettra de sonder plus précisément le fonctionnement de cette voie en laboratoire, ce qui est probablement essentiel pour que les mouches - et peut-être d'autres espèces - survivent jusqu'à l'âge adulte."
Afin de produire de nouvelles protéines, les cellules transcrivent leur ADN en ARN messagers (ou ARNm), qui fournissent les informations nécessaires à la fabrication des protéines . Lorsqu'un ARNm donné a atteint son objectif, il est dégradé. Le processus de dégradation est souvent dirigé par de minuscules séquences d'ARN appelées microARN.
Dans des travaux antérieurs, les chercheurs ont montré que certains transcrits d'ARNm ou d'ARN non codant, plutôt que d'être dégradés par des microARN, peuvent à la place renverser la situation sur les microARN et conduire à leur destruction par une voie appelée dégradation des microARN dirigée par la cible, ou TDMD. "Cette voie conduit à un renouvellement rapide de certains microARN dans la cellule", explique Elena Kingston, ancienne étudiante diplômée du Bartel Lab.
Kingston voulait mieux comprendre les fonctions de la voie TDMD dans les cellules. "Je voulais comprendre le" pourquoi "", a-t-elle déclaré. "Pourquoi les microARN sont-ils régulés de cette manière, et pourquoi est-ce important dans un organisme ?"
Les travaux antérieurs sur la voie TDMD ont été principalement menés dans des cellules en culture. Pour la nouvelle étude, les chercheurs ont décidé d'utiliser la mouche des fruits Drosophila melanogaster. Un modèle de mouche pourrait fournir plus d'informations sur le fonctionnement de la voie dans un organisme vivant, y compris si elle a ou non un effet sur la forme physique de l'organisme ou si elle est essentielle à la survie.
Les chercheurs ont créé un modèle pour étudier le TDMD en utilisant des mouches présentant des mutations dans un gène essentiel de la voie TDMD appelé Dora (le gène humain équivalent est appelé ZSWIM8, comme détaillé dans cet article). Très peu de mouches porteuses de mutations chez Dora ont atteint l'âge adulte. La plupart sont morts au début du développement, ce qui suggère que la voie TDMD était probablement importante pour leur viabilité embryonnaire.
Mettre le doigt sur les déclencheurs de la voie TDMD
Alors que les microARN n'ont pas besoin de nombreuses paires de bases complémentaires pour se lier et réguler leurs cibles d'ARNm, l'inverse est vrai dans la voie TDMD. Pour fonctionner correctement, la voie TDMD a besoin d'un déclencheur hautement spécifique, qui peut être soit un ARNm codant pour des protéines, soit un ARN non codant. "Ce qui est unique à propos d'un déclencheur, c'est qu'il possède un site auquel le microARN peut se lier et qui présente une grande complémentarité avec le microARN", a déclaré Kingston.
Lors de l'isolement de la première pandémie de COVID-19, Kingston a entrepris d'écrire un programme qui pourrait sélectionner les déclencheurs probables de la dégradation des microARN chez la drosophile en fonction de leurs séquences. Le programme a renvoyé des milliers de visites et les chercheurs se sont mis au travail pour déterminer quels sites étaient les meilleurs candidats à tester chez les mouches.
"Dès que nous avons pu retourner au laboratoire [après le verrouillage], j'ai pris nos 10 meilleurs candidats environ et j'ai essayé de les perturber avec des mouches", a-t-elle déclaré. "Heureusement pour moi, environ la moitié d'entre eux ont fini par s'entraîner."
Ces six nouveaux déclencheurs font plus que doubler la liste des séquences d'ARN connues pouvant diriger la dégradation des microARN. Pour aller plus loin dans cette découverte, les chercheurs ont mené une analyse de ce qui arrivait aux mouches lorsqu'un déclencheur était perturbé.
Les chercheurs ont découvert que l'un des déclencheurs - un long ARN non codant - joue un rôle dans le bon développement de la cuticule ou de la coque externe imperméable d'un embryon de mouche. "Nous avons remarqué que lorsque nous avons perturbé ce déclencheur, les cuticules des embryons de mouches avaient une élasticité altérée", a déclaré Kingston. "Lorsque nous avons sorti les embryons de leurs coquilles d'œufs, nous avons pu voir ces cuticules se dilater et gonfler."
En raison du phénotype gonflé, Kingston a décidé de nommer la longue marge d'ARN non codant d'après tante Marge, un personnage de la série Harry Potter. Dans "Harry Potter et le prisonnier d'Azkaban", les railleries de tante Marge conduisent Harry à lui faire accidentellement de la magie, la faisant gonfler et flotter.
À l'avenir, Kingston, qui a depuis obtenu son diplôme et commencé une carrière dans l'industrie biotechnologique, espère que les chercheurs reprendront le flambeau pour apprendre les rôles des autres déclencheurs TDMD. "Nous avons encore plusieurs autres déclencheurs [de cet article] où il n'y a pas de rôle biologique connu pour eux dans la mouche", a-t-elle déclaré. "Je pense que cela ouvre le champ pour que d'autres interviennent et posent les questions, 'Où agissent ces déclencheurs ? Que font-ils ? Et quel est le phénotype quand vous les perdez ?'" + Explorer plus loin