Les mutants sont cool, droit? X Men, Les Teenage Mutant Ninja Turtles et les super-héros à travers les bandes dessinées et les films nous impressionnent avec les pouvoirs spéciaux qui ont été dérivés de leurs mutations génétiques. Cependant, ces mutations génétiques fictives sont assez difficiles à trouver – vous devez avoir été mordu par une araignée spéciale ou exposé à une substance radioactive.
Mais et si faire des modifications génétiques n'était pas seulement facile, mais rapide et pas cher, trop? Deviendrez-vous volontairement un mutant ? Bien, avec une technologie appelée CRISPR, vous pourrez peut-être. Ne vous méprenez pas, CRISPR ne va pas vous transformer en super-héros, mais cette découverte scientifique a le potentiel de nous avoir un impact considérable.
Court pour répétitions palindromes courtes et régulièrement espacées , CRISPR nous permet de déplacer des gènes de n'importe quel être vivant vers un autre, altérer l'ADN pour les générations à venir. Cela nous permet de couper les gènes qui font des choses terribles - comme ceux qui causent des maladies - et de les remplacer par des segments d'ADN inoffensifs.
À la fois, La technologie CRISPR est si puissante que les humains pourraient commencer à l'utiliser pour plus que simplement guérir les gens de la maladie. Peut-être pour créer des cultures et du bétail plus résistants aux maladies. Ou pour fabriquer des levures mutantes qui produisent des carburants que nous pouvons utiliser pour alimenter nos voitures. Nous pourrions commencer à être vraiment créatifs et à faire des bébés de créateurs, ou même utiliser la technologie pour le mal – concevoir des armes biologiques spécifiques à une espèce et effacer des espèces entières de la surface de la planète.
Alors que nous en apprenons davantage sur ce que le MIT Technology Review a appelé « la plus grande découverte biotechnologique du siècle, " nous devons également réfléchir au moment où nous devrions utiliser CRISPR et à la manière dont il devrait être régulé.
Contenu
Bien que la technologie CRISPR soit assez impressionnante, les humains modifiant génétiquement différents organismes n'ont rien de nouveau. Côté low-tech, nous sélectionnons des cultures de manière sélective depuis longtemps. Lorsque les agriculteurs sont tombés sur une orange juteuse ou une tomate aux couleurs vives, ils ont préservé ces gènes désirables en plantant des graines de cette plante.
Mais ces dernières années, nous avons fait monter la biotechnologie d'un cran. Au début des années 2000, les scientifiques ont découvert comment utiliser les enzymes, appelées nucléases à doigt de zinc, supprimer et remplacer des gènes indésirables spécifiques dans une variété d'organismes. Les enzymes à doigts de zinc, cependant, étaient chers (plus de 5 $, 000 par pop), difficile à faire, et le taux de réussite n'était pas optimal [source :Ledford].
Alors que la technologie pour modifier les gènes était là, ce n'est que lorsque CRISPR est arrivé que l'idée de changer délibérément l'ADN d'un organisme s'est sentie à portée de main. La première référence à CRISPR était dans un article de journal de 1987 où les scientifiques ont rapporté avoir trouvé les courtes répétitions d'ADN qui sont à la base de la technologie dans E. coli bactéries. Mais ce n'est qu'en 2012 que CRISPR est devenu pertinent. Depuis, l'utilisation de CRISPR a explosé dans la communauté scientifique. Plus d'un milliard de dollars ont été levés en capital de démarrage pour les entreprises de biotechnologie qui utilisent la technique [source :Ledford]. Le financement du gouvernement pour la recherche CRISPR est également à travers le toit.
Rien qu'en 2014, près de 90 millions de dollars ont été engagés par les National Institutes of Health pour la recherche CRISPR [source :Ledford]. Et depuis 2010, plus de 200 brevets liés au CRISPR ont été déposés [source :Ledford]. Le rythme rapide de la recherche ne semble pas ralentir. Alors que les scientifiques en apprennent davantage sur CRISPR, il semble qu'ils en apprennent moins sur les limites de la technique et sur sa puissance. T
Alors, qu'est-ce qui la rend si puissante dans cette technique ?
En 1987, scientifiques étudiant E. coli découvert des segments répétés dans l'ADN de la bactérie. Ce type de modèle dans l'ADN bactérien est inhabituel, alors ils se sont ragaillardis quand ils l'ont remarqué, et a rapporté la découverte. Heures supplémentaires, les scientifiques ont commencé à voir ce schéma dans de nombreux types de bactéries, mais il n'y avait toujours aucune hypothèse sur ce que c'était et pourquoi c'était là. Mais en 2005, une recherche dans une base de données d'ADN a montré que les "répétitions palindromiques courtes et régulièrement espacées en cluster" (ou CRISPR) correspondaient à l'ADN du virus.
Mais pourquoi les bactéries auraient-elles hébergé l'ADN du virus ? Le scientifique Eugene Koonin a émis l'hypothèse que lorsque les bactéries survivent à une attaque virale, ils découpent le virus en petits morceaux et stockent une partie de l'ADN du virus dans leur propre génome afin qu'ils puissent plus tard reconnaître et attaquer le virus s'ils le rencontrent à nouveau. Ils stockent essentiellement une image du virus dans leur poche arrière afin qu'ils puissent reconnaître le méchant s'il devait jamais réapparaître – un mécanisme de défense remarquable du système immunitaire bactérien.
L'hypothèse de Koonin était juste. Si ce virus frappe à nouveau, les bactéries fabriquent des « assassins » spéciaux. Ces assassins peuvent lire la séquence d'ARN de n'importe quel ADN de virus qu'ils rencontrent, reconnaître si cela correspond aux informations qu'ils ont stockées dans leur ADN, le piéger et le hacher. C'est comme si la bactérie avait créé très spécifique, ciseaux intelligents.
Cette découverte était plutôt cool, mais pas aussi cool que ce que l'Université de Californie, La scientifique de Berkeley Jennifer Doudna (qui a depuis remporté le prix Nobel de chimie 2020 avec Emmanuelle Charpentier pour leurs travaux sur CRISPR) a pensé à faire avec l'information. Elle a suggéré que les scientifiques pourraient utiliser CRISPR comme un outil pour les aider à modifier les gènes. S'ils équipaient les bactéries d'un segment d'ADN connu pour être mauvais - disons un gène qui cause la cécité - ils pourraient envoyer les bactéries chercher le mauvais gène, où les bactéries le trouveraient et l'assassineraient. Et puis nous pourrions profiter du mécanisme de réparation naturel des cellules bactériennes pour lancer à sa place un gène plus désirable [source :RadioLab].
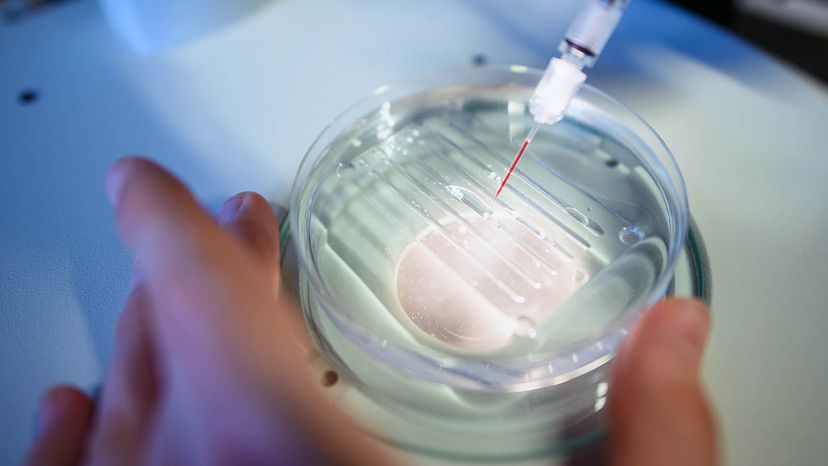
Ça a marché! Et ça a continué à fonctionner ! L'inversion des mutations de la cécité vient d'être l'un des modes de fonctionnement de CRISPR. Il a empêché les cellules cancéreuses de se multiplier, rendu les cellules imperméables au VIH, nous a aidés à créer du blé et du riz résistants aux maladies, et d'innombrables autres avancées. En 2015, Des scientifiques chinois ont même tenté d'utiliser la technologie sur des embryons humains non viables, mais dans quelques cas seulement, CRISPR a fait les bonnes coupes dans l'ADN [source :Maxmen].
Mais cela soulève la question :voulons-nous même l'utiliser sur des embryons ? Doit-on y être autorisé ? Qui réglementera l'utilisation de CRISPR ?
La technologie CRISPR est si relativement nouvelle que la communauté scientifique n'a pas encore pleinement compris toute sa puissance. Mais une chose est sûre :ils savent que sa capacité à avoir un impact sur la race humaine peut être inégalée par aucune autre biotechnologie. Avec ce grand potentiel, la nécessité d'élaborer des réglementations concernant son utilisation est impérative. Mais le rythme effréné auquel la recherche est menée en laboratoire a laissé peu de temps pour discuter de ce que devraient être les règles entourant la recherche et l'utilisation. Cela sonne bien que CRISPR puisse éliminer les mauvais, gènes indésirables et les remplacer par des gènes plus désirables. Mais qui peut dire ce qui est mal et ce qui est bien ?
Sans aucune réglementation, CRISPR pourrait être développé au point où il peut être utilisé en toute sécurité sur un embryon humain pour modifier son ADN. Un parent dirait-il non à CRISPR s'il apprenait que son enfant a le gène de la maladie de Huntington et que CRISPR pourrait l'enlever avant la naissance du bébé ? Et si nous permettions aux parents de prendre la décision de modifier l'ADN de leur bébé avant sa naissance, où cela s'arrêterait-il ? Pourraient-ils décider de rendre leur bébé grand au lieu de petit ? Blonde au lieu de brune ? Les changements que les parents pourraient choisir de transmettre à leur enfant seraient des changements permanents qui seraient transmis de génération en génération. Si ce scénario se produit, il est facile de voir comment cela pourrait creuser davantage le fossé entre les nantis et les démunis. Et nous ne savons pas ce qui pourrait arriver à long terme à un enfant dont les gènes sont remplacés.
En décembre 2015, un groupe de scientifiques, des bioéthiciens et des experts politiques de différents pays se sont rencontrés pour discuter de la réglementation de l'édition des gènes humains. Un expert américain a mentionné que la Food and Drug Administration devait non seulement réglementer la technologie, mais également des utilisations spécifiques de celle-ci pour empêcher l'utilisation hors indication. Elle a également mentionné qu'il pourrait y avoir plus de risques liés à l'édition de gènes végétaux qu'à l'édition de gènes humains [source :Regulatory Affairs Professionals Society].
Avec la grande puissance de cette technologie, les questions sur CRISPR doivent être traitées séparément de celles sur les organismes génétiquement modifiés. Mettre tout le monde à travers le monde sur la même page, cependant, continuera d'être un défi.
Publié à l'origine :3 mai 2016
Écrire des articles comme celui-ci me fait peur. Cette technologie est ainsi, tellement excitant. Les implications semblent généralement très cool, mais on a aussi l'impression que nous avons commencé à comprendre tellement de choses sur la façon de manipuler la vie avec la technologie que nous sommes obligés de tout gâcher à un moment donné. CRISPR nous donne tellement de pouvoir - et d'une manière que nous ne pouvons pas anticiper. Le monde fonctionne bien, vous savez? Jouer avec ça fait juste peur. Puis encore, comment pourrions-nous ignorer une technique aussi puissante qui pourrait nous aider de tant de manières ?