En utilisant des nanoparticules administrées directement dans le liquide céphalo-rachidien (LCR), une équipe de recherche a développé un traitement qui pourrait surmonter d'importants défis dans le traitement d'un cancer du cerveau particulièrement mortel.
Les chercheurs, dirigés par les professeurs Mark Saltzman et Ranjit Bindra, ont administré à des souris atteintes de médulloblastome un traitement contenant des nanoparticules spécialement conçues pour transporter des médicaments. L'étude, publiée dans Science Translational Medicine , ont montré que les souris ayant reçu ce traitement vivaient significativement plus longtemps que les souris du groupe témoin.
Le médulloblastome, un cancer du cerveau qui touche principalement les enfants, débute souvent par une tumeur située profondément à l'intérieur du cerveau. Le cancer a tendance à se propager le long de deux membranes protectrices appelées leptoméninges dans tout le système nerveux central, en particulier à la surface du cerveau et du LCR.
La propagation leptoméningée est observée dans un certain nombre de tumeurs cérébrales primitives, ainsi que dans les métastases cérébrales provenant de tumeurs solides du sein, du poumon et d'autres endroits. Puisqu'il n'existe aucune barrière anatomique dans le LCR pour empêcher une croissance ultérieure, ces cancers peuvent se propager rapidement.
Cibler les tumeurs dans le LCR s'est avéré difficile, en partie parce que le liquide circule rapidement dans le système nerveux central environ quatre fois par jour chez l'homme, éliminant généralement les médicaments antitumoraux avant qu'ils n'aient eu la chance de s'accumuler et d'avoir un effet.
"C'est comme un système de cascade, avec un écoulement de fluide rapide et rapide", a déclaré Minsoo Khang, auteur principal de l'étude et ancien étudiant diplômé du laboratoire de Saltzman.
Pour contourner cet obstacle, l’équipe de recherche a fabriqué des nanoparticules qui adhèrent aux tumeurs. Conçues dans le laboratoire de Saltzman, ces nanoparticules sont fabriquées à partir de polymères dégradables qui libèrent lentement un inhibiteur de la réparation de l'ADN, le talazoparib, approuvé par la FDA et actuellement utilisé en clinique pour un certain nombre de cancers. Le médicament fait partie d’une classe relativement nouvelle de médicaments anticancéreux connus sous le nom d’inhibiteurs de PARP, qui bloquent une enzyme qui aide à réparer l’ADN. Sans la capacité de réparer leur ADN, les cellules tumorales risquent davantage de mourir.
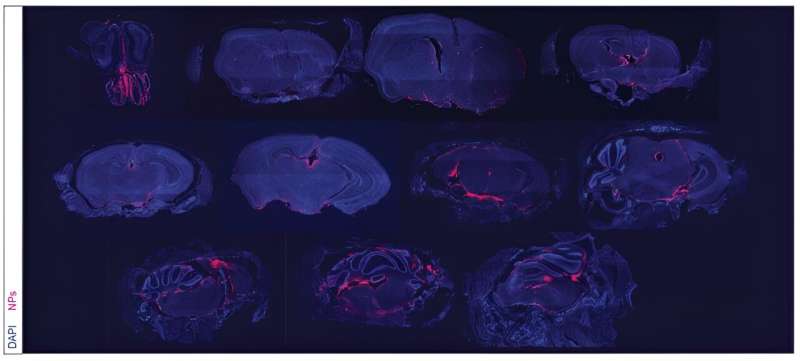
Le traitement aux nanoparticules est injecté par voie intrathécale, c'est-à-dire qu'il est administré directement entre les leptoméninges protégeant le LCR. Sur une période de plusieurs semaines, les chercheurs ont détecté la présence de nanoparticules dans le LCR jusqu'à 21 jours après une seule dose.
"Nous étions très heureux d'avoir trouvé un support capable de retenir à long terme dans cet espace fluide, ce qui autrement représente un défi", a déclaré Khang.
Le traitement des cancers du cerveau en général est un défi puisque peu de traitements peuvent pénétrer la barrière hémato-encéphalique, un système de défense naturel qui peut bloquer des médicaments potentiellement utiles. La méthode de l'équipe de recherche pourrait offrir une solution.
"Il y a eu très peu de travaux sur l'administration intrathécale de nanoparticules, nous sommes donc très enthousiastes car cela peut nous permettre de lutter contre la propagation leptoméningée de la maladie à partir de métastases cérébrales", a déclaré Bindra, professeur Harvey et Kate Cushing de radiologie thérapeutique et professeur de Pathologie. "Cela a vraiment ouvert une toute nouvelle façon de traiter ces patients, même s'il reste encore beaucoup à faire."
L’utilisation des nanoparticules pour cibler les tumeurs a permis aux chercheurs d’utiliser le médicament talazoparib, qui s’est révélé efficace dans un certain nombre de tumeurs solides en dehors du cerveau. Étant donné que le médicament a une pénétration limitée, voire nulle, dans le système nerveux central, une dose administrée par voie orale aurait une efficacité limitée contre les tumeurs à propagation leptoméningée.
"En l'encapsulant dans une nanoparticule et en l'injectant directement dans le LCR, nous obtenons désormais une exposition très élevée dans ce domaine précis", a déclaré Saltzman, professeur de génie biomédical, de génie chimique et environnemental et de physiologie à la Fondation Goizueta, et membre de Yale. Centre de lutte contre le cancer.
L'administration intrathécale du médicament évite également de l'injecter directement dans le cerveau, une technique appelée administration améliorée par convection, une procédure très difficile qui ne peut être effectuée que quelques fois par an. Les injections intrathécales, en revanche, sont beaucoup moins invasives et peuvent être administrées sans hospitalisation.
"C'est énorme pour nous, car nous pouvons désormais effectuer plusieurs traitements de nanoparticules au fil du temps", a déclaré Bindra.
En plus de l'injection de nanoparticules, les souris ont également reçu une dose orale d'un médicament de chimiothérapie appelé témozolomide.
"C'est une nouvelle plate-forme où nous pouvons administrer des chimiothérapies orales qui traversent la barrière hémato-encéphalique et un agent ciblé uniquement dans le système nerveux central", a déclaré Bindra. "Essentiellement, ce compartimentage de la thérapie combinée améliorera la destruction synergique des cellules tumorales tout en minimisant la toxicité systémique."
Les souris ayant reçu le traitement à base de nanoparticules ont vécu beaucoup plus longtemps que les souris ayant reçu un traitement médicamenteux n'utilisant pas de nanoparticules, et même plus longtemps que les souris n'ayant reçu aucun traitement. De plus, la propagation du cancer a été bien moindre chez les souris ayant reçu les nanoparticules porteuses du médicament.
Les chercheurs ont déclaré que les prochaines étapes consisteront à valider l’approche sur des modèles animaux plus grands, éventuellement suivis par des tests sur l’homme. L'équipe prévoit également de tester la méthode de traitement sur d'autres cancers, notamment ceux qui ont tendance à se propager au cerveau.
Plus d'informations : Minsoo Khang et al, Administration intrathécale d'un inhibiteur de nanoparticules PARP dans le liquide céphalo-rachidien pour le traitement du médulloblastome métastatique, Science Translational Medicine (2023). DOI :10.1126/scitranslmed.adi1617
Informations sur le journal : Science Médecine translationnelle
Fourni par l'Université de Yale