Une équipe de chimistes et de bio-ingénieurs de l'Université Rice et de l'Université de Houston ont franchi une étape importante dans leurs travaux visant à créer un biomatériau pouvant être utilisé pour cultiver des tissus biologiques en dehors du corps humain.
Le développement d'un nouveau processus de fabrication pour créer des hydrogels de nanofibres alignés pourrait offrir de nouvelles possibilités de régénération des tissus après une blessure et fournir un moyen de tester des médicaments thérapeutiques candidats sans utiliser d'animaux.
L'équipe de recherche, dirigée par Jeffrey Hartgerink, professeur de chimie et de bio-ingénierie, a développé des hydrogels à base de peptides qui imitent la structure alignée des tissus musculaires et nerveux. L'alignement est essentiel à la fonctionnalité des tissus, mais il s'agit d'une caractéristique difficile à reproduire en laboratoire, car elle implique l'alignement de cellules individuelles.
Depuis plus de dix ans, l’équipe conçoit des peptides multidomaines (MDP) qui s’auto-assemblent en nanofibres. Celles-ci ressemblent aux protéines fibreuses présentes naturellement dans le corps, un peu comme une toile d'araignée à l'échelle nanométrique.
Dans leur dernière étude, publiée dans la revue ACS Nano , les chercheurs ont découvert une nouvelle méthode pour créer des « nouilles » alignées en nanofibres MDP.
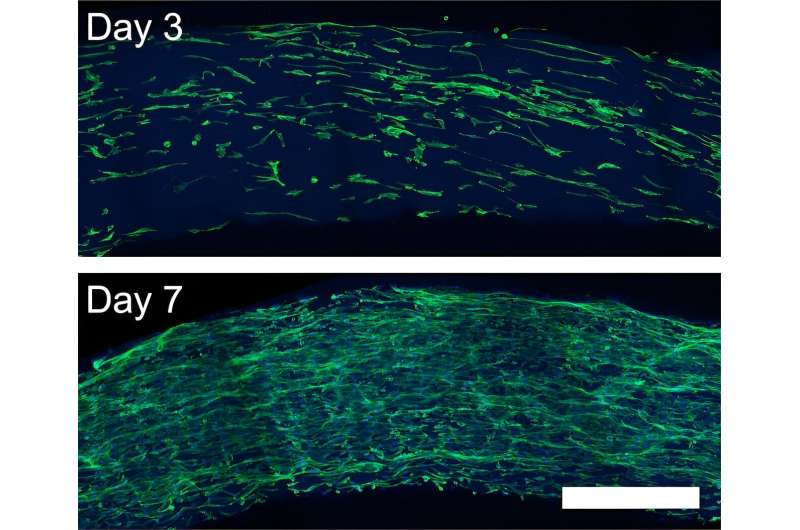
En dissolvant d’abord les peptides dans l’eau, puis en les extrudant dans une solution salée, ils ont pu créer des nanofibres peptidiques alignées, comme des brins de corde torsadés plus petits qu’une cellule. En augmentant la concentration d'ions, ou de sel, dans la solution et en répétant le processus, ils ont obtenu un alignement encore plus grand des nanofibres.
"Nos résultats démontrent que notre méthode peut produire des nanofibres peptidiques alignées qui guident efficacement la croissance cellulaire dans la direction souhaitée", a expliqué l'auteur principal Adam Farsheed, qui a récemment obtenu son doctorat. en bio-ingénierie de Rice.
"Il s'agit d'une étape cruciale vers la création de tissus biologiques fonctionnels pour des applications en médecine régénérative."
L’une des principales conclusions de l’étude a été une découverte inattendue :lorsque l’alignement des nanofibres peptidiques était trop fort, les cellules ne s’alignaient plus. Une enquête plus approfondie a révélé que les cellules devaient être capables de « tirer » sur les nanofibres peptidiques pour reconnaître l’alignement. Lorsque les nanofibres étaient trop rigides, les cellules étaient incapables d'exercer cette force et ne parvenaient pas à s'organiser dans la configuration souhaitée.
"Cette connaissance du comportement cellulaire pourrait avoir des implications plus larges pour l'ingénierie tissulaire et la conception de biomatériaux", a déclaré Hartgerink.
"Comprendre comment les cellules interagissent avec ces matériaux à l'échelle nanométrique pourrait conduire à des stratégies plus efficaces pour construire des tissus."
Les co-auteurs supplémentaires de l’étude de Rice incluent le doctorat du département de chimie. les diplômés Tracy Yu et Carson Cole, l'étudiant diplômé Joseph Swain et le chercheur de premier cycle Adam Thomas. Jonathan Makhoul, chercheur de premier cycle en bioingénierie, Eric Garcia Huitron, étudiant diplômé, et le professeur K. Jane Grande-Allen étaient également co-auteurs de l'étude. L'équipe de chercheurs de l'Université de Houston comprend un doctorat. l'étudiant Christian Zevallos-Delgado, l'assistant de recherche Sajede Saeidifard, le professeur assistant de recherche Manmohan Singh et le professeur d'ingénierie Kirill Larin.
Plus d'informations : Adam C. Farsheed et al, Alignement macroscopique accordable de nanofibres peptidiques auto-assemblantes, ACS Nano (2024). DOI :10.1021/acsnano.4c02030
Informations sur le journal : ACS Nano
Fourni par l'Université Rice