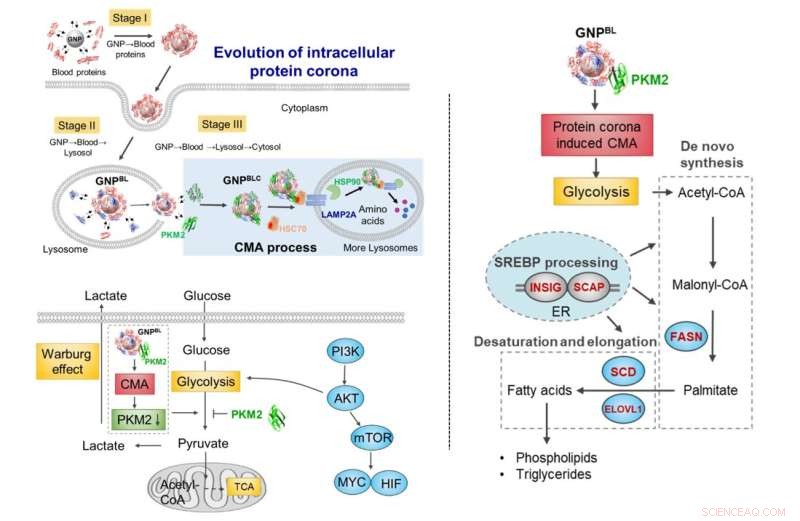
Évolution de la couronne nano-protéique au cours du transport cellulaire. Au cours du transport depuis le cytoplasme sanguin-lysosomal, l'échange de composants de la couronne protéique avec des protéines intracellulaires (protéines chaperons, kinases métaboliques) déclenche une augmentation de l'activité d'autophagie médiée par les protéines chaperons et remodèle sélectivement le métabolisme cellulaire. Crédit :Chen Chunying et al.
Une équipe de recherche dirigée par le professeur Chen Chunying du National Center for Nanoscience and Technology (NCNST) de l'Académie chinoise des sciences (CAS) a récemment étudié l'évolution de la couronne de nano-protéines au cours de l'endocytose et sa perturbation de l'homéostasie des protéines et des cellules. métabolisme. Leurs résultats ont été publiés dans PNAS .
Lorsque les nanoparticules pénètrent dans les systèmes biologiques, les biomolécules de fluide biologique se lient rapidement à la surface des nanoparticules. La couronne de nano-protéines formée en interagissant avec des molécules de protéines dans le sang comme étape de départ a un impact énorme sur le transport et le devenir des nanoparticules. La façon dont la formation de la couronne de nanoprotéines affecte la reconnaissance, le transport, la distribution, la fonction et les effets biologiques des nanoparticules dans les tissus et les cellules de différents systèmes de barrière est une "boîte noire" pour l'application médicale des nanomatériaux, qui non seulement limite la livraison l'efficacité de la nanomédecine, mais affecte également sérieusement l'efficacité et la sécurité.
Un défi important dans ce domaine est la complexité de la couronne nano-protéique, qui est influencée par la diversité des biomolécules dans différents tissus et organes, ainsi que par les états physiologiques et pathologiques. À l'heure actuelle, il est urgent de comprendre comment la composition protéique et les caractéristiques structurelles de la couronne protéique évoluent dans les microenvironnements biologiques.
Pour résoudre ce problème, les chercheurs ont révélé le schéma d'évolution dynamique de la composition protéique de la couronne nano-protéique dans le processus de transport cellulaire grâce à l'application innovante de la multi-omique multidimensionnelle (protéomique, métabolomique, lipidomique), des interactions intermoléculaires , et imagerie par spectrométrie de masse in situ.
En prenant comme modèle les nanoparticules d'or, le processus d'évolution dynamique de la couronne protéique du système sanguin vers l'intracellulaire (sang-lysosomal-cytoplasme) a été étudié. Lorsque les nanoparticules étaient endocytosées dans le lysosome à partir de l'environnement sanguin, puis s'échappaient du lysosome dans le cytoplasme, la composition protéique à la surface des nanoparticules changeait considérablement. La plupart ont été remplacées par des molécules de protéines intracellulaires, ne conservant qu'une partie des composants corona protéiques formés dans l'environnement sanguin.
Par la suite, l'évolution intracellulaire de la couronne de nano-protéines a non seulement perturbé l'homéostasie des protéines intracellulaires (protéostase), mais a également déclenché l'enrichissement des protéines chaperons (HSC70, HSP90) et de la pyruvate kinase M2 (PKM2) à la surface de la nano-couronne intracellulaire, et stimulé l'autophagie médiée par le chaperon. Il a également affecté la glycolyse cellulaire, provoquant des modifications du métabolisme énergétique cellulaire et régulant le processus de métabolisme des lipides cellulaires.
Cette étude élucide le schéma évolutif des nanoparticules du sang vers un microenvironnement subcellulaire et identifie la spécificité du microenvironnement intracellulaire de la couronne de nanoprotéines, remodelant ainsi le métabolisme cellulaire. Il fournit également un support théorique pour une compréhension approfondie des effets biologiques complexes des nanomatériaux et de la régulation de l'interface nanobiotique. Les effets de la protéine corona sur les interactions des liposomes visualisés par AIE avec ce