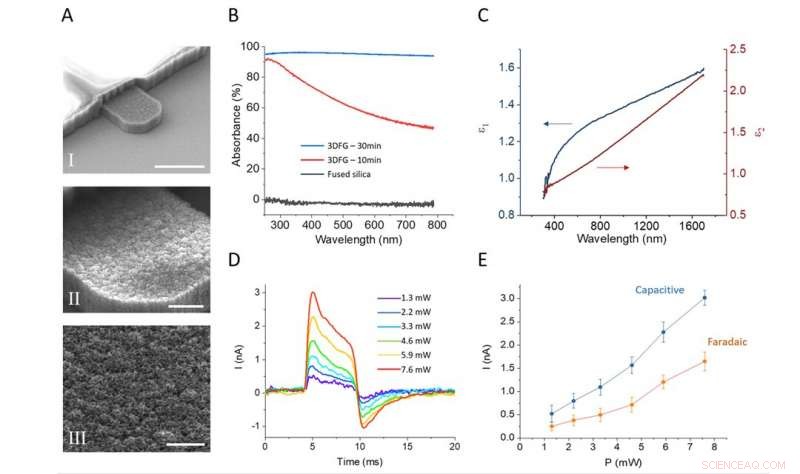
Les images SEM permettent d'observer de plus près les électrodes 3DFG. Crédit :Université Carnegie Mellon, Département de génie biomédical
Derrière chaque battement cardiaque et signal cérébral se cache un orchestre massif d'activité électrique. Alors que les techniques d'observation électrophysiologiques actuelles se limitent pour la plupart à des enregistrements extracellulaires, un groupe de chercheurs avant-gardistes de l'Université Carnegie Mellon et de l'Istituto Italiano di Tecnologia a identifié un à bas prix, et plate-forme biocompatible pour permettre des enregistrements intracellulaires plus riches.
Le partenariat unique du groupe "à travers l'océan" a commencé il y a deux ans à la Bioelectronics Winter School (BioEl) avec des libations et un croquis de serviette de table. Il est devenu une recherche publiée dans Avancées scientifiques , détaillant une nouvelle plate-forme de microélectrodes qui exploite le graphène flou tridimensionnel (3DFG) pour permettre des enregistrements intracellulaires plus riches des potentiels d'action cardiaque avec un rapport signal sur bruit élevé. Cette avancée pourrait révolutionner les recherches en cours liées aux maladies neurodégénératives et cardiaques, ainsi que le développement de nouvelles stratégies thérapeutiques.
Un leader clé dans ce travail, Tzahi Cohen-Karni, professeur agrégé de génie biomédical et de science et ingénierie des matériaux, a étudié les propriétés, effets, et les applications potentielles du graphène tout au long de sa carrière. Maintenant, il fait un pas de collaboration dans une direction différente, en utilisant une orientation verticale de l'extraordinaire matériau à base de carbone (3DFG) pour accéder au compartiment intracellulaire de la cellule et enregistrer l'activité électrique intracellulaire.
En raison de ses propriétés électriques uniques, le graphène se distingue comme un candidat prometteur pour les dispositifs de biodétection à base de carbone. Des études récentes ont montré le déploiement réussi de biocapteurs au graphène pour surveiller l'activité électrique des cardiomyocytes, ou des cellules cardiaques, en dehors des cellules, ou en d'autres termes, enregistrements extracellulaires de potentiels d'action. Enregistrements intracellulaires, d'autre part, sont restés limités en raison d'outils inefficaces… jusqu'à présent.
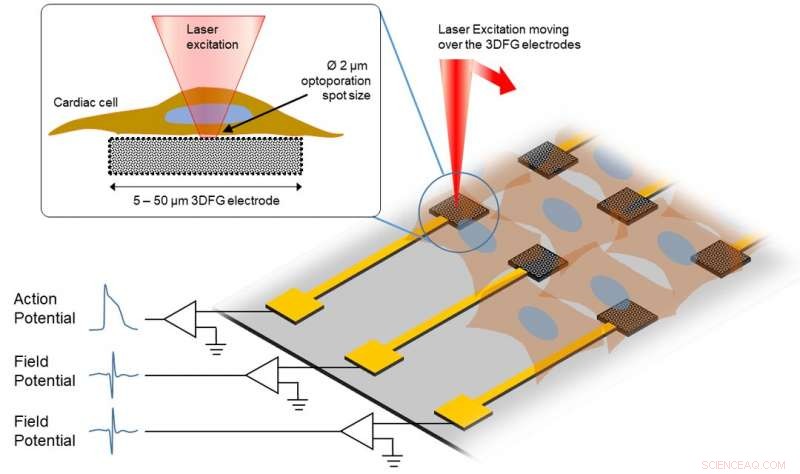
Ce croquis montre la procédure expérimentale du laser ultra-rapide se déplaçant sur les électrodes 3DFG. Crédit :Collège d'ingénierie, L'université de Carnegie Mellon
"Notre objectif est d'enregistrer l'ensemble de l'orchestre - de voir tous les courants ioniques qui traversent la membrane cellulaire - pas seulement le sous-ensemble de l'orchestre montré par les enregistrements extracellulaires, " explique Cohen-Karni. " L'ajout de la dimension dynamique des enregistrements intracellulaires est fondamentalement important pour le criblage des médicaments et les tests de toxicité, mais ce n'est qu'un aspect important de notre travail."
"Le reste est l'avancement de la technologie, " Cohen-Karni poursuit. " 3DFG est bon marché, plate-forme flexible et tout carbone ; aucun métal impliqué. Nous pouvons générer des électrodes de la taille d'une plaquette de ce matériau pour permettre des enregistrements intracellulaires multi-sites en quelques secondes, ce qui est une amélioration significative par rapport à un outil existant, comme un patch-clamp, ce qui demande des heures de temps et d'expertise."
Donc, Comment ça marche? En s'appuyant sur une technique développée par Michele Dipalo et Francesco De Angelis, chercheurs de l'Istituto Italiano di Tecnologia, un laser ultra-rapide est utilisé pour accéder à la membrane cellulaire. En projetant de courtes impulsions laser sur l'électrode 3DFG, une zone de la membrane cellulaire devient en quelque sorte poreuse, permettant d'enregistrer l'activité électrique dans la cellule. Puis, les cardiomyocytes sont cultivés pour étudier plus avant les interactions entre les cellules.
De façon intéressante, 3DFG est noir et absorbe la majeure partie de la lumière, résultant en des propriétés optiques uniques. Combiné avec sa structure en mousse et son énorme surface exposée, 3DFG possède de nombreuses caractéristiques souhaitables qui sont nécessaires pour fabriquer de petits biocapteurs.
« Nous avons développé une électrode plus intelligente ; une électrode qui nous permet un meilleur accès, " souligne Cohen-Karni. " Le plus gros avantage de mon côté est que nous pouvons avoir accès à cette richesse de signal, pour être en mesure d'examiner les processus d'importance intracellulaire. Disposer d'un outil comme celui-ci va révolutionner la façon dont nous pouvons étudier les effets de la thérapeutique sur les organes terminaux, comme le cœur."
Au fur et à mesure que ce travail avance, l'équipe prévoit d'appliquer ses apprentissages dans des interfaces cellules/tissus à grande échelle, pour mieux comprendre le développement des tissus et la toxicité des composés chimiques (p. toxicité médicamenteuse).