
Les microcapsules avec des coques d'épaisseur variable (rouge) peuvent encapsuler de manière stable la cargaison et la libérer à un étalonnage précis, faible pression osmotique, permettant l'administration sûre de médicaments et d'autres substances à l'intérieur du corps humain. Crédit :Institut Wyss de l'Université Harvard
Casser un œuf pour libérer son jaune nécessite d'appliquer une force externe (comme être frappé contre le bord d'un bol) pour vaincre la force de la coquille. De la même manière, la délivrance de biomolécules thérapeutiques contenues dans des microcapsules dans le corps humain nécessite que leurs contenants soient brisés après leur injection, afin que la cargaison puisse être livrée au bon endroit au bon moment. Un certain nombre de stimuli externes peuvent être utilisés pour déclencher la libération de molécules encapsulées, l'une des plus faciles est la pression osmotique, car il nécessite simplement l'introduction d'eau pour faire gonfler et éclater les microcapsules. Cependant, afin de créer une pression interne suffisante pour casser l'enveloppe de la capsule, de grandes quantités d'un agent osmotique doivent être ajoutées à la microcapsule pour attirer l'eau, et la pression d'éclatement élevée qui en résulte pourrait endommager les tissus ou provoquer des caillots sanguins.
Une solution à cette pierre d'achoppement a maintenant été développée par des chercheurs du Wyss Institute for Biologically Inspired Engineering de Harvard et de la John A. Paulson School of Engineering and Applied Sciences (SEAS), qui a conçu un moyen de créer des microcapsules avec des coques d'épaisseur inégale qui leur permet d'éclater à des pressions osmotiques plus basses, les rendant plus sûrs pour une utilisation dans le corps humain. La recherche est publiée dans Petit .
"La partie la plus faible de nos carapaces est 40 fois plus fine que la partie la plus solide, ce qui leur permet de casser et de libérer beaucoup plus facilement leur cargaison, " a déclaré le premier auteur Weixia Zhang, Doctorat., un boursier postdoctoral au Wyss Institute et au SEAS. « D'un autre côté, ces microcapsules sont extrêmement durables et ne fuient pas si elles ne sont pas exposées à une pression osmotique élevée, ce qui les rend très stables et capables de stocker leur contenu pendant longtemps."
Pour fabriquer leurs microcapsules inhomogènes, les chercheurs ont utilisé un dispositif microfluidique capillaire en verre qui employait une méthode eau-dans-huile-dans-eau pour encapsuler une solution aqueuse contenant du saccharose, un agent osmotique, dans une coquille de monomères en suspension dans l'huile. Lorsque les monomères sont exposés à la lumière UV, ils réagissent entre eux et se réticulent pour former un solide, enveloppe polymère autour de la solution de saccharose. En faisant varier les vitesses auxquelles la solution de saccharose « cargo » et l'huile de monomère « coquille » s'écoulent à travers le dispositif, l'équipe a découvert qu'ils pouvaient introduire des variations dans l'épaisseur des coquilles qui se sont formées, créant des capsules déséquilibrées avec des parois plus épaisses d'un côté et plus minces de l'autre.
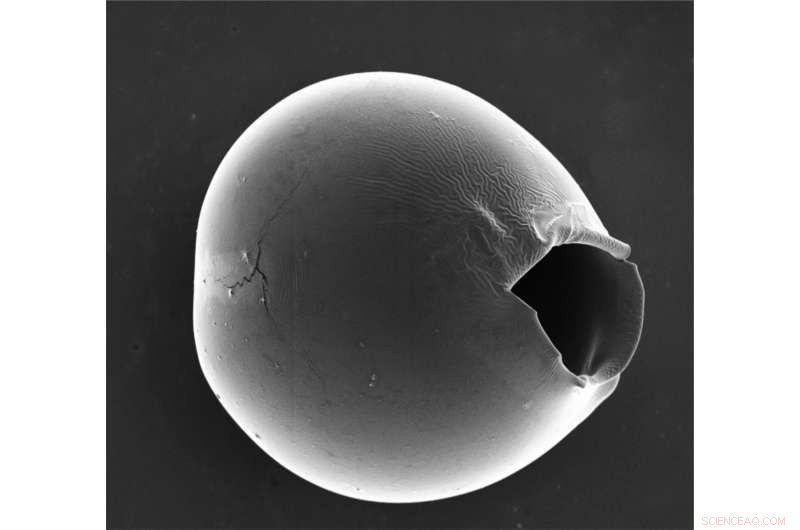
Les microcapsules éclatent au niveau de la partie la plus fine de la coque, laissant une ouverture de quelques dizaines de microns qui permet à la plupart des biomolécules et des médicaments d'être libérés. Crédit :Institut Wyss de l'Université Harvard
Les chercheurs ont ensuite soumis leurs microcapsules à un choc osmotique en ajoutant de l'eau, qui a diffusé dans les microcapsules et les a fait commencer à gonfler à la partie la plus fine de la coquille. Après environ 20-30 minutes, la coquille amincie s'est fissurée, formant une ouverture de plusieurs dizaines de micromètres, qui est assez grand pour que la plupart des biomolécules et des nanomatériaux soient libérés avec succès. L'augmentation de la différence entre la partie la plus fine et la partie la plus épaisse de la coque a conduit à un plus grand nombre de microcapsules éclatées, confirmant que le degré d'inhomogénéité a eu un impact sur l'efficacité de la libération de la cargaison.
"Être capable de créer des microcapsules avec un degré élevé d'inhomogénéité en modifiant l'épaisseur de la coque pendant le processus de fabrication et de libérer la cargaison avec une pression osmotique beaucoup plus faible ouvre une nouvelle application dans la libération contrôlée, ce qui est très important pour l'administration de médicaments en médecine, ainsi que d'autres domaines, " a déclaré le co-premier auteur Liangliang Qu, Doctorat., un boursier postdoctoral au Wyss Institute et au SEAS.
Pour tester la durabilité des microcapsules, l'équipe a encapsulé un polymère fluorescent à l'intérieur et mesuré le changement d'intensité de fluorescence dans leurs noyaux au fil du temps. Ils n'ont observé aucun changement d'intensité pendant 30 jours après l'encapsulation, démontrant que les microcapsules retenaient leur cargaison sans fuite. Par ailleurs, la taille du polymère est beaucoup plus petite que la plupart des biomolécules, tels que les anticorps et les enzymes, suggérant que les coquilles pourraient être utilisées pour protéger et stocker des biomolécules ou des médicaments pendant de longues périodes.
Finalement, les chercheurs ont co-encapsulé une protéase (une enzyme qui décompose les protéines) et du saccharose à l'intérieur de leurs microcapsules pendant 37 jours, puis appliqué un choc osmotique pour déclencher la libération de leur contenu. La protéase a conservé 91% de son activité d'origine, démontrant que cette méthode de stockage n'altère pas significativement sa fonction biologique.
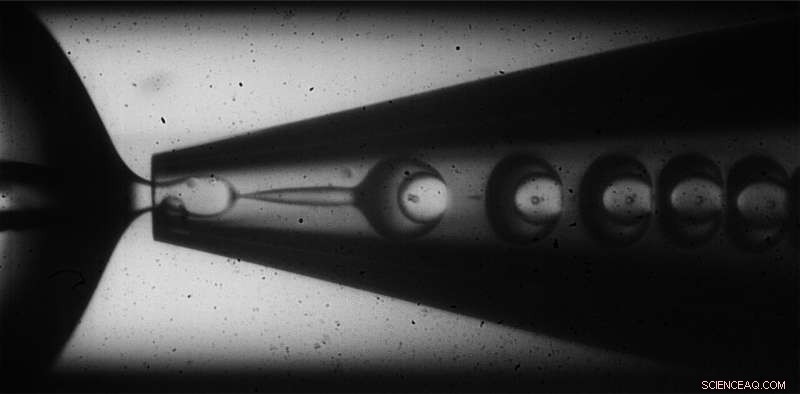
Les microcapsules sont créées à l'aide d'une technique huile dans eau dans huile qui permet d'obtenir une épaisseur de coque non homogène en faisant varier les débits de la coque et des matériaux de la cargaison. Crédit :Institut Wyss de l'Université Harvard
« Par rapport à d'autres transporteurs à libération contrôlée, comme les cellules, nanoparticules, ou des vésicules, ce système est très polyvalent, stable, et personnalisable, ce qui en fait une alternative attrayante pour l'administration sûre et efficace de médicaments et d'autres biomolécules pour la santé humaine et d'autres applications, " a déclaré l'auteur correspondant David Weitz, Doctorat., membre principal du corps professoral du Wyss Institute, qui est également professeur Mallinckrodt de physique et de physique appliquée à SEAS.
L'équipe continue de développer ses microcapsules en optimisant le matériau de l'enveloppe pour diminuer encore la pression osmotique nécessaire à leur rupture. Ils prévoient d'abord d'appliquer leur technologie à l'administration de médicaments, tels que les anticorps thérapeutiques, dans le but de pouvoir utiliser la forte teneur en eau du corps humain pour agir comme déclencheur de rupture après injection.
"Ce projet est un excellent exemple de la façon dont des solutions plus simples peuvent souvent être meilleures que des solutions compliquées, comme la seule entrée nécessaire pour éclater les microcapsules est la pression mécanique, plutôt que des chimies complexes ou des commutateurs moléculaires, " a déclaré le co-auteur Donald Ingber, MARYLAND., Doctorat., qui est le directeur fondateur du Wyss Institute, le professeur Judah Folkman de biologie vasculaire au HMS et le programme de biologie vasculaire du Boston Children's Hospital, et professeur de bio-ingénierie à SEAS.