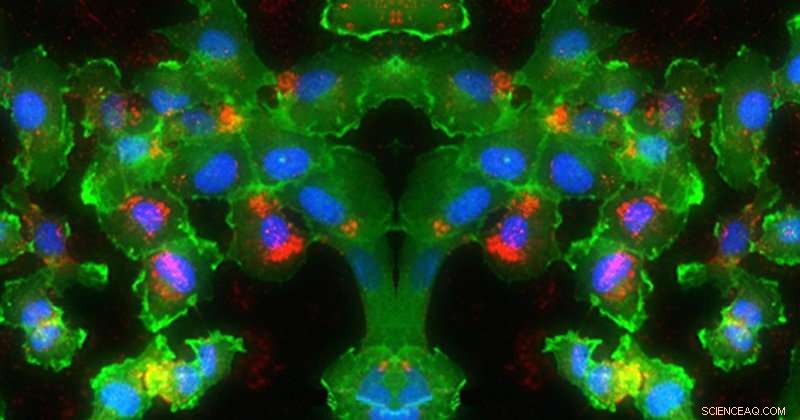
Dans cette image, L'ARN (rouge) est délivré dans les noyaux (bleu) des cellules (vert). Crédit :Université du Delaware, Evan Krapé, Emily Day et Joy Smoker
Les traitements contre le cancer, de la radiothérapie à la chirurgie en passant par la chimiothérapie, sont conçus pour éliminer ou tuer les cellules cancéreuses, mais les cellules saines deviennent souvent des dommages collatéraux dans le processus. Et si vous pouviez utiliser des lasers pour localiser la zone de traitement et administrer des médicaments uniquement aux cellules cancéreuses ?
Une équipe de recherche de l'Université du Delaware, dirigé par Emily Day, professeur assistant en génie biomédical, pose les bases d'une méthode pour inhiber les gènes favorisant le cancer dans les cellules cancéreuses tout en laissant intactes les cellules saines. Dans un nouvel article publié dans Lettres nano , l'équipe révèle des informations sans précédent sur cette méthode prometteuse, qui consiste à revêtir des nanoparticules d'agents de régulation génétique, puis à les exposer à une dose de lumière laser pour libérer ce matériau.
Parce que les nanoparticules maintiennent les agents régulateurs géniques inactifs jusqu'à ce que leur libération soit déclenchée à la demande par la lumière, ils ont un potentiel substantiel pour permettre une thérapie anticancéreuse de haute précision tout en minimisant l'impact sur les cellules saines non irradiées. Day et son équipe ont testé leur nouvelle méthode contre les cellules tumorales cérébrales en utilisant les nanoparticules pour faire taire l'expression de la protéine fluorescente verte (GFP) dans les cellules.
Une nouvelle façon de combiner lasers et nanoparticules
Comme les scalpels et les sutures, les lasers sont souvent utilisés dans les procédures médicales. Les ophtalmologistes utilisent des lasers pour remodeler les cornées lors de la chirurgie oculaire de correction de la vision. Les dermatologues utilisent des lasers pour estomper les cicatrices sur la peau. Les cardiologues utilisent des lasers pour ouvrir les artères obstruées. Les oncologues utilisent des lasers pour détruire les cellules cancéreuses et les tumeurs.
Le Day Lab vise à combiner des lasers avec des nanoparticules régulatrices de gènes sensibles à la lumière pour annihiler stratégiquement les cellules cancéreuses et minimiser les dommages collatéraux.
Ils commencent par de petits ARN interférents, connus sous le nom d'ARNsi, qui sont des molécules constituées de brins complémentaires d'ARN qui peuvent réduire l'expression de certains gènes dans les cellules cancéreuses. Les siRNA sont enrobés de nanoparticules de silice et d'or, qui mesurent plus petit que la largeur d'un cheveu humain. Ces particules protègent les siRNA jusqu'à ce qu'ils atteignent la zone de traitement souhaitée. La question est :comment les relâcher exactement au bon endroit ?
"Précédemment, si les gens voulaient livrer de l'ARN avec des nanoparticules, ils pourraient enrober les nanoparticules d'un polymère ou d'un peptide pénétrant dans les cellules, un agent pour faciliter l'absorption et la livraison des cellules, " Day a dit. "Le problème est que ces agents ne sont pas spécifiques. Vous finissez par obtenir une régulation génique dans toutes les cellules, pas seulement les cellules cancéreuses que vous aviez l'intention de cibler pour la régulation des gènes."
C'est là qu'intervient la précision des lasers.
"La libération d'ARNsi déclenchée par la lumière vous permet de faire taire les gènes uniquement là où les particules et la lumière sont combinées, " Dit Day. " Puisque tu choisis où va la lumière, et donc où le siRNA est libéré, vous pouvez obtenir un silençage génique très spécifique dans les cellules tumorales, réduisant le potentiel d'effets hors cible."
Pour ces expériences, Day et son équipe (dirigée par Rachel Riley, étudiante diplômée du Département de génie biomédical) ont exposé les nanoparticules recouvertes d'ARNsi à une lumière à onde continue ou à de courtes impulsions de lumière administrées tous les quadrillions de seconde. Les deux types d'irradiation ont déclenché la libération de siRNA sous des formes double brin et simple brin, ce qui était une surprise puisque des études précédentes dans la littérature scientifique suggéraient que l'irradiation par ondes continues ne libérerait que des brins simples de siARN (ce qui signifie que les deux brins complémentaires du siARN se sont séparés l'un de l'autre, plutôt que le duplex entier libéré de la surface des nanoparticules).
"C'est la première fois que quelqu'un montre que vous pouvez libérer à la fois des duplex d'ARNsi et des brins simples d'ARN à partir de nanoparticules en utilisant un laser à onde continue comme source d'excitation, " dit Day. " Cependant, nos études révèlent également que la lumière pulsée est beaucoup plus efficace pour libérer des duplex d'ARNsi que la lumière à onde continue. Il est impératif que principalement les duplex soient libérés des nanoparticules car seul l'ARNsi duplex fonctionnera à l'intérieur des cellules pour faire taire l'expression des gènes ciblés. »
La journée a continué, "Plus loin, nos études montrent que la lumière pulsée ne chauffe pas les cellules comme le fait la lumière à ondes continues. Ceci est important car trop de chaleur peut endommager les cellules par des mécanismes autres que la régulation génétique souhaitée. »
Son groupe de laboratoire est bien équipé pour découvrir de telles informations concernant le mécanisme de libération d'ARN déclenché par la lumière à partir de nanoparticules, car ils effectuent des recherches interdisciplinaires uniques.

De gauche, Margaret Billingsley, Emilie jour, et Rachel Riley travaillent sur l'une de leurs précédentes études de recherche, celui-ci sur la détection du cancer. Crédit :Université du Delaware, Evan Krapé, Emily Day et Joy Smoker
"Mon laboratoire a beaucoup d'expertise dans la livraison d'ARN et la biologie du cancer, nous avons donc beaucoup plus de compétences en biologie moléculaire qu'un laboratoire de nanotechnologie traditionnel pourrait en avoir, et cela nous permet d'étudier la fonction des nanoporteurs d'ARN avec des détails sans précédent, " elle a dit.
La nouvelle idée que la recherche de Day apporte sur l'utilisation de la lumière à onde continue par rapport à la lumière pulsée pour la libération déclenchée d'ARNsi à partir de nanoparticules est une contribution importante au domaine de l'administration de médicaments. En plus de démontrer les différences fonctionnelles entre les deux modes d'excitation lumineuse, l'équipe a également montré que l'ARNsi libéré par les nanoparticules lors de l'exposition à la lumière pulsée réduisait l'expression du gène ciblé (protéine fluorescente verte) mieux qu'un matériau disponible dans le commerce souvent utilisé pour administrer l'ARNsi dans les cellules lors d'expériences en laboratoire. Ce fut une observation passionnante démontrant l'impact potentiel de ce nouveau système.
Ce travail a été mené en collaboration avec Lars Gundlach dans le Département de Chimie et Biochimie et le Département de Physique et Astronomie à l'UD, qui possède le laser pulsé utilisé dans ces expériences. Beaucoup plus de recherches sont nécessaires avant que cela puisse être traduit en un traitement viable pour les patients atteints de cancer.
Et après?
"La prochaine étape serait de montrer que nous pouvons le faire avec une cargaison d'ARN plus fonctionnelle et biologiquement pertinente que le siRNA ciblant la protéine fluorescente verte qui a été utilisée dans ce travail, " Day said. "There are a lot of different genes that are known to control cancer growth, so we will deliver RNA that targets genes that we know to be important in tumor progression and see if we are delivering enough to have an impact."
The team is particularly interested in studying the delivery of siRNA targeting beta-catenin, which plays an important role in triple-negative breast cancer, and also the delivery of microRNA (which is similar to siRNA, but can regulate multiple genes simultaneously). Par exemple, Day's team hopes to deliver miR-34a, which is considered a master regulator of gene expression in cancer.
In addition to Day and Gundlach, the paper's authors include Rachel Riley, a doctoral student in the Department of Biomedical Engineering; Megan Dang, a doctoral student in Department of Biomedical Engineering; Maggie Billingsley, a senior undergraduate student in the Department of Biomedical Engineering; Baxter Abraham, a doctoral student in the Department of Chemistry and Biochemistry.
Riley, who will soon begin work as a postdoctoral associate at the University of Pennsylvania, started graduate school at UD because she wanted to do science that could make a real impact on the medical field. After losing an aunt to cancer, she was especially motivated to put her talents toward research that could someday help patients.
"The Day Lab's idea of incorporating nanoparticles for specific delivery of therapeutic agents was a really unique approach, " elle a dit.
Billingsley has done research in the Day Lab since her first year at UD and wrote three peer-reviewed papers based on her work in the group. In 2017, she was the first author on a paper published in PLOS Un . Prochain, Billingsley will attend graduate school at the University of Pennsylvania, where she will study immunotherapy. (She and Riley, a duo Day calls a "dream team, " could likely work together in the future.)
"When interviewing with graduate schools, this experience with The Day Lab was the main thing that helped me stand out in interviews and also understand what I wanted out of graduate school, " Billingsley said. "I have had so many opportunities to go down my own path and also work with others on new methods, idées, and areas of research."
This paper also gave Billingsley a taste of an important aspect of scientific discovery.
"We found some results that conflicted with literature, which was a new experience for me, " she said. "That was more exciting that just confirming what was expected."
Globalement, Day and her team are excited to further pursue this technology to reveal its potential as a high precision cancer therapy.