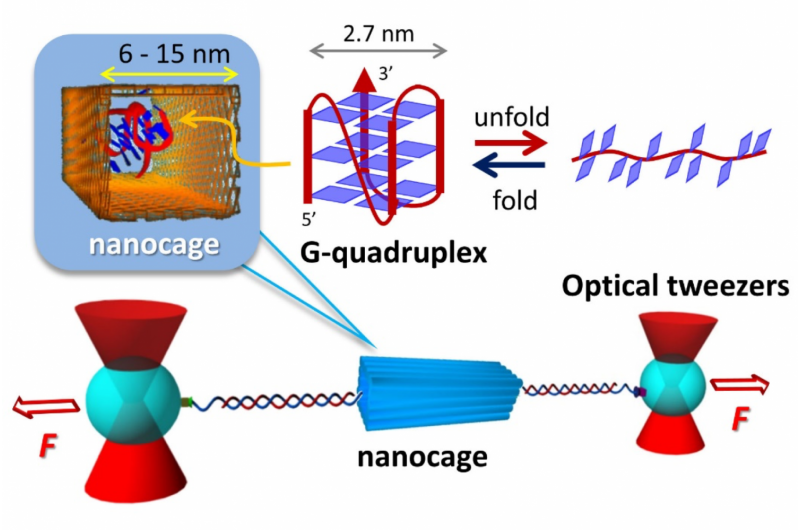
La nanocage faite d'ADN, entoure un G-quadruplex, un groupe d'acides nucléiques de guanine, les 'G' dans la séquence d'ADN. La molécule G-quadruplex se replie et se déplie 100 fois plus vite à l'intérieur de la nanocage que sans nanocage, indiquant que le nanoespace stabilise la structure. Les chercheurs ont utilisé des pincettes optiques pour mener l'expérience à l'échelle nanométrique. Crédit :iCeMS de l'Université de Kyoto
Les macromolécules se replient et se déplient régulièrement à l'intérieur des cellules. Leurs diverses structures tridimensionnelles aident à déterminer leurs fonctions. Comprendre le repliement des molécules peut faire la lumière sur des processus physiques complexes qui peuvent influencer les maladies, cancers et allergies.
Les G-quadruplexes sont des groupes d'acides nucléiques de guanine, les 'G' dans la séquence d'ADN, qui forment des formes spécifiques aux allures futuristes, immeubles de bureaux de trois étages. Ils ont longtemps été rejetés comme n'ayant pas de fonction biologique, mais sont maintenant pensés pour aider à réguler l'expression des gènes, y compris pour les maladies. Comprendre les processus physiques que subissent ces composés lorsqu'ils se replient dans des espaces extra-étroits pourrait un jour aider à développer des traitements médicamenteux qui les ciblent.
Mener des expériences pour en savoir plus sur le processus de repliement dans des zones confinées est extrêmement difficile car il est facile de perturber non seulement la molécule cible, qui ne mesure que quelques nanomètres de long, mais aussi les infrastructures environnantes, qui est juste une fraction plus grande.
Une équipe dirigée par Hiroshi Sugiyama et Masayuki Endo de l'Institute for Integrated Cell-Material Sciences (iCeMS) de l'Université de Kyoto, en collaboration avec l'équipe de la Kent State University, a conçu des structures et un système expérimental qui manipulent avec succès les G-quadruplexes à l'intérieur des nanocages, qui sont également constitués d'ADN. L'équipe a mesuré comment des espaces de tailles différentes affectent la stabilité thermodynamique et la cinétique de dépliement et de repliement de ces molécules.
"Sous le nano-espace confiné, les structures G-quadruplex ont révélé une cinétique de pliage rapide sans précédent avec des stabilités mécaniques et thermodynamiques accrues, qui appuyait directement les prédictions théoriques, " concluent les chercheurs dans leur étude publiée récemment dans la revue Nature Nanotechnologie .
Les chercheurs ont construit des nanocages en forme de rectangle à partir d'ADN qu'ils ont enroulés autour d'une molécule G-quadruplex. Des attaches faites d'encore plus d'ADN attachaient la molécule à deux billes. Les perles, contrôlé par des lasers appelés pinces optiques, exerce une force sur la molécule. Cela a incité la molécule à se déplier puis à se replier. Il n'y avait pas d'interférence entre la nanocage et la cible, car ils ont tous les deux des charges négatives et se repoussent comme des aimants.
L'équipe a construit petit, nanocages moyennes et grandes. Les molécules se sont dépliées et repliées 100 fois plus rapidement dans les petites et moyennes nanocages par rapport aux molécules sans nanocages.
Les résultats soutiennent les prédictions faites par d'autres chercheurs dans le domaine, mais c'est la première démonstration sans interaction entre la molécule et la cage. Les chercheurs prévoient que la méthode peut être appliquée pour l'observation d'autres biomolécules telles que des protéines en utilisant des nanocages conçues plus précisément.