Crédit :Société chimique américaine
Des téléphones portables et ordinateurs portables aux véhicules électriques, Les batteries lithium-ion sont la source d'énergie qui alimente la vie quotidienne. Mais ces dernières années, ils ont également attiré l'attention pour avoir pris feu. Dans un effort pour développer une batterie plus sûre, les scientifiques rapportent dans la revue ACS Lettres nano que l'ajout de nanofils peut non seulement améliorer les capacités de résistance au feu de la batterie, mais aussi ses autres propriétés.
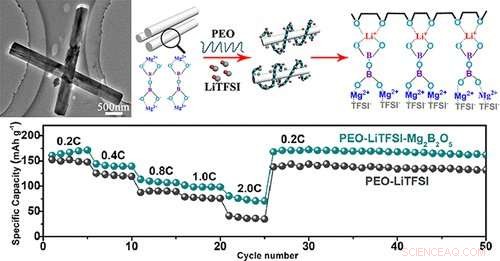
Dans les batteries lithium-ion (LIB), les ions lithium vont et viennent entre les électrodes à travers un électrolyte. Les LIB traditionnels ont un électrolyte liquide composé de sels et de solvants organiques, mais il s'évapore facilement et peut être un risque d'incendie. Donc, les chercheurs ont tourné leur attention vers les électrolytes à l'état solide comme alternatives potentielles. Plusieurs options ont été proposées pour les électrolytes à l'état solide, mais la plupart ne sont pas stables ou ne peuvent pas répondre aux demandes à grande échelle. Les électrolytes polymères ont montré du potentiel car ils sont stables, peu coûteux et flexible; mais ils ont une conductivité et des propriétés mécaniques médiocres. Donc, les scientifiques ont ajouté une gamme de composés pour améliorer l'électrolyte. Xinyong Tao et ses collègues fabriquaient auparavant du borate de magnésium (Mg
L'équipe a mélangé l'électrolyte à l'état solide avec 5, dix, 15 et 20 pour cent en poids du Mg