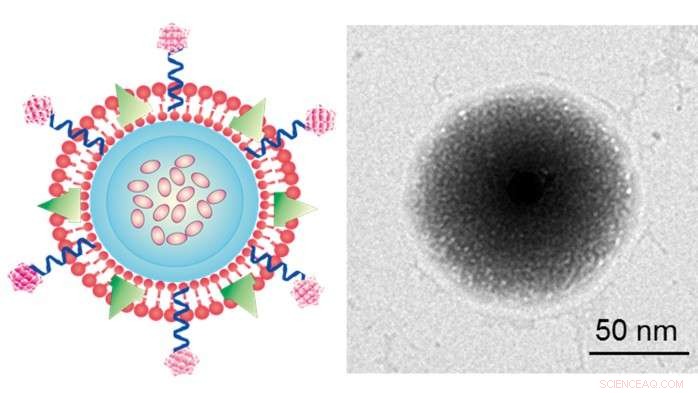
Sur la gauche se trouve la conception schématique du système d'administration de nanogel recouvert d'une membrane plaquettaire chargé TRAIL/Dox. Le TRAIL est fixé à la surface de la membrane et Dox est chargé dans le noyau du nanogel. Sur la droite se trouve une image au microscope électronique à transmission du système d'administration du médicament. Le noir est le noyau synthétique nanogel, l'enveloppe extérieure est la membrane plaquettaire.
Des chercheurs ont pour la première fois mis au point une technique qui enrobe des médicaments anticancéreux dans des membranes fabriquées à partir des propres plaquettes d'un patient, permettant aux médicaments de durer plus longtemps dans le corps et d'attaquer à la fois les tumeurs cancéreuses primaires et les cellules tumorales circulantes qui peuvent provoquer la métastase d'un cancer. Le travail a été testé avec succès dans un modèle animal.
"Il y a deux avantages clés à utiliser des membranes plaquettaires pour enrober des médicaments anticancéreux, " dit Zhen Gu, auteur correspondant d'un article sur les travaux et professeur adjoint au programme conjoint de génie biomédical de la North Carolina State University et de l'Université de Caroline du Nord à Chapel Hill. "D'abord, la surface des cellules cancéreuses a une affinité pour les plaquettes – elles se collent les unes aux autres. Seconde, parce que les plaquettes proviennent du propre corps du patient, les porteurs de médicaments ne sont pas identifiés comme des objets étrangers, donc durent plus longtemps dans le sang."
"Cette combinaison de caractéristiques signifie que les médicaments peuvent non seulement attaquer le site tumoral principal, mais sont plus susceptibles de trouver et de s'attacher aux cellules tumorales circulant dans le sang - attaquant essentiellement les nouvelles tumeurs avant qu'elles ne commencent, " dit Quanyin Hu, auteur principal de l'article et titulaire d'un doctorat. étudiant dans le programme conjoint de génie biomédical.
Voici comment fonctionne le processus. Le sang est prélevé sur un patient – une souris de laboratoire dans le cas de cette recherche – et les plaquettes sont recueillies à partir de ce sang. Les plaquettes isolées sont traitées pour extraire les membranes plaquettaires, qui sont ensuite placés dans une solution avec un gel nanométrique contenant le médicament anticancéreux doxorubicine (Dox), qui attaque le noyau d'une cellule cancéreuse. La solution est compressée, forcer le gel à travers les membranes et créer des sphères nanométriques constituées de membranes plaquettaires avec des noyaux de Dox-gel. Ces sphères sont ensuite traitées pour que leurs surfaces soient enduites du médicament anticancéreux TRAIL, qui est le plus efficace pour attaquer les membranes cellulaires des cellules cancéreuses.
Lorsqu'il est libéré dans la circulation sanguine d'un patient, ces pseudo-plaquettes peuvent circuler jusqu'à 30 heures, contre environ six heures pour les véhicules à l'échelle nanométrique sans revêtement.
Lorsqu'une des pseudo-plaquettes entre en contact avec une tumeur, trois choses se produisent plus ou moins en même temps. D'abord, les protéines P-Selectin sur la membrane plaquettaire se lient aux protéines CD44 à la surface de la cellule cancéreuse, le verrouiller en place. Seconde, le TRAIL à la surface de la pseudo-plaquette attaque la membrane des cellules cancéreuses. Troisième, la pseudo-plaquette nanométrique est effectivement avalée par la plus grande cellule cancéreuse. L'environnement acide à l'intérieur de la cellule cancéreuse commence alors à briser la pseudo-plaquette, libérant le Dox pour attaquer le noyau de la cellule cancéreuse.
Dans une étude utilisant des souris, les chercheurs ont découvert que l'utilisation de Dox et TRAIL dans le système d'administration de médicaments pseudo-plaquettaires était significativement plus efficace contre les grosses tumeurs et les cellules tumorales circulantes que l'utilisation de Dox et TRAIL dans un système d'administration de nano-gel sans membrane plaquettaire.
"Nous aimerions faire des tests précliniques supplémentaires sur cette technique, " dit Gu. " Et nous pensons qu'il pourrait être utilisé pour délivrer d'autres médicaments, tels que ceux ciblant les maladies cardiovasculaires, dans lequel la membrane plaquettaire pourrait nous aider à cibler des sites pertinents dans le corps."