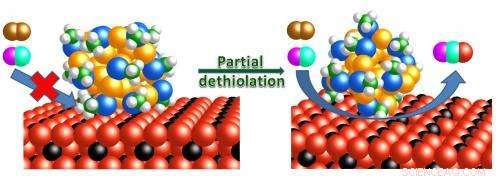
Le mécanisme de réaction de l'oxydation du monoxyde de carbone est montré sur des nanoclusters d'or intacts et partiellement dépourvus de ligand, supportés par des tiges d'oxyde de cérium.Crédit :Wu, Z., et al.
(Phys.org) — La vieille pensée était que l'or, bien que bon pour les bijoux, n'était pas d'une grande utilité pour les chimistes car il est relativement peu réactif. Cela a changé il y a une dizaine d'années lorsque les scientifiques ont découvert un riche filon de découvertes révélant que ce métal noble, lorsqu'il est structuré en particules de taille nanométrique, peut accélérer les réactions chimiques importantes pour atténuer les polluants environnementaux et produire des produits chimiques de spécialité difficiles à fabriquer. Les nanoparticules d'or catalytiques ont depuis suscité des centaines d'articles dans des revues scientifiques. Alors que le marché mondial des catalyseurs devrait atteindre 19,5 milliards de dollars d'ici 2016, les nanoparticules d'or peuvent avoir une importance commerciale aussi bien qu'intellectuelle, car ils pourraient conduire à terme à de nouveaux catalyseurs pour l'énergie, pharmacologie et divers produits de consommation.
Mais avant que les nanoparticules d'or puissent être utiles aux consommateurs, les chercheurs doivent les rendre à la fois stables et actifs. Récemment, les scientifiques ont appris à faire minuscule, amas hautement ordonnés avec des nombres très spécifiques d'atomes d'or qui sont stabilisés par des composés appelés ligands. Ces amas d'or stabilisés et leurs ligands peuvent être considérés comme de grosses molécules. En collaboration avec des scientifiques de l'Université Carnegie Mellon, des chercheurs du laboratoire national d'Oak Ridge du ministère de l'Énergie ont découvert une nouvelle molécule d'or, un catalyseur contenant exactement 25 atomes d'or, qui est puissant ainsi que sophistiqué. Il catalyse la conversion d'une variété de molécules, y compris la transformation du monoxyde de carbone toxique en dioxyde de carbone inoffensif, une réaction qui peut trouver une application dans des appareils à proximité de conduits de fumée ou de poêles à bois. Malheureusement, les ligands qui créent et stabilisent les clusters modifiés bloquent également les sites mêmes nécessaires pour catalyser la conversion du monoxyde de carbone en dioxyde de carbone.
"Les ligands sont des épées à double tranchant, " a déclaré le responsable de l'étude Zili Wu de l'ORNL, dont l'enquête a été menée dans le groupe catalyse de l'ORNL, qui est dirigé par Steve Overbury. "Nous sommes intéressés par l'utilisation de clusters d'or comme catalyseurs ou précurseurs de catalyseurs. Les ligands d'une part stabilisent la structure des particules d'or mais d'autre part diminuent leurs performances catalytiques. Équilibrer ces deux facteurs est la clé pour créer un nouveau système catalytique. Un moyen est d'utiliser un oxyde métallique (ici, oxyde de cérium) comme ligand inorganique pour stabiliser les amas d'or lorsque le ligand organique doit être retiré pour la catalyse.
De nombreux systèmes catalytiques sont constitués de particules métalliques aux propriétés catalytiques placées sur un support d'oxyde métallique aux propriétés catalytiques propres. Le métal et l'oxyde métallique travaillent ensemble pour créer un nouveau type d'activité catalytique. "Nous essayons de comprendre comment cela se passe, " a déclaré Wu.
Leur étude, publié dans le Journal de l'American Chemical Society , ont décrit comment les ligands ont permis au nanocluster d'or de s'arrimer sur un support d'oxyde de cérium en forme de tige. Les catalyseurs produits étaient tous identiques. Les chercheurs aimeraient concevoir de futurs supports d'oxyde sous la forme de cubes ou d'octaèdres pour découvrir comment ces nanostructures pourraient modifier la configuration de l'or et la réactivité du système de composants final. Une meilleure compréhension des agents stabilisants peut aider à concevoir de nouveaux catalyseurs pour des réactions chimiques critiques, notamment l'oxydation, hydrogénation et couplage.
Carnegie Mellon professeur Rongchao Jin, son étudiante Chenjie Zeng et les stagiaires postdoctoraux de l'ORNL Amanda Mann et Zhen-An Qiao ont synthétisé les amas d'or. Mann a fabriqué les tiges d'oxyde de cérium. Wu et Mann ont placé les grappes d'or sur les supports et ont effectué des études de réaction chimique. David Mullins de l'ORNL a effectué des mesures de la structure fine de l'absorption étendue des rayons X pour apprendre comment la taille des amas change avec la température. Larry Allard de l'ORNL a vérifié la nature des structures avec une microscopie corrigée des aberrations, et De-en Jiang, anciennement de l'ORNL mais maintenant à l'Université de Californie-Riverside, ont utilisé le cluster institutionnel d'Oak Ridge pour explorer informatiquement les structures des clusters d'or liés à des ligands.
Activer l'or
"Ces ligands affectent la réactivité - ils empoisonnent essentiellement la surface de l'or - donc l'or doit vraiment être activé, " Overbury, l'auteur principal de l'étude, expliqué. "On met l'or sur un support, et il a ces ligands qui le protègent. Nous devons éliminer ces ligands, donc nous chauffons essentiellement ce [nanocluster d'or] ou le traitons dans du gaz à des températures élevées. "
Lorsque les grappes d'or sont chauffées, les ligands commencent à se détacher et l'activité catalytique de l'or augmente. The optimal temperature for producing gold nanocluster catalysts for carbon monoxide oxidation is 498 Kelvin (225 degrees Celsius or 437 degrees Fahrenheit), dit Wu. If heating increases further, catalytic activity decreases because the gold particles become fluid and aggregate on the support.
Next the scientists are interested in varying the gold-cluster size and stabilizing the new clusters to make novel uniform catalysts. "We want to understand how other kinds of reactions can be catalyzed by these. So far we've only looked at carbon monoxide oxidation, which is kind of a test reaction, " Overbury said. "Our primary interest is using the gold-nanocluster complex as a toolbox for learning about how other complex reactions occur."
Added Overbury, "We're only just starting to mine all the catalytic possibilities for gold."
DOE's Office of Science sponsored the research described in the Journal de l'American Chemical Society papier. Raman and Fourier transform infrared spectroscopies and catalytic measurements were conducted at the Center for Nanophase Materials Sciences, a DOE Office of Science User Facility at ORNL. Extended X-ray absorption fine structure work was performed at the National Synchrotron Light Source, which is also a DOE Office of Science User Facility, at Brookhaven National Laboratory.