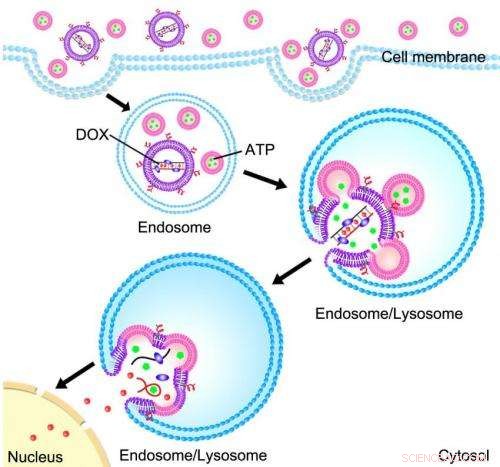
Des chercheurs en génie biomédical ont mis au point une méthode d'administration de médicaments anticancéreux qui fait essentiellement passer le médicament en contrebande dans une cellule cancéreuse avant de déclencher sa libération. Crédit :Ran Mo
(Phys.org) — Des chercheurs en génie biomédical ont mis au point une méthode d'administration de médicaments anticancéreux qui fait essentiellement passer le médicament en contrebande dans une cellule cancéreuse avant de déclencher sa libération. La méthode peut être comparée à garder une bombe anticancéreuse et son détonateur séparés jusqu'à ce qu'ils soient à l'intérieur d'une cellule cancéreuse, où ils se combinent ensuite pour détruire la cellule.
"C'est une solution efficace, moyen à action rapide d'administrer des médicaments aux cellules cancéreuses et de déclencher la mort cellulaire, " dit le Dr Ran Mo, auteur principal d'un article sur les travaux et chercheur postdoctoral dans le programme conjoint de génie biomédical de la North Carolina State University et de l'Université de Caroline du Nord à Chapel Hill. « Nous avons également utilisé des nanocapsules à base de lipides qui sont déjà utilisées pour des applications cliniques, le rendant plus proche de l'utilisation dans le monde réel."
La technique utilise des capsules à base de lipides à l'échelle nanométrique, ou liposomes, pour administrer à la fois le médicament et le mécanisme de libération dans les cellules cancéreuses. Un ensemble de liposomes contient de l'adénosine-5'-triphosphate (ATP), la soi-disant "molécule d'énergie". Un deuxième ensemble de liposomes contient un médicament anticancéreux appelé doxorubicine (Dox) qui est intégré dans un complexe de molécules d'ADN. Lorsque les molécules d'ADN entrent en contact avec des niveaux élevés d'ATP, ils déplient et libèrent le Dox. La surface des liposomes est intégrée avec des lipides ou des peptides chargés positivement, qui agissent comme des tire-bouchons pour introduire les liposomes dans les cellules cancéreuses.
Comme les liposomes sont absorbés dans une cellule cancéreuse, ils sont isolés du reste de la cellule dans un endosome - un compartiment qui retient tous les corps étrangers qui pénètrent dans une cellule.
L'environnement à l'intérieur d'un endosome est acide, ce qui provoque la fusion des liposomes Dox et des liposomes ATP, ainsi qu'à la paroi de l'endosome lui-même.
Pendant ce temps, deux autres choses se produisent simultanément. D'abord, les liposomes ATP déversent leur ATP dans les liposomes Dox, libérant le Dox de sa cage à ADN. Seconde, les parois des liposomes Dox créent une ouverture dans l'endosome, renversant leur contenu riche en Dox dans la cellule environnante, entraînant la mort cellulaire.
Dans un modèle de souris, les chercheurs ont découvert que la nouvelle technique réduisait considérablement la taille des tumeurs du cancer du sein par rapport au traitement utilisant Dox sans liposomes à l'échelle nanométrique.
"Ce travail est quelque peu similaire aux recherches précédentes que nous avons effectuées avec des nanogels à base de polymère - mais il y a une différence clé, " dit le Dr Zhen Gu, auteur principal de l'article et professeur adjoint au programme conjoint de génie biomédical. "La différence est que cette technique à base de liposomes nous permet d'introduire de l'ATP supplémentaire dans la cellule cancéreuse, libérer le médicament plus rapidement.
"Être capable d'ajuster les niveaux d'ATP est important car certaines cellules cancéreuses sont déficientes en ATP, " ajoute Gu. "Mais cette technique fonctionnerait même dans ces environnements."