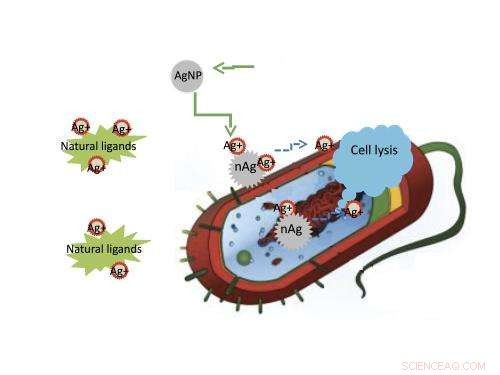
Les ions d'argent délivrés par les nanoparticules aux bactéries favorisent la lyse, le processus par lequel les cellules se décomposent et finissent par mourir, ce qui fait des nanoparticules d'argent un agent antibactérien supérieur et largement utilisé. Une nouvelle recherche de l'Université Rice a révélé que les ions d'argent, pas les particules elles-mêmes, sont toxiques pour les bactéries. Ils ont également découvert que les ligands à proximité d'une bactérie peuvent se lier aux ions argent et les empêcher d'atteindre leur cible. Crédit :Zongming Xiu/Université du riz
(Phys.org) -- Les chercheurs de l'Université Rice ont réglé une controverse de longue date sur le mécanisme par lequel les nanoparticules d'argent, le nanomatériau le plus utilisé au monde, tuer les bactéries.
Leur travail est accompagné d'un avertissement à la Nietzsche :utilisez-en suffisamment. Si vous ne les tuez pas, vous les rendez plus forts.
Les scientifiques savent depuis longtemps que les ions d'argent, qui s'écoulent des nanoparticules lorsqu'elles sont oxydées, sont mortels pour les bactéries. Les nanoparticules d'argent sont utilisées un peu partout, y compris en cosmétique, des chaussettes, contenants alimentaires, détergents, sprays et une large gamme d'autres produits pour arrêter la propagation des germes.
Mais les scientifiques ont également soupçonné que les nanoparticules d'argent elles-mêmes peuvent être toxiques pour les bactéries, en particulier le plus petit d'entre eux à environ 3 nanomètres. Pas si, selon l'équipe Rice qui a publié ses résultats ce mois-ci dans la revue American Chemical Society Lettres nano .
En réalité, lorsque la possibilité d'ionisation est retirée à l'argent, les nanoparticules sont pratiquement bénignes en présence de microbes, dit Pedro Alvarez, George R. Brown Professeur et président du Département de génie civil et environnemental de Rice.
"Vous seriez surpris de voir combien de fois les gens commercialisent des choses sans une compréhension mécanique complète de leur fonction, " dit Alvarez, qui étudie le devenir des nanoparticules dans l'environnement et leur toxicité potentielle, particulièrement aux humains. "Le préfixe 'nano' peut être une arme à double tranchant. Il peut vous aider à vendre un produit, et dans d'autres cas, cela pourrait susciter des inquiétudes quant à d'éventuelles conséquences imprévues. »
Il a déclaré que la réponse directe à la question vieille de dix ans est que les nanoparticules d'argent insolubles ne tuent pas les cellules par contact direct. Mais les ions solubles, lorsqu'il est activé par oxydation au voisinage de bactéries, faire le travail bien.
Pour comprendre cela, les chercheurs ont dû dépouiller les particules de leurs pouvoirs. "Notre attente initiale était que plus une particule est petite, plus la toxicité est grande, " dit Zongming Xiu, un chercheur postdoctoral Rice et auteur principal de l'article. Xiu a entrepris de tester des nanoparticules, à la fois disponibles dans le commerce et synthétisés sur mesure de 3 à 11 nanomètres, pour voir s'il y avait une corrélation entre la taille et la toxicité.
"Nous n'avons pas pu obtenir des résultats cohérents, " a-t-il dit. " C'était très frustrant et vraiment bizarre. "
Xiu a décidé de tester la toxicité des nanoparticules dans un environnement anaérobie, c'est-à-dire scellé à l'intérieur d'une chambre sans exposition à l'oxygène - pour contrôler la libération des ions d'argent. Il a découvert que les particules filtrées étaient beaucoup moins toxiques pour les microbes que les ions d'argent.
En collaboration avec le laboratoire de la chimiste Rice Vicki Colvin, l'équipe a ensuite synthétisé des nanoparticules d'argent à l'intérieur de la chambre anaérobie pour éliminer tout risque d'oxydation. "Nous avons trouvé les particules, même jusqu'à une concentration de 195 parties par million, n'étaient toujours pas toxiques pour les bactéries, " dit Xiu. " Mais pour l'argent ionique, une concentration d'environ 15 parties par milliard tuerait toutes les bactéries présentes. Cela nous a dit que la particule est 7, 665 fois moins toxique que les ions argent, indiquant une toxicité négligeable."
"Le but de cette expérience, " Alvarez a dit, "était de montrer que beaucoup de gens obtenaient des données qui étaient confondues par une libération d'ions, qui se produisait pendant l'exposition dont ils n'étaient peut-être pas au courant."
Alvarez a suggéré que la méthode anaérobie de l'équipe pourrait être utilisée pour tester la toxicité de nombreux autres types de nanoparticules métalliques et pourrait aider à affiner les qualités antibactériennes des particules d'argent. Dans leurs tests, les chercheurs de Rice ont également trouvé des preuves d'hormèse; E. coli a été stimulé par les ions d'argent lorsqu'ils ont rencontré des doses trop faibles pour les tuer.
"Finalement, nous voulons contrôler le taux de libération (ionique) pour obtenir les concentrations souhaitées qui font juste le travail, " Alvarez a dit. " Vous ne voulez pas dépasser et surcharger l'environnement avec des ions toxiques tout en appauvrissant l'argent, qui est un métal noble, une ressource précieuse – et un désinfectant un peu cher. Mais vous ne voulez pas sous-estimer, Soit."
Il a déclaré que la découverte devrait déplacer le débat sur la taille, forme et revêtement de nanoparticules d'argent. "Bien sûr qu'ils comptent, " Alvarez a dit, "mais seulement indirectement, dans la mesure où ces variables affectent la vitesse de dissolution des ions. Le principal déterminant de la toxicité est les ions d'argent. L'accent devrait donc être mis sur les processus de transfert de masse et les mécanismes de libération contrôlée. »
"Ces résultats suggèrent que l'application antibactérienne des nanoparticules d'argent pourrait être améliorée et que les impacts environnementaux pourraient être atténués en modulant le taux de libération des ions, par exemple, grâce à des revêtements polymères réactifs, " dit Xiu.