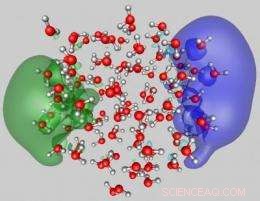
Cette image montre le mode d'attachement en surface de deux électrons en excès à un amas d'eau (diamètre moyen proche de 2 nm) composé de 105 molécules. La configuration présentée a été obtenue à partir de simulations quantiques de premier principe. Les deux fonctions d'onde occupées chacune par un électron en excès, représenté en bleu et vert, sont localisés sur les côtés opposés de l'amas et ils sont représentés superposés sur les molécules d'eau. Les oxygènes et hydrogènes des molécules d'eau sont représentés par des sphères rouges et grises, respectivement. Crédit :Uzi Landman/Georgia Tech
Les scientifiques ont découvert les étapes fondamentales du chargement de gouttelettes d'eau de taille nanométrique et dévoilé le mécanisme longtemps recherché de l'émission d'hydrogène à partir de l'eau irradiée. En travaillant ensemble au Georgia Institute of Technology et à l'Université de Tel Aviv, les scientifiques ont découvert lorsque le nombre de molécules d'eau dans un cluster dépasse 83, deux électrons en excès peuvent s'y attacher - formant des diélectrons - ce qui en fait une nanogouttelette doublement chargée négativement. Par ailleurs, les scientifiques ont trouvé des preuves expérimentales et théoriques que dans les gouttelettes composées de 105 molécules ou plus, les diélectrons en excès participent à un processus de séparation de l'eau entraînant la libération d'hydrogène moléculaire et la formation de deux anions hydroxyde solvatés. Les résultats paraissent dans le numéro du 30 juin du Journal de chimie physique A .
On sait depuis le début des années 1980 que si des électrons uniques peuvent se fixer à de petits amas d'eau contenant aussi peu que deux molécules, seuls des amas beaucoup plus gros peuvent attacher plus que des électrons isolés. Taille sélectionnée, à électrons multiples, des amas d'eau chargés négativement n'ont pas été observés jusqu'à présent.
Comprendre la nature des électrons en excès dans l'eau a attiré l'attention des scientifiques pendant plus d'un demi-siècle, et les électrons hydratés sont connus pour apparaître comme des réactifs importants dans les réactions aqueuses induites par la charge et les processus de biologie moléculaire. De plus, depuis la découverte au début des années 1960 que l'exposition de l'eau aux rayonnements ionisants provoque l'émission d'hydrogène moléculaire gazeux, les scientifiques ont été intrigués par le mécanisme sous-jacent à ce processus. Après tout, les liaisons dans les molécules d'eau qui retiennent les atomes d'hydrogène aux atomes d'oxygène sont très fortes. La réaction diélectron-hydrogène-évolution (DEHE), qui produit de l'hydrogène gazeux et des anions hydroxyde, peut jouer un rôle dans les réactions radio-induites avec de l'ADN oxydé qui sont à l'origine de la mutagenèse, cancer et autres maladies.
"La fixation de plusieurs électrons aux gouttelettes d'eau est contrôlée par un équilibre fin entre les forces qui lient les électrons aux molécules d'eau polaires et la forte répulsion entre les électrons chargés négativement, " a déclaré Uzi Landman, Regents' et professeur d'institut de physique, Président F.E. Callaway et directeur du Center for Computational Materials Science (CCMS) à Georgia Tech.
"En outre, la liaison d'un électron à l'amas perturbe les arrangements d'équilibre entre les molécules d'eau à liaison hydrogène et cela doit également être contrebalancé par les forces de liaison attractives. Pour calculer le modèle et la force de la charge à un ou deux électrons de gouttelettes d'eau de taille nanométrique, nous avons développé et utilisé des simulations de dynamique moléculaire en mécanique quantique de principes premiers qui vont bien au-delà de celles qui ont été utilisées dans ce domaine, " il ajouta.
Les investigations sur des clusters sélectionnés de taille contrôlée permettent d'explorer les propriétés intrinsèques d'agrégats de matériaux de taille finie, ainsi que de sonder l'évolution en fonction de la taille des propriétés des matériaux de l'échelle moléculaire nanométrique au régime de phase condensée.
Dans les années 1980, Landman, avec les chercheurs principaux du CCMS Robert Barnett, feu Charles Cleveland et Joshua Jortner, professeur de chimie à l'université de Tel Aviv, découvert qu'il existe deux manières pour les électrons en excès de se fixer aux amas d'eau - l'une par laquelle ils se lient à la surface de la goutte d'eau, et l'autre où ils se localisent dans une cavité à l'intérieur de la goutte, comme dans le cas de l'eau en vrac. Ensuite, Landman, Barnett et l'étudiant diplômé Harri-Pekka Kaukonen ont rendu compte en 1992 d'études théoriques concernant l'attachement de deux électrons en excès aux amas d'eau. Ils ont prédit qu'une telle double charge ne se produirait que pour des nano-gouttelettes suffisamment grosses. Ils ont également commenté la possible réaction de dégagement d'hydrogène. Aucun autre travail sur la charge diélectronique des gouttelettes d'eau n'a suivi depuis.
C'est jusqu'à récemment, quand Landman, aujourd'hui l'un des leaders mondiaux dans le domaine des clusters et des nanosciences, et Barnett ont fait équipe avec Ori Chesnovsky, professeur de chimie, et associée de recherche Rina Giniger à l'Université de Tel Aviv, dans un projet commun visant à comprendre le processus de charge diélectronique des amas d'eau et le mécanisme de la réaction qui s'ensuit - ce qui n'avait pas été observé auparavant dans des expériences sur des gouttelettes d'eau. En utilisant à grande échelle, des simulations dynamiques de premier plan à la pointe de la technologie, développé au CCMS, with all valence and excess electrons treated quantum mechanically and equipped with a newly constructed high-resolution time-of-flight mass spectrometer, the researchers unveiled the intricate physical processes that govern the fundamental dielectron charging processes of microscopic water droplets and the detailed mechanism of the water-splitting reaction induced by double charging.
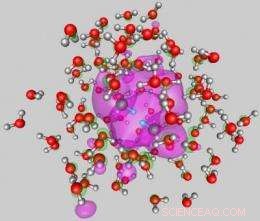
This image shows the internal attachment mode of two electrons to a water cluster (average diameter of close to 2nm) comprised of 105 molecules. The shown configuration was obtained from first-principles quantum simulations. The wave function of the two excess electrons is depicted in pink and it is shown superimposed on the water molecules of the cluster. The compact dielectron distribution is localized in a hydration cavity in the interior of the cluster. The configuration shown here corresponds to the start of the dielectron hydrogen-evolution reaction. The protons of the two reacting neighboring water molecules, located approximately in the middle of the figure, are depicted by smaller blue spheres. Together with the dielectron these protons would form, in the course of the reaction, a hydrogen molecule. The oxygens and hydrogens of the water molecules are represented by red and gray spheres, respectivement. Credit:Uzi Landman/Georgia Tech
The mass spectrometric measurements, performed at Tel Aviv, revealed that singly charged clusters were formed in the size range of six to more than a couple of hundred water molecules. Cependant, for clusters containing more than a critical size of 83 molecules, doubly charged clusters with two attached excess electrons were detected for the first time. Most significantly, for clusters with 105 or more water molecules, the mass spectra provided direct evidence for the loss of a single hydrogen molecule from the doubly charged clusters.
The theoretical analysis demonstrated two dominant attachment modes of dielectrons to water clusters. The first is a surface mode (SS'), where the two repelling electrons reside in antipodal sites on the surface of the cluster (see the two wave functions, depicted in green and blue, in Figure 1). The second is another attachment mode with both electrons occupying a wave function localized in a hydration cavity in the interior of the cluster the so-called II binding mode (see wave function depicted in pink in Figure 2). While both dielectron attachment modes may be found for clusters with 105 molecules and larger ones, only the SS' mode is stable for doubly charged smaller clusters.
"De plus, starting from the II, internal cavity attachment mode in a cluster comprised of 105 water molecules, our quantum dynamical simulations showed that the concerted approach of two protons from two neighboring water molecules located on the first shell of the internal hydration cavity, leads, in association with the cavity-localized excess dielectron (see Figure 2), to the formation of a hydrogen molecule. The two remnant hydroxide anions diffuse away via a sequence of proton shuttle processes, ultimately solvating near the surface region of the cluster, while the hydrogen molecule evaporates, " said Landman.
"Quoi de plus, in addition to uncovering the microscopic reaction pathway, the mechanism which we discovered requires initial proximity of the two reacting water molecules and the excess dielectron. This can happen only for the II internal cavity attachment mode. Par conséquent, the theory predicts, in agreement with the experiments, that the reaction would be impeded in clusters with less than 105 molecules where the II mode is energetically highly improbable. Maintenant, that's a nice consistency check on the theory, " il ajouta.
As for future plans, Landman remarked, "While I believe that our work sets methodological and conceptual benchmarks for studies in this area, there is a lot left to be done. Par exemple, while our calculated values for the excess single electron detachment energies are found to be in quantitative agreement with photoelectron measurements in a broad range of water cluster sizes containing from 15 to 105 molecules providing a consistent interpretation of these measurements, we would like to obtain experimental data on excess dielectron detachment energies to compare with our predicted values, " il a dit.
"En outre, we would like to know more about the effects of preparation conditions on the properties of multiply charged water clusters. We also need to understand the temperature dependence of the dielectron attachment modes, the influence of metal impurities, and possibly get data from time-resolved measurements. The understanding that we gained in this experiment about charge-induced water splitting may guide our research into artificial photosynthetic systems, as well as the mechanisms of certain bio-molecular processes and perhaps some atmospheric phenomena."
"Tu sais, " he added. "We started working on excess electrons in water clusters quite early, in the 1980s close to 25 years ago. If we are to make future progress in this area, it will have to happen faster than that."