À un moment donné de votre vie, vous avez probablement suivi – ou suivrez éventuellement – un cours de physique. C'est pour votre bien, bien qu'il soit possible que vous ne ressentiez pas la vérité à ce moment-là. L'une des raisons pour lesquelles les cours de physique sont utiles est de mettre un nom et une image sur des choses que vous connaissez déjà.
Prenez la loi de Boyle, l'une des lois des gaz qui régit la façon dont la température, le volume et la pression affectent les gaz. La loi de Boyle, du nom de Robert Boyle, le scientifique du 17ème siècle qui a publié pour la première fois à ce sujet, est une description de la relation entre la pression et le volume de gaz dans un récipient (étant donné que la température reste constante). Vos yeux viennent peut-être de devenir vitreux, mais vous savez déjà tout sur la loi de Boyle, et c'est pourquoi vous avez besoin d'un cours de physique pour mettre un nom sur ce que vous avez déjà découvert lorsque vous avez fait éclater votre premier ballon. Parfois, la science n'est qu'un moyen d'établir des liens entre ce que vous savons et nous savoir, collectivement.
La loi de Boyle dit qu'il existe une relation inverse entre le volume à l'intérieur d'un récipient rempli de gaz et la pression sous laquelle se trouve le gaz. Par exemple, supposons que vous ayez gonflé un ballon à moitié rempli de gaz — dans ce cas, le gaz est le mélange de vapeur d'eau et de dioxyde de carbone qui sort de nos poumons lorsque nous expirons.
Dans le ballon à moitié plein, il y a beaucoup d'espace pour que tous ces atomes de gaz puissent se cogner sans trop encombrer l'un d'entre eux - le ballon lui-même peut être assez souple. Cependant, lorsque vous pincez tout l'air à une extrémité du ballon, la partie du ballon qui contient du gaz devient tendue. Le nombre de molécules de gaz dans le ballon n'a pas changé, juste la taille du conteneur. Si vous réduisiez ensuite la taille du récipient, la pression à l'intérieur du ballon augmenterait au point que le ballon finirait par éclater.
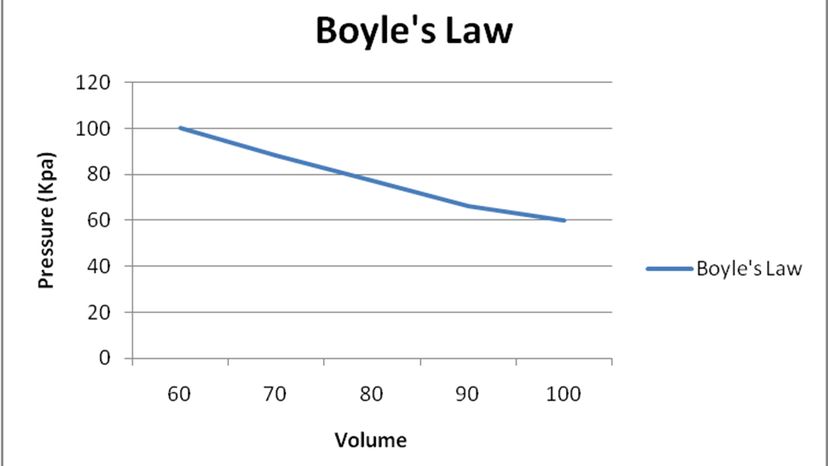
La loi de Boyle dit que lorsque le volume d'un récipient contenant du gaz diminue, la pression à l'intérieur du récipient augmente - et, inversement, lorsque le volume augmente, la pression diminue. Boyle a même proposé une formule mathématique pour nous aider à déterminer la pression ou le volume d'un gaz dans un espace confiné :peu importe comment vous modifiez la pression ou le volume dans un récipient de gaz, multiplier l'un par l'autre donnera un produit constant. .
Maintenant c'est intéressantRobert Boyle s'intéressait au concept de race et croyait que la couleur de la peau était héritée plutôt que le produit de l'exposition au soleil, comme le croyaient d'autres philosophes naturels de l'époque.