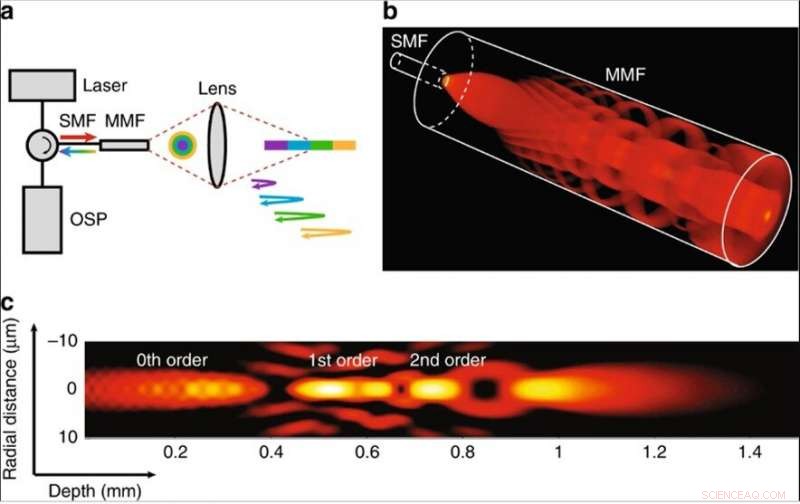
(a) Le concept d'utilisation d'un système de fibre monomode-multimode pour la réflectométrie codée en profondeur. Le motif de couleur correspond à différents modes de propagation. Fibre monomode SMF, Fibre multimode MMF, Unité de traitement du signal optique OSP. (b) Rendu 3D du profil d'intensité à l'intérieur de la fibre multimode montrant les processus de génération de quelques modes d'un système de fibre SMM. Les dimensions latérales et axiales ne sont pas dessinées à l'échelle. Le SMF a un diamètre de champ de mode de 5 μm, et le MMF a un diamètre de noyau de 50 μm et une longueur de 1,2 mm. Une longueur d'onde système de 800 nm est supposée. (c) Simulations de la distribution de l'intensité du champ focalisé dans l'espace image. La longueur de l'entretoise est de 1,6 mm, et l'objectif a une distance focale d'environ 0,5 mm. Nous supposons un indice de réfraction de 1,34 dans l'espace image. La distribution de l'intensité du champ focalisé est normalisée par l'intensité maximale et affichée sur l'échelle dB avec une plage dynamique de 16 dB. Crédit :Lumière :Science &Applications, doi:10.1038/s41377-019-0211-5
Une nouvelle technique d'imagerie développée par Biwei Yin et des chercheurs interdisciplinaires du Massachusetts General Hospital et de la Harvard Medical School aux États-Unis, fournit une résolution au niveau subcellulaire pour imager le système vasculaire du cœur. Par conséquent, les cardiologues peuvent étudier et diagnostiquer les maladies coronariennes humaines avec une plus grande précision. Classiquement, les cardiologues utilisent la tomographie par cohérence optique (OCT) intravasculaire pour évaluer l'accumulation de plaque coronarienne, qui peut rétrécir les artères et provoquer une maladie coronarienne.
La technique OCT est, cependant, limité par une résolution latérale de seulement 30 microns (µm), les chercheurs sont donc incapables d'obtenir des images au niveau subcellulaire pour comprendre la maladie. Le système d'imagerie intravasculaire par interférométrie à quelques modes nouvellement développé contient une résolution de trois microns pour fournir des images des structures cellulaires et subcellulaires dans la paroi artérielle. La vue améliorée peut fournir des informations détaillées sur les cristaux individuels, les cellules musculaires lisses et les cellules inflammatoires avec une plus grande précision lors du diagnostic de la maladie. Les travaux de recherche sont maintenant publiés sur Lumière :science et applications .
La topographie par cohérence optique (OCT) est une méthode d'imagerie traditionnelle utilisée pour obtenir une réflectance transversale principalement en milieu clinique afin d'imager une gamme de tissus humains, y compris les organes luminaux du corps. L'OCT intravasculaire (IVOCT) présente un intérêt pour accéder à la structure de la plaque coronaire et guider l'intervention coronarienne percutanée (ICP) au cours de la maladie coronarienne ; une cause majeure de mortalité dans le monde. Des bio-ingénieurs et des cardiologues ont récemment démontré des techniques IVOCT avancées, telles que l'IVOCT multimodale pour combiner la forme conventionnelle avec des modes d'imagerie et de détection supplémentaires, telles que la fluorescence et la spectroscopie proche infrarouge. Parmi les innovations supplémentaires, citons l'IVOCT sensible à la polarisation pour mesurer la biréfringence tissulaire et fournir un contraste d'imagerie, ainsi que le rythme cardiaque IVOCT pour imager de manière dense les artères coronaires in vivo sans introduire d'artefacts de mouvement. L'obstacle technique le plus difficile pour augmenter la résolution latérale d'un système OCT comprend l'ajustement de la profondeur de champ (DOF) pour l'imagerie en coupe transversale. Les études précédentes qui ont atteint un DOF accru, avoir un facteur de forme ou une complexité pour empêcher les applications cliniques intraluminales pour l'imagerie coronarienne.
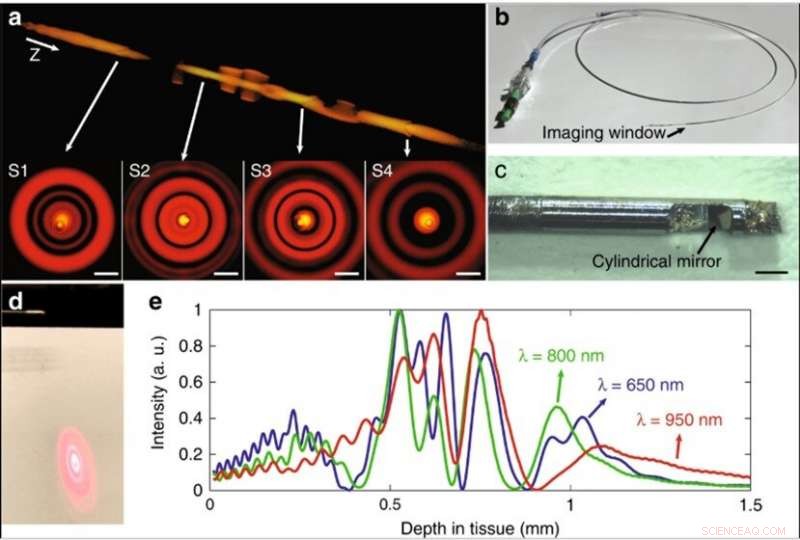
(a) Simulation de l'intensité aberrante du champ du faisceau lorsque les diffuseurs sont positionnés au centre du trajet du faisceau. Quatre diffuseurs ont été modélisés, noté S1–S4. Les diffuseurs avaient un diamètre de 2 µm et un indice de réfraction de 1,5. Le rendu 3D du champ du faisceau et les distributions d'intensité transversales montrent que l'aberration introduite par un diffuseur individuel est confinée à l'intérieur de chaque mode. Z indique la direction de propagation du faisceau. Barre d'échelle :10 μm. (b) Photographie du cathéter coronaire à échange rapide de fil de guidage 2.6-F terminé. (c) Une photographie de l'extrémité distale du cathéter, prise à l'aide d'un microscope. La sonde fibre avait un diamètre de 500µm et une longueur rigide inférieure à 4µmm. Barre d'échelle :500 μm. (d) Photographie du motif annulaire de la lumière transmise à travers la sonde à fibre optique du cathéter, correspondant à plusieurs modes de propagation. L'écran était positionné à un petit angle par rapport à la direction de propagation du faisceau, montrant que le miroir cylindrique dirige le faisceau à un angle de ~8° normal à la gaine pour réduire la réflexion spéculaire. (e) Simulation de la distribution d'intensité de champ normalisée sur l'axe par rapport à la profondeur pour la longueur d'onde centrale et les deux extrémités des spectres, montrant que l'effet de décalage focal chromatique atténue la discontinuité de l'intensité du champ. Crédit :Lumière :Science &Applications, doi:10.1038/s41377-019-0211-5
Dans le travail present, Yin et al. a décrit un système d'imagerie intravasculaire basé sur l'interférométrie à quelques modes avec un DOF étendu pour l'imagerie en coupe transversale à résolution cellulaire, sur une plage de profondeur supérieure à 1 mm. La technologie leur a permis d'observer les structures cellulaires et sous-cellulaires d'artères intactes de taille coronaire humaine ex vivo et in vivo à l'aide d'un système flexible, cathéter de diamètre submillimétrique. Les chercheurs ont utilisé une interférométrie à faible cohérence qui résolvait le retard de longueur de trajet pour décoder les informations transportées par chaque mode se déplaçant à une longueur de trajet optique différente dans la configuration expérimentale.
De multiples modes de propagation pourraient interroger simultanément un échantillon à différentes profondeurs pour transmettre le signal codé en profondeur via un canal commun pour le traitement. Le processus a augmenté la capacité d'acquisition du système de réflectométrie sans canaux d'éclairage et de détection supplémentaires. Pour visualiser les effets, Yin et al. simulé le champ de faisceau focalisé à différentes profondeurs le long du centre du trajet du faisceau, où les particules de diffusion introduisaient une aberration dans le champ du faisceau en tant que perturbation du champ. La propriété d'auto-guérison (auto-reconstruction) du processus de propagation suggère l'indépendance de chaque mode dans le milieu de diffusion.
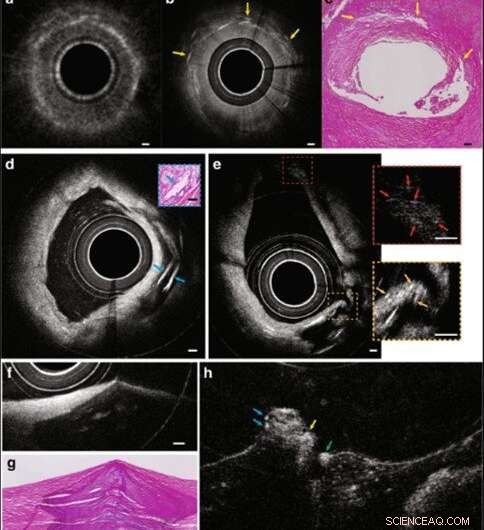
(a–c) IVOCT, IVFMI, et des images histologiques montrant une coupe transversale de l'artère contenant des dépôts de cristaux de cholestérol. Dans l'image IVOCT standard (a), les structures hautement diffusantes seraient considérées comme des accumulations de macrophages selon les critères IVOCT actuels21, tandis que l'image IVFMI (b) démontre que ces caractéristiques étaient des cristaux, un résultat qui est cohérent avec l'histologie correspondante. (d) Une coupe transversale d'une artère qui avait plusieurs cristaux de cholestérol caractérisés par des réflexions de leurs surfaces supérieure et inférieure. (e) Image montrant que l'IVFMI pouvait résoudre simultanément de petits cristaux à des distances proches de la gaine (quelques centaines de microns) et éloignées de la gaine (~ 1 mm). (F, g) IVFMI et images histologiques correspondantes d'un nodule calcifié, respectivement. (h) était à environ 1,3 mm de distance longitudinalement de (g), où un thrombus a été observé sur le nodule calcifié. Les flèches bleues sont des caractéristiques qui correspondent aux leucocytes, la flèche jaune évoque un thrombus, et la flèche verte montre une cellule qui est probablement un monocytes/macrophage. Un filtre de flou gaussien avec un rayon de 2 m a été appliqué aux images IVFMI en coupe transversale. Les barres d'échelle pour toutes les images sont de 100 μm. Crédit :Lumière :Science &Applications, doi:10.1038/s41377-019-0211-5
Sur la base du concept, l'équipe de recherche a créé un dispositif d'imagerie par interférométrie intravasculaire à quelques modes (IVFMI) avec un laser supercontinuum comme source lumineuse. Ils ont utilisé un interféromètre à faible cohérence comme unité de traitement du signal optique, un cathéter pour le codage en profondeur et la détection du signal de rétrodiffusion, ainsi que l'optomécanique pour la numérisation. À l'aide de la configuration, les chercheurs ont effectué un balayage hélicoïdal de la paroi de la lumière pour une reconstruction tridimensionnelle (3-D) de l'artère. À l'aide d'un cathéter à l'intérieur d'une artère, ils ont acquis des images en coupe transversale à 17 images par seconde. Avec une amélioration de près de 1000 fois de la résolution volumétrique, l'équipe de recherche a résolu les structures cellulaires et subcellulaires à l'aide de l'IVFMI (interférométrie intravasculaire à quelques modes) contrairement à la méthode conventionnelle IVOCT (OCT intravasculaire).
Par exemple, lorsque les scientifiques ont comparé des images IVOCT et IVFMI standard correspondant à la même coupe transversale d'une artère coronaire de cadavre humain, ils pouvaient clairement distinguer les cristaux densément emballés en utilisant uniquement l'IVFMI. En revanche, les images obtenues avec la technique IVOCT standard étaient floues et globuleuses, ce qui les rend plus susceptibles de les caractériser à tort comme des accumulations de macrophages. De la même manière, l'équipe de recherche a observé des cellules musculaires lisses à l'aide du cathéter IVFMI, qui n'a pas pu être résolu par la méthode IVOCT conventionnelle.
Reconstruction 3-D et images transversales correspondantes de données IVFMI obtenues à partir d'une artère coronaire de cadavre humain. La lumière montre des macrophages individuels résidant à la surface d'une plaque fibroathéromateuse. (une, b) Rendu 3D et images en coupe montrant une cellule individuelle (flèches jaunes) qui semble transmigrer à travers l'endothélium vers un dépôt de cristaux intimaux (flèches rouges). (c, d) rendu 3D et images en coupe montrant deux macrophages attachés à la surface endothéliale, polarisés l'un vers l'autre avec des pseudopodes étendus (flèche bleue). Barres d'échelle :50 μm. Crédit :Lumière :Science &Applications, doi:10.1038/s41377-019-0211-5.
La coupe transversale IVFMI d'une artère a également résolu les cristaux de cholestérol qui sont généralement difficiles à imager à l'aide de méthodes conventionnelles en raison de leurs réflexions notables. En raison du DOF étendu activé avec la configuration IVFMI, les chercheurs ont résolu des microstructures situées à quelques centaines de microns à quelques millimètres de la gaine du cathéter, simultanément dans un balayage circonférentiel.
Étant donné que les cellules inflammatoires entraînent le développement de plaques d'athérosclérose, Yin et al. représentaient des cellules musculaires lisses de l'intima et des macrophages subissant une diapédèse à l'aide de l'IVFMI. Les images montraient des détails fins de la masse intraluminale, y compris la présence de cellules brillantes telles que des leucocytes noyés dans le maillage de fibrine pour former ce qui semblait être un thrombus. Les chercheurs ont utilisé les données IVFMI obtenues à partir d'une paroi de lumière coronaire de cadavre pour des reconstructions 3D et ont également développé des reconstructions 3D des données IVFMI obtenues à partir d'une aorte de lapin vivant avec une plaque athérosclérotique. Ils ont détecté la plaque de la paroi artérielle normale en observant la morphologie de la surface surélevée, qui se projetait dans la lumière (espace intérieur d'une structure tubulaire telle qu'une artère).

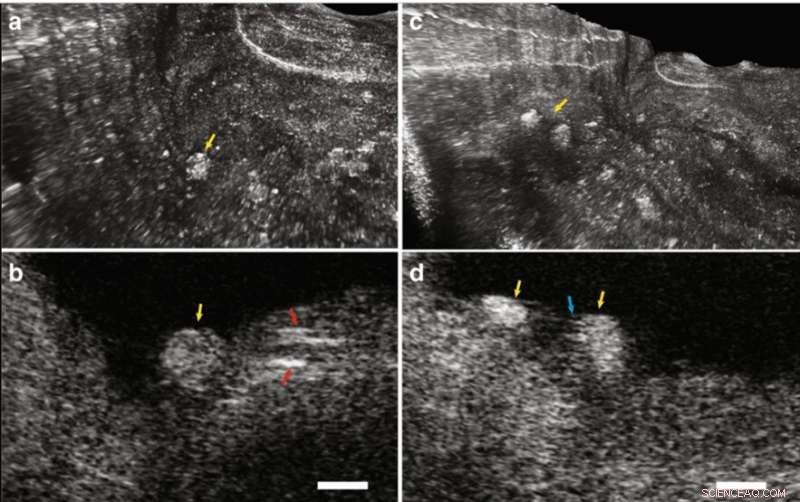
Images IVFMI d'artères de lapin acquises in vivo. (a) Reconstruction 3D de l'aorte athérosclérotique du lapin. La flèche blanche indique le fil guide. Les flèches bleues et rouges indiquent les régions de plaques d'athérosclérose. (b) Image en coupe transversale de la paroi de la lumière qui contient le tissu normal de la média aortique et la lésion athéromateuse indiquée par la flèche bleue en (a). (c) Image agrandie correspondant à la région en pointillés bleus en (b). La flèche jaune délimite une région contenant des cellules musculaires lisses intégrées dans un réseau de collagène dans une partie de la paroi aortique normale, tandis que la flèche verte indique une plaque d'athérosclérose. (d) Reconstruction 3D d'un stent implanté dans l'artère iliaque. Les flèches violettes et rouges indiquent les entretoises de stent. (e) Une image en coupe correspondant à l'emplacement indiqué par la flèche violette en (d). Les flèches oranges mettent en évidence les minuscules, ponctuer, caractéristiques hautement diffusantes qui correspondent aux plaquettes autour de l'entretoise du stent (flèche rouge), avec les flèches vertes indiquant la paroi de l'artère. Un filtre de flou gaussien avec un rayon de 2 m a été appliqué aux images IVFMI en coupe transversale. Barre d'échelle :100 m. Crédit :Lumière :Science &Applications, doi:10.1038/s41377-019-0211-5.
À l'aide d'images en coupe, l'équipe a observé un réseau de collagène et de cellules musculaires lisses dans les milieux normaux avec une clarté améliorée. Ils ont également obtenu des données IVFMI reconstruites en 3D sur un segment de la paroi de la lumière implantée avec un stent une heure avant l'imagerie. Le processus IVFMI a visualisé les détails microstructuraux des entretoises du stent avec des détails sans précédent pour l'imagerie intravasculaire. Yin et al. observé petit, haute réflectivité, des points de la taille d'un micron entourant certaines des entretoises du stent et pourraient même identifier les détails fins des plaquettes microstructurales dans les images.
De cette façon, Biwei Yin et ses collègues ont développé et démontré une technique pour surmonter les problèmes de mise en œuvre de l'interférométrie à quelques modes, augmenter la profondeur de champ (DOF) de plus d'un ordre de grandeur. La technologie de configuration optique a un faible encombrement, capacité de codage en profondeur et stabilité de la transmission, avec des applications importantes en endomicroscopie résolue en profondeur. Les résultats ont confirmé le potentiel de la nouvelle technologie pour acquérir des images avec un bon rapport signal/bruit et montrer des microstructures cellulaires et subcellulaires pertinentes pour la maladie bien définies dans les artères coronaires de cadavres humains ex vivo et les artères de lapin in vivo.
Le dispositif est physiquement et mécaniquement identique aux cathéters coronaires utilisés pour l'imagerie IVOCT conventionnelle en clinique. Ces résultats indiquent la possibilité de traduire la nouvelle technique IVFMI pour l'imagerie clinique pour visualiser la pathologie coronarienne cellulaire chez l'homme au laboratoire de cathétérisme cardiaque. La technique peut être utilisée pour visualiser l'imagerie cellulaire au-delà de l'imagerie intravasculaire pour inclure des organes luminaux tels que le tractus gastro-intestinal et les voies pulmonaires afin d'augmenter la précision du diagnostic clinique.
© 2019 Réseau Science X