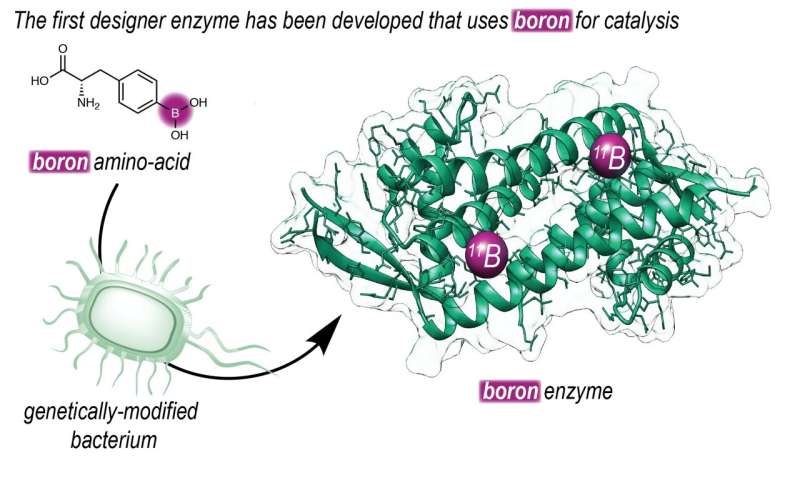
L’acide boronique est utilisé en chimie organique depuis des décennies, même s’il n’est présent dans aucun organisme. "Cela donne lieu à des réactions chimiques différentes de celles que l'on trouve dans la nature", explique Gerard Roelfes, professeur de chimie biomoléculaire et de catalyse à l'université de Groningue.
Son groupe a créé une enzyme avec de l'acide boronique en son centre réactif, puis a utilisé l'évolution dirigée pour la rendre plus sélective et améliorer son pouvoir catalytique. De plus, les réactions enzymatiques sont plus durables que les réactions chimiques classiques, car elles se déroulent à basse température et sans solvants toxiques. L'étude a été publiée en ligne dans la revue Nature le 8 mai.
L'application du bore en chimie organique remonte à environ soixante-dix ans et a reçu le prix Nobel de chimie en 1979. Ces dernières années, l'intérêt pour le bore en tant que catalyseur s'est accru, mais son utilisation dans l'industrie chimique est encore limitée.
Roelfes explique :« Jusqu'à présent, la catalyse au bore est trop lente et n'est pas très adaptée aux réactions énantiosélectives. Ces types de réactions sont utilisés pour créer des molécules chirales, qui peuvent exister en deux versions qui sont des images miroir l'une de l'autre, comme une gauche et une main droite.
"Dans de nombreux médicaments, les deux mains peuvent avoir un effet différent. Il est donc important de produire sélectivement la main appropriée, en particulier pour l'industrie pharmaceutique."
"Pour rendre cela possible, nous avons décidé d'introduire du bore dans une enzyme. Notre groupe conçoit depuis longtemps des enzymes qui n'existent pas dans la nature", explique Roelfes. Le groupe Roelfes a utilisé un code génétique élargi pour introduire un acide aminé non naturel contenant un groupe acide boronique réactif dans une enzyme. "Grâce à cette technique, nous pouvons déterminer, au niveau de l'ADN, où nous plaçons l'acide aminé dans une protéine."
Une fois qu’ils ont fabriqué une enzyme avec de l’acide boronique en son centre réactif, ils ont pu utiliser une évolution dirigée pour augmenter son efficacité, ce qui aurait pour résultat une catalyse plus rapide. Roelfes ajoute :« De plus, en plaçant l'acide boronique dans le contexte chiral d'une enzyme, nous avons pu réaliser une catalyse hautement énantiosélective. La réaction décrite est une preuve de principe et montre la manière d'exploiter le pouvoir catalytique du bore dans enzymes."
L’utilisation d’enzymes pour créer des composés organiques est importante pour l’industrie pharmaceutique. "Dans leur volonté de produire des médicaments plus écologiques et plus durables, ils envisagent la biocatalyse pour remplacer les réactions chimiques conventionnelles", explique Roelfes.
À l'Université de Groningen, des efforts concertés sont déployés pour atteindre cet objectif. Roelfes conclut :"Nous avons un certain nombre de groupes de recherche à la Faculté des sciences et de génie engagés dans ce type de travail, en utilisant différentes approches pour créer des solutions biocatalytiques pour l'industrie chimique."
Dans ce contexte, Roelfes et son équipe continueront à développer leurs enzymes à base d'acide boronique et à créer d'autres enzymes nouvelles dans la nature.
Plus d'informations : Gerard Roelfes, Catalyse du bore dans une enzyme de conception, Nature (2024). DOI :10.1038/s41586-024-07391-3. www.nature.com/articles/s41586-024-07391-3
Informations sur le journal : Nature
Fourni par l'Université de Groningen