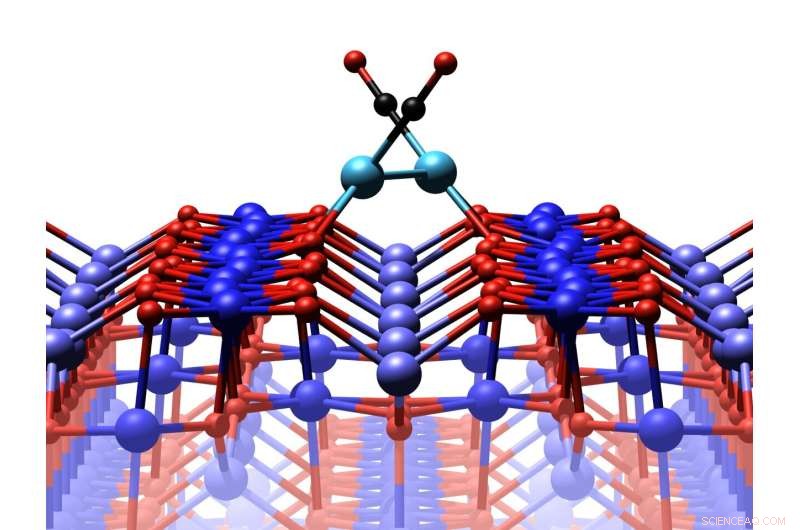
La surface de l'oxyde de fer avec deux atomes de platine, dont chacun est attaché à une molécule de monoxyde de carbone. Crédit :TU Wien
Que se passe-t-il lorsqu'un chat grimpe sur un tournesol ? Le tournesol est instable, se pliera rapidement et le chat tombera au sol. Cependant, si le chat n'a besoin que d'un coup de pouce rapide pour attraper un oiseau à partir de là, le tournesol peut agir comme une "étape intermédiaire métastable". C'est essentiellement le mécanisme par lequel les atomes individuels d'un catalyseur capturent des molécules afin de les transformer chimiquement.
Il y a plusieurs années, le groupe de physique des surfaces de l'Université de technologie de Vienne a découvert que les catalyseurs à "atome unique" de platine pouvaient oxyder le monoxyde de carbone à des températures qui, selon leurs modèles théoriques, n'auraient pas dû être possibles. Maintenant, à l'aide d'images au microscope à l'échelle atomique et de simulations informatiques complexes, ils ont pu montrer que le catalyseur lui-même et le matériau sur lequel il est ancré prennent des états "métastables" énergétiquement défavorables pendant une courte période pour permettre la réaction. se produire d'une manière spéciale. Les résultats ont été publiés dans la revue Science Advances .
Des atomes simples comme catalyseurs
Le groupe de recherche du professeur Gareth Parkinson de l'Institut de physique appliquée de la TU Wien étudie les plus petits catalyseurs possibles :des atomes de platine individuels sont placés sur une surface d'oxyde de fer. Ils entrent ensuite en contact avec le monoxyde de carbone et se transforment en dioxyde de carbone, comme cela se produit dans un échappement de voiture moderne.
"Ce processus est techniquement très important, mais ce qui se passe exactement lorsque la taille du catalyseur est réduite à la limite d'un seul atome n'était pas clair jusqu'à présent", explique Gareth Parkinson. "Dans notre groupe de recherche, nous étudions ces processus de plusieurs manières :d'une part, nous utilisons un microscope à effet tunnel pour produire des images à très haute résolution sur lesquelles vous pouvez étudier le mouvement d'atomes individuels. Et d'autre part, , nous analysons le processus de réaction avec la spectroscopie et des simulations informatiques."
Le fait que les atomes de platine soient actifs en tant que catalyseur dépend de la température. Dans l'expérience, le catalyseur est chauffé lentement et uniformément jusqu'à ce que la température critique soit atteinte, et le monoxyde de carbone est converti en dioxyde de carbone. Ce seuil est d'environ 550 Kelvin. "Cependant, cela ne correspondait pas à nos simulations informatiques d'origine", explique Matthias Meier, premier auteur de la publication actuelle. "Selon la théorie de la fonctionnelle de la densité, qui est normalement utilisée pour de tels calculs, le processus ne pouvait avoir lieu qu'à 800 Kelvin. Nous savions donc :quelque chose d'important avait été négligé ici jusqu'à présent."
Un état métastable :de courte durée, mais important
Pendant plusieurs années, l'équipe a acquis une vaste expérience avec les mêmes matériaux dans d'autres réactions, et en conséquence, une nouvelle image a émergé étape par étape. "Avec la théorie de la fonctionnelle de la densité, vous calculez normalement l'état du système qui a la plus faible énergie", explique Matthias Meier. "Cela a du sens, car c'est l'état que le système adopte le plus souvent. Mais dans notre cas, il y a un deuxième état qui joue un rôle central :un état dit métastable."
Les atomes de platine et la surface de l'oxyde de fer peuvent basculer entre différents états physiques quantiques. L'état fondamental, avec la plus faible énergie, est stable. Lorsque le système passe à l'état métastable, il revient inévitablement à l'état fondamental après un court laps de temps, comme le chat essayant d'atteindre le sommet sur un poteau d'escalade instable. Mais dans la conversion catalytique du monoxyde de carbone, il suffit que le système soit dans un état métastable pendant une très courte période :tout comme un bref instant dans un état d'escalade bancal peut suffire au chat pour attraper un oiseau avec sa patte , le catalyseur peut convertir le monoxyde de carbone à l'état métastable.
Lorsque le monoxyde de carbone est introduit pour la première fois, deux atomes de platine se lient pour former un dimère. Lorsque la température est suffisamment élevée, le dimère peut se déplacer vers une position moins favorable où les atomes d'oxygène de surface sont moins faiblement liés. Dans l'état métastable, l'oxyde de fer change sa structure atomique précisément à ce stade, libérant l'atome d'oxygène dont l'oxyde de carbone a besoin pour former du dioxyde de carbone, qui s'envole instantanément, complétant ainsi le processus de catalyse. "Si nous incluons ces états à court terme précédemment non pris en compte dans notre simulation informatique, nous obtenons exactement le résultat qui a également été mesuré dans l'expérience", déclare Matthias Meier.
"Nos résultats de recherche montrent qu'en physique des surfaces, il faut souvent beaucoup d'expérience", déclare Gareth Parkinson. "Si nous n'avions pas étudié des processus chimiques très différents au fil des ans, nous n'aurions probablement jamais résolu ce puzzle." Récemment, l'intelligence artificielle a également été utilisée avec beaucoup de succès pour analyser les processus chimiques quantiques, mais dans ce cas, Parkinson en est convaincu, cela n'aurait probablement pas été couronné de succès. Pour trouver des solutions créatives en dehors de ce que l'on pensait auparavant possible, vous avez probablement besoin d'humains après tout. Atomes simples comme catalyseurs