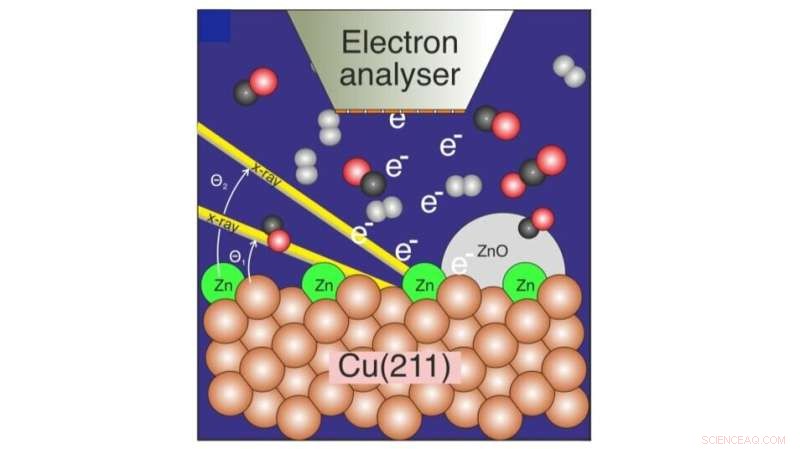
La figure illustre une surface de Cu recouverte d'une petite quantité de Zn sondée par spectroscopie photoélectronique lors de la réaction de CO2, CO et H2 en méthanol. Crédit :Université de Stockholm
Des chercheurs de l'Université de Stockholm ont pour la première fois pu étudier la surface d'un catalyseur cuivre-zinc lorsque le dioxyde de carbone est réduit en méthanol. Les résultats sont publiés dans la revue scientifique Science . Une meilleure connaissance du procédé catalytique et la possibilité de trouver des matériaux encore plus performants ouvrent la porte à une transition verte dans l'industrie chimique.
Le méthanol est actuellement l'un des produits chimiques de base pétrochimiques les plus importants, avec une production annuelle de 110 millions de tonnes métriques, et peut être converti en dizaines de milliers de produits différents et utilisé pour la fabrication, par exemple, de plastiques, de détergents, de produits pharmaceutiques et de carburants. . Le méthanol a également le potentiel de devenir un futur vecteur énergétique où, par exemple, le carburant d'aviation peut être produit en utilisant du dioxyde de carbone et de l'hydrogène capturés à partir de l'électrolyse de l'eau au lieu d'utiliser du gaz naturel. Une future transformation verte de l'industrie chimique, similaire à celle de l'acier vert, où l'énergie éolienne ou solaire entraîne des cellules électrolytiques est donc une possibilité.
"Le défi a été d'étudier expérimentalement la surface du catalyseur avec des méthodes sensibles à la surface dans des conditions de réaction réelles à des pressions et des températures relativement élevées. Ces conditions n'ont pas été réalisables pendant de nombreuses années et différentes hypothèses sur la disponibilité du zinc sous forme d'oxyde, de métal ou d'alliage avec du cuivre est apparue mais n'a pas pu être vérifiée sans ambiguïté », explique Anders Nilsson, professeur de physique chimique à l'Université de Stockholm.
"C'est fantastique que nous ayons pu faire la lumière sur ce sujet complexe de la formation de méthanol sur un catalyseur cuivre-zinc après de nombreuses années d'efforts", déclare Peter Amann, premier auteur de la publication.
"Ce qui est spécial, c'est que nous avons construit un instrument de spectroscopie photoélectronique à Stockholm qui permet d'étudier les surfaces de catalyseurs sous haute pression et ainsi d'observer directement ce qui se passe lorsque la réaction a lieu", explique David Degerman, Ph.D. étudiant en physique chimique à l'Université de Stockholm. "Nous avons ouvert une nouvelle porte vers la catalyse avec notre nouvel instrument."
"Nous avons réussi à utiliser notre instrument pour démontrer que le zinc est allié au cuivre directement à la surface, ce qui fournit des sites atomiques spéciaux où le méthanol est créé à partir de dioxyde de carbone", explique Chris Goodwin, chercheur en physique chimique à l'université de Stockholm. "Au cours des processus industriels, une petite quantité de monoxyde de carbone est mélangée, ce qui empêche la formation d'oxyde de zinc à partir de dioxyde de carbone."
"Avoir notre instrument de Stockholm sur l'une des sources de rayons X les plus brillantes au monde à PETRA III à Hambourg a été crucial pour mener l'étude", déclare Patrick Lömker, postdoctorant à l'Université de Stockholm. "Nous pouvons désormais imaginer l'avenir avec des sources encore plus brillantes lorsque la machine passera à PETRA IV."
"Nous avons maintenant les outils pour mener des recherches menant à d'éventuels autres matériaux catalyseurs qui peuvent être mieux utilisés pour s'adapter à l'hydrogène produit par électrolyse pour la transition verte de l'industrie chimique, qui est aujourd'hui entièrement fossile et représente 8 % de les émissions mondiales de dioxyde de carbone », déclare Anders Nilsson. Synthèse du méthanol :aperçu de la structure d'un catalyseur énigmatique