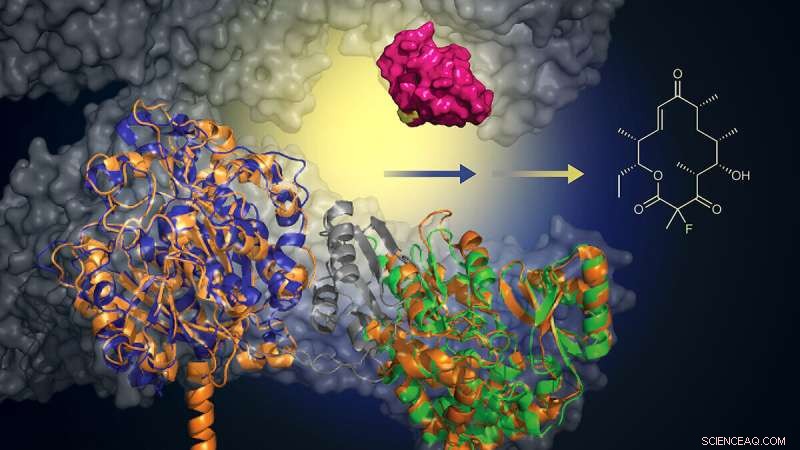
Avec l'ajout d'un biocatalyseur d'origine murine (vert), cette protéine modifiée peut ajouter un atome de fluorure pour créer des analogues de macrolides (structure, à droite). Cette approche offre une méthode plus verte et plus efficace pour créer de nouveaux antibiotiques. Crédit :Martin Grininger et Rajani Arora
Une équipe internationale de chercheurs a développé une méthode pour modifier une classe d'antibiotiques, en utilisant des organismes microscopiques qui produisent ces composés naturellement.
Les résultats, publiés le 25 juillet dans Nature Chemistry , pourrait conduire à une production plus efficace d'antibiotiques efficaces contre les bactéries résistantes aux médicaments.
L'équipe a commencé avec un micro-organisme génétiquement programmé pour produire l'antibiotique érythromycine. Scientifiques de l'Institut de Chimie Organique et Chimique
La biologie de l'université allemande de Goethe s'est demandé si le système pouvait être modifié génétiquement pour assembler l'antibiotique avec un atome de fluor supplémentaire, ce qui peut souvent améliorer les propriétés pharmaceutiques.
"Nous analysions la synthèse des acides gras depuis plusieurs années lorsque nous avons identifié une partie d'une protéine de souris qui, selon nous, pourrait être utilisée pour la biosynthèse dirigée de ces antibiotiques modifiés, si elle était ajoutée à un système biologique qui peut déjà fabriquer le composé natif", a déclaré Martin Grininger, professeur de chimie biomoléculaire à l'Université Goethe.
En collaboration avec le laboratoire de David Sherman de l'Université du Michigan, spécialisé dans ce système d'assemblage biologique, l'équipe a utilisé l'ingénierie des protéines pour remplacer une partie de la machinerie native du système par le gène de souris fonctionnellement similaire.
"C'est comme prendre une pièce de moteur d'une Mercedes et la mettre dans une Porsche pour en faire un meilleur moteur hybride. Vous obtenez un moteur Porsche qui peut faire de nouvelles choses et qui fonctionne encore mieux", a déclaré Sherman, membre du corps professoral de l'U-M Life. Institut des Sciences et professeur de chimie médicinale au Collège de Pharmacie.
"Nous pouvons désormais tirer parti de cette ingénierie des protéines pour créer de nouveaux composés contenant cet atome de fluor très recherché, que les chimistes ont du mal à ajouter aux antibiotiques macrolides depuis longtemps."
La raison pour laquelle cet atome de fluor ajouté est si souhaitable est qu'il modifie non seulement la structure du produit final, mais également la capacité du produit à tuer les bactéries et à agir en toute sécurité chez les patients.
L'érythromycine agit en se liant et en bloquant l'activité du ribosome bactérien, qui est essentiel à la survie des bactéries. Certaines bactéries ont développé des moyens d'empêcher cette liaison, les rendant résistantes au traitement avec des antibiotiques. La modification de la structure de l'antibiotique avec un atome de fluor surmonte cet avantage évolutif, restaurant la capacité du composé à combattre les bactéries.
Alors que les chimistes ont développé des méthodes pour ajouter le fluor de manière synthétique, le processus est ardu et nécessite l'utilisation de réactifs chimiques toxiques. La nouvelle méthode de biosynthèse développée par les chercheurs de l'Université Goethe et de l'U-M surmonte ces défis.
"C'est un développement très excitant, car nous pouvons contourner toutes les étapes de synthèse chronophages et les produits chimiques dangereux", a déclaré Sherman. "Nous avons montré que nous pouvions essentiellement reprogrammer un organisme pour fabriquer directement le produit fluoré."
Les chercheurs soulignent que les composés fluorés sont encore à quelques années d'être disponibles en clinique. Mais les résultats offrent une voie plus efficace pour développer de nouveaux antibiotiques, et même des antiviraux et des médicaments anticancéreux.
"Notre approche a fait ses preuves sur un petit ensemble d'antibiotiques, mais elle pourrait finalement être utilisée pour développer une large gamme de produits pharmaceutiques avec une utilisation minimale de produits chimiques et de sous-produits toxiques", a déclaré Grininger. La structure des protéines offre des indices sur le mécanisme de résistance aux médicaments