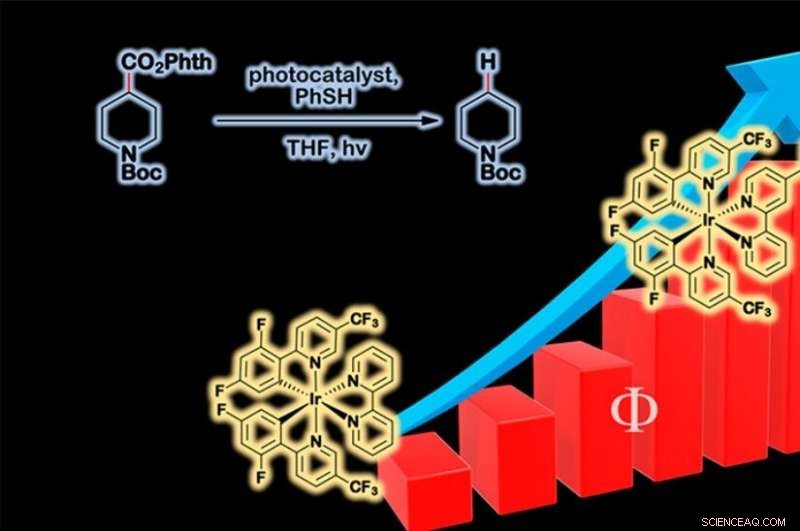
Le rendement quantique de la réaction, c'est ainsi que les chercheurs mesurent l'efficacité d'une réaction activée par la lumière. Crédit :Anna Zieleniewska.
S'inspirant de la photosynthèse et de la manière dont elle peut atteindre une efficacité élevée dans les plantes, Les professeurs régents Tom Moore et Ana Moore de la School of Molecular Sciences de l'Arizona State University et leurs groupes, avec des collègues du Département de chimie de l'Université de Princeton (y compris les professeurs Gregory Scholes et Robert Knowles), ont introduit un catalyseur bioinspiré qui allonge l'état productif de certaines réactions chimiques.
« Travailler avec les groupes de Princeton de Knowles et Scholes nous a donné de nouvelles perspectives et applications pour notre bioinspiré, systèmes photosynthétiques artificiels, ", a déclaré Ana Moore. Les professeurs régents Ana et Thomas Moore de l'École des sciences moléculaires de l'ASU. Crédit d'image:Mary Zhu Télécharger l'image complète
"Dans ce cas, nous avons repensé un photocatalyseur important dans l'industrie chimique en utilisant le principe du transfert d'électrons à couplage de protons (PCET) pour fournir une efficacité catalytique améliorée.
« Le PCET est largement utilisé dans les catalyseurs naturels où les voies de réaction à faible énergie produisant un seul produit sont essentielles. Il est gratifiant de trouver une application pratique pour les constructions PCET que nous avons récemment développées. Améliorer l'efficacité catalytique des réactions qui aboutissent à des composés avec des l'activité pharmacologique pourrait contribuer au développement plus durable d'une industrie chimique plus verte."
L'équipe a utilisé PCET pour manipuler le photocatalyseur afin de ralentir la recombinaison de charge, imitant essentiellement le processus qui fait bourdonner la photosynthèse.
Leur mécanisme cale une étape élémentaire du processus d'un facteur 24 par rapport à un composé de référence. PCET est une classe de réactions impliquant le transfert d'un électron et d'un proton.
Au cœur de cette recherche collaborative se trouve un modèle chimique, une sous-structure PCET, développé par les chercheurs ici à l'ASU. Le modèle est lié à un complexe d'iridium qui diminue efficacement la force motrice de la recombinaison de charge, prolongeant ainsi l'état actif dans lequel la chimie peut avoir lieu.
Le modèle est basé sur le complexe de dégagement d'oxygène dans la photosynthèse qui se trouve dans chaque plante, l'enzyme qui produit de l'oxygène pour le monde entier. Il y a deux acides aminés à proximité du complexe évoluant de l'oxygène - la tyrosine et l'histidine liées à l'hydrogène - et ces deux acides aminés éloignent les électrons du complexe évoluant de l'oxygène, par un mécanisme PCET, afin que l'enzyme soit capable de produire de l'oxygène.
Les Moore et ses collègues ont fait ce modèle, benzimidazole-phénol (BIP), qui est chimiquement très similaire à ces deux acides aminés dans la photosynthèse. Ceci est ensuite utilisé pour contrôler la direction du transfert d'électrons en catalyse.
Le papier, "Ligand basé sur PCET limite la recombinaison de charge avec un catalyseur photoredox Ir (III), " vient d'être publié dans le Journal de l'American Chemical Society .
La recherche combine des contributions aux mécanismes de photocatalyse du laboratoire Knowles, spectroscopie résolue en temps ultra-rapide du laboratoire Scholes, et le modèle BIP des laboratoires de Thomas Moore et Ana Moore.
Centre de recherche sur la frontière énergétique
La recherche répond à l'une des principales priorités du groupe Bioinspired Light-Escalated Chemistry (BioLEC) basé à Princeton, un centre de recherche Energy Frontier créé en 2018 et financé par le ministère de l'Énergie. BioLEC est dirigé par Scholes, William S. Todd de Princeton, professeur de chimie et président du département.
"C'est absolument dû au centre. Rob, Tom et Ana étaient les moteurs intellectuels de cette idée, " dit Scholes. " Tiens, nous avons ajouté un « circuit » supplémentaire au photocatalyseur moléculaire qui a supprimé la voie de désactivation. Notre circuit sert en quelque sorte de tampon, maintenant les espèces à haute énergie en place jusqu'à ce que le catalyseur puisse initier la réaction chimique. Je pense que c'est une belle réussite."
"Travailler avec Rob et Greg et les étudiants et post-doctorants du centre s'est avéré encore plus excitant et gratifiant que ce que nous espérions lorsque l'idée a été formulée pour la première fois pour la proposition BioLEC, " ont déclaré les Moore.
Dans la nature, la photosynthèse se produit lorsqu'une plante absorbe de la lumière qui génère une séparation de charge dans son « centre de réaction ». Cette réaction entraîne à la fois l'oxydation de l'eau et la fixation du dioxyde de carbone dans les combustibles utilisés par la plante. La recombinaison des charges court-circuite essentiellement le processus photosynthétique. Donc, la nature a développé des moyens de maintenir cette séparation en utilisant des relais redox.
Les chercheurs ont utilisé ces relais très redox dans leur enquête comme les composants essentiels d'une série de courte distance, étapes de transfert d'équivalent redox rapides qui concurrencent efficacement la recombinaison de charge.
Des processus évolutifs ont sélectionné ces relais redox où, grâce au transfert d'un électron et d'un proton entre deux acides aminés à liaison hydrogène, il peut effectuer des transferts très rapides qui séparent davantage les charges.
En éloignant rapidement les charges, vous empêchez cette recombinaison de charge. Cela conduit à l'efficacité de la photosynthèse. Les chercheurs ont utilisé cette idée.
La structure du modèle BIP développé par les Moores est similaire à ces deux acides aminés.
"Assez sur, des études dans le laboratoire de Scholes du catalyseur remanié avec le BIP ont montré une durée de vie plus longue pour l'intermédiaire radicalaire réactif et - voici la preuve dans le pudding - le rendement de la réaction a plus que doublé, " a déclaré Tom Moore. " La nature utilise le PCET en catalyse, et Dame Nature sait une chose ou deux sur l'efficacité, chimie durable."