Des chercheurs de l'Université de l'Illinois démontrent une méthode plus efficace et plus respectueuse de l'environnement pour produire du peroxyde d'hydrogène avec des nanoparticules de palladium-or, un catalyseur qu'ils ont trouvé fonctionne mieux lorsque les particules de palladium sont entourées d'or. Crédit :Claire Benjamin/Université de l'Illinois Urbana-Champaign
Peroxyde d'hydrogène (H
Une équipe dirigée par l'Université de l'Illinois Urbana-Champaign a démontré une méthode plus efficace et respectueuse de l'environnement pour produire H
« Alors que les deux ingrédients, l'hydrogène et l'oxygène, sont soit peu coûteux, soit disponibles gratuitement dans l'atmosphère, le peroxyde d'hydrogène est très réactif et instable, ce qui le rend très difficile à produire, " a déclaré le premier auteur Tomas Ricciardulli, un étudiant diplômé en génie chimique et biomoléculaire à l'UIUC.
Actuellement, produire H
Il y a des décennies, les chercheurs ont proposé une méthode plus simple, moins cher, et une méthode alternative « plus verte » en une étape où un catalyseur (des nanoparticules de palladium-or) entraîne la réaction à la place. Bonus :le catalyseur peut être recyclé pour produire encore et encore du peroxyde d'hydrogène.
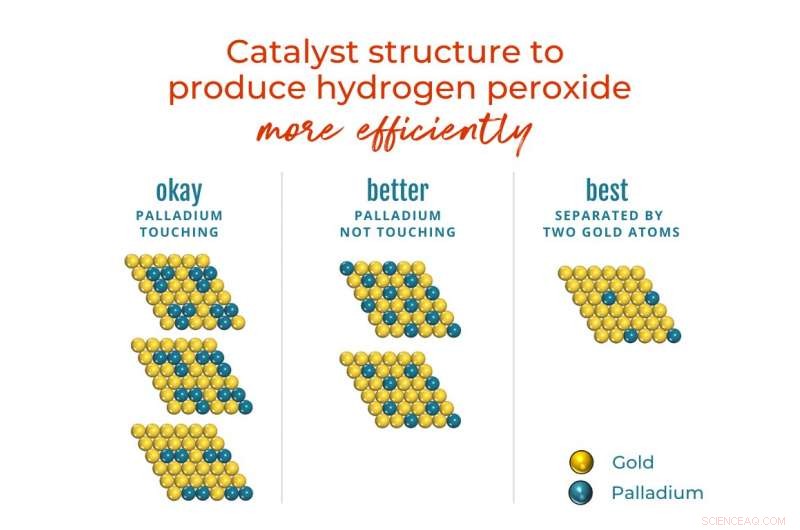
"Toutefois, l'hydrogène et l'oxygène forment également de l'eau, et cette méthode de «synthèse directe» proposée était connue pour synthétiser 80 pour cent d'eau et seulement 20 pour cent de peroxyde d'hydrogène, " a déclaré l'auteur principal David Flaherty, professeur de génie chimique et biomoléculaire à l'UIUC. "Les scientifiques ont débattu avec acharnement de l'arrangement des atomes de palladium et d'or nécessaires dans les nanoparticules pour augmenter la sélectivité pour le peroxyde d'hydrogène et pourquoi cela fonctionne."
Un rapport plus élevé d'atomes d'or et de palladium dans le catalyseur produit plus de H
Le professeur David Flaherty de l'Université de l'Illinois et l'étudiant diplômé Tomas Ricciardulli démontrent une méthode plus efficace et plus respectueuse de l'environnement pour produire du peroxyde d'hydrogène, qui est très demandé pour ses propriétés antiseptiques. Crédit :Claire Benjamin/Université de l'Illinois Urbana-Champaign
Significativement, les catalyseurs offrent des performances stables sur plusieurs jours d'utilisation, atteindre continuellement ces sélectivités remarquables à H
L'organisation de ces atomes au sein du catalyseur compte aussi :les atomes de palladium qui se touchent favorisent la formation d'eau, tandis que les atomes de palladium entourés d'or favorisent H
Quoi de plus, ils ont découvert que l'influence s'étend du premier anneau d'atomes voisins qui entourent l'atome de palladium à la deuxième couche d'atomes, appelé le prochain voisin le plus proche. Plus H
"Nous avons démontré comment créer un catalyseur très efficace et sélectif, " dit Flaherty, qui est également un boursier de la faculté de Dow Chemical Company. « Tout en promettant, il y a encore des obstacles à surmonter pour adopter cette méthode commercialement."
Le groupe de recherche Flaherty poursuit le développement de catalyseurs à nanoparticules avec de nouvelles compositions et de nouveaux réacteurs pour permettre des méthodes hybrides chimiques-électrochimiques pour cette réaction. "Notre objectif ultime est de développer une technologie réalisable pour la production distribuée de H
Les chercheurs s'attendent également à ce que leurs activités révèlent d'autres concepts scientifiques clés pour électrifier la fabrication de produits chimiques en cours de route. 