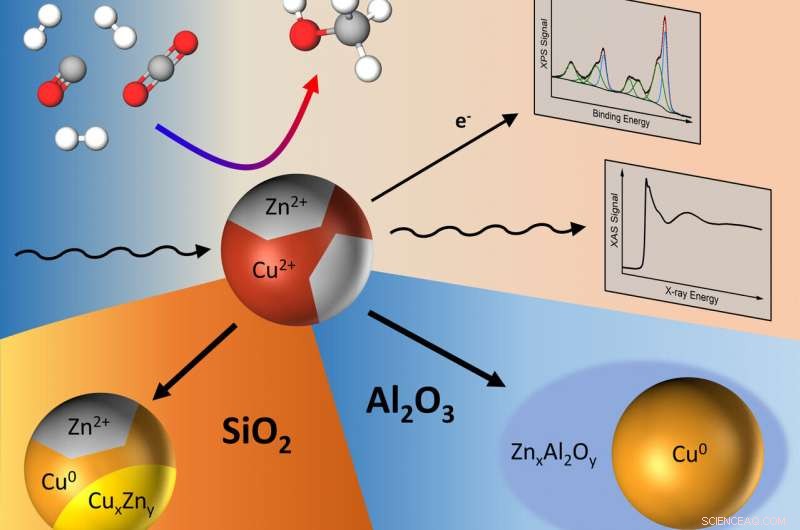
Les nanoparticules bimétalliques Cuivre-Zinc convertissent le CO, CO2 et H2 dans le méthanol. Crédit :© FHI/Kordus
La production commerciale actuelle de méthanol par hydrogénation du gaz à effet de serre CO
Le méthanol peut servir de source d'énergie ou de matière première pour la production d'autres produits chimiques, avec plus de 60 millions de tonnes métriques produites chaque année. Le cuivre traditionnel, le catalyseur d'oxyde de zinc et d'oxyde d'aluminium convertit le gaz de synthèse, qui est composé de H2, CO et CO
L'équipe a étudié le processus catalytique dans des conditions de réaction réalistes reproduisant celles appliquées dans le processus industriel, ce qui signifie des pressions élevées (20-60 bar) et des températures douces. Cela nécessitait un rayonnement X généré par le synchrotron. Simon R. Bare de la source lumineuse à rayonnement synchrotron de Stanford, qui a contribué aux expériences, explique :« Les réactions à de telles températures et hautes pressions doivent avoir lieu dans un récipient fermé qui doit également être transparent pour les rayons X, ce qui rend les mesures difficiles. La conception spéciale du réacteur en combinaison avec le rayonnement synchrotron nous a permis d'entreprendre des mesures dites operando, où nous avons observé en direct ce qui arrive aux composants catalytiques dans les conditions de réaction pertinentes sur le plan industriel. » Cela a permis aux chercheurs de suivre non seulement la naissance et la mort du catalyseur, mais aussi son évolution et ses transformations entraînant des évolutions de son activité et de sa sélectivité.
En combinant les résultats de la microscopie, spectroscopie et mesures catalytiques, l'équipe a constaté que certains supports avaient une influence plus positive sur les performances du catalyseur que d'autres en raison de la façon dont ils interagissaient avec l'oxyde de zinc, qui était disponible de manière très diluée dans le cadre des nanoparticules de Cu-Zn. Sur des supports en oxyde de silicium, l'oxyde de zinc a été partiellement réduit en zinc métallique ou a donné naissance à un alliage de laiton au cours du processus catalytique, ce qui, au fil du temps, s'est avéré préjudiciable à la production de méthanol. Lors de l'utilisation d'oxyde d'aluminium comme support, le zinc interagit fortement avec le support et s'incorpore à son réseau, donnant lieu à une modification de la sélectivité de la réaction vis-à-vis de l'éther diméthylique. "C'est une découverte intéressante", dit David Kordus, l'autre auteur principal de l'étude et le doctorat. étudiant au Département des Sciences de l'Interface de FHI. "Nous savons maintenant que le choix du matériau de support a une influence sur la façon dont les composants actifs du catalyseur se comportent et s'adaptent dynamiquement aux conditions de réaction. En particulier, l'état d'oxydation du zinc est fortement influencé par cela, qui devrait être pris en compte pour la conception future du catalyseur. »
Cet ouvrage publié dans Communication Nature démontre que l'oxyde de zinc n'a pas besoin d'être disponible dans le cadre du support, mais qu'il a toujours une fonction bénéfique même lorsqu'il est disponible sous une forme hautement diluée dans le cadre du catalyseur à nanoparticules lui-même. Cela aidera à mieux élucider les catalyseurs de synthèse du méthanol et potentiellement conduire à une amélioration du catalyseur pour cet important processus industriel.