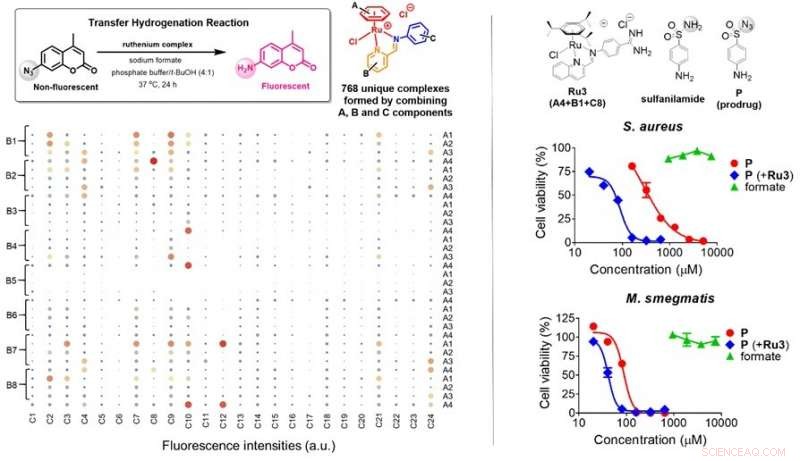
(À gauche) Un total de 768 complexes de ruthénium uniques (4x8x24) ont été générés via des réactions d'auto-assemblage utilisant des composants moléculaires A (4 types), B (8 types) et C (24 types) en solutions aqueuses, puis criblés pour les activités d'hydrogénation de transfert en présence de formiate. La taille des cercles grisés indique l'efficacité des complexes de ruthénium dans la réalisation de l'hydrogénation par transfert sur la sonde conduisant à l'activation de la fluorescence. Six candidats possibles ont été identifiés. (À droite) Les propriétés antibactériennes du promédicament P (rouge) chez S. aureus et M. smegmatis ont été activées en présence de Ru3 (bleu) tandis que la supplémentation en formiate (vert) n'a eu aucun effet sur la croissance bactérienne. Ru3, assemblé au format A4, B1 et C8, a pu utiliser le formiate présent dans les cellules bactériennes pour activer P. Crédit : Angewandte Chemie Édition Internationale
Des chercheurs de l'Université nationale de Singapour ont développé une approche pour cibler sélectivement les bactéries pathogènes en exploitant un métabolite intracellulaire connu sous le nom de formiate, abondante dans ces bactéries, comme nouvelle stratégie antimicrobienne. Le formiate est un métabolite essentiel nécessaire à la croissance de certaines souches pathogènes, mais on ne le trouve qu'en faibles quantités dans les cellules de mammifères.
L'abondance et l'évolution du comportement pathogène des microorganismes bactériens engendrent une tolérance et une résistance aux antibiotiques, qui représentent un danger pour la santé publique mondiale. De nouvelles stratégies thérapeutiques sont donc nécessaires pour faire face à cette menace croissante.
L'équipe de recherche dirigée par le professeur Ang Wee Han du département de chimie, NUS a proposé une nouvelle approche pour cibler les bactéries en exploitant le formiate, un métabolite cellulaire que l'on ne trouve que dans des espèces bactériennes particulières, pour activer un promédicament antibactérien et inhiber sélectivement la croissance bactérienne. Les chercheurs ont développé un système de mise en cage moléculaire pour les médicaments antibactériens sulfamides en remplaçant leur groupe fonctionnel amide essentiel par l'azide (N
Le professeur Ang a dit, "Il s'agit du premier rapport qui exploite un métabolite cellulaire unique pour déclencher l'activation d'un promédicament dans les bactéries. Il ouvre la voie à une nouvelle approche de thérapie antibactérienne ciblée en exploitant les différences dans l'apparition de métabolites naturels parmi les souches pathogènes."
Le promédicament sulfonamide conçu de manière rationnelle avec une partie de mise en cage azide a été efficacement activé par les complexes organoruthéniques dans des bactéries abondantes en formate avec une amélioration jusqu'à 8 fois de l'efficacité du médicament, en particulier dans les bactéries pathogènes, Staphylococcus aureus et Escherichia coli. En revanche, élévation de l'efficacité chez Mycobacterium smegmatis, qui a une capacité de génération de formate limitée, n'a été multiplié que par deux. Cela a validé la thèse selon laquelle le formiate de métabolite intracellulaire peut être ciblé pour le développement de nouvelles stratégies thérapeutiques antibactériennes.
Le professeur Ang a dit, "La résistance aux antibiotiques est l'un des défis les plus sérieux auxquels l'humanité est confrontée et pourtant le développement de nouveaux antibiotiques n'a pas suivi le rythme de cette menace croissante. Le métabolome bactérien unique offre de nouvelles possibilités pour résoudre ce problème. Nous espérons que cette découverte stimulera de nouvelles recherches ciblant des métabolites pour le développement d'agents antibactériens meilleurs et plus sélectifs."
L'équipe de recherche travaille au développement d'autres stratégies d'activation de promédicaments qui peuvent exploiter le formiate bactérien endogène. En outre, des investigations sur d'autres antibiotiques cliniques tels que le triméthoprime et le sulfaméthoxazole sont également en cours.