
Dommages de guerre avec conséquences :après la Seconde Guerre mondiale, Le relief en marbre de Giuseppe Torretti "Adoration des bergers" n'a survécu que par fragments (sections brunâtres), qui sont montrés ici en combinaison avec une photo en noir et blanc de l'œuvre d'art intacte pour donner une impression globale. Crédit :Laboratoire de recherche Rathgen, Staatliche Museen zu Berlin – Fondation du patrimoine culturel prussien
Le relief "Adoration des bergers" du sculpteur italien Giuseppe Torretti est défiguré par des cristaux de sel grumeleux. Maintenant, un groupe de recherche de l'Institut Max Planck pour la recherche sur l'état solide de Stuttgart a établi que l'hémihydrate d'acétate de calcium qui constitue ces efflorescences a une structure similaire à celle de la protéine collagène. Les caractéristiques structurelles permettent non seulement d'éviter les dommages de ce type, mais ont également fourni aux chercheurs de nouvelles idées intéressantes pour la chimie bioinorganique.
Le relief en marbre "Adoration des bergers" a environ 300 ans et a certainement eu une histoire mouvementée. A la fin de la Seconde Guerre mondiale, il a été déplacé de Berlin vers l'Union soviétique, où des tentatives ont été faites pour réparer les dommages qu'elle avait subis pendant la guerre, y compris en utilisant de la colle. Au début des années 1990, l'œuvre de Giuseppe Torretti (1664-1743) a été restituée au Musée d'art byzantin de Berlin, où les spécialistes enlevaient la colle à l'acétate d'éthyle, un ester d'acide acétique.
C'est précisément ce processus qui semble avoir provoqué des changements chimiques dans la surface, conduisant à la formation de blanc, efflorescences en forme d'aiguilles quelques années plus tard. Les experts du laboratoire de recherche Rathgen à Berlin les ont identifiés comme un hémihydrate d'acétate de calcium chimique, c'est-à-dire le sel de calcium de l'acide acétique qui contient également de l'eau. Heures supplémentaires, en d'autres termes, le calcium du marbre s'était lié aux ions acétate du solvant pour former un nouveau sel - et cette substance a également été trouvée sur d'autres œuvres d'art anciennes.
Cependant, ce n'est que maintenant que la structure cristalline du composé a été déterminée avec précision. Les restaurateurs s'appuient sur les caractéristiques structurelles comme données de référence pour pouvoir identifier les produits de corrosion et expliquer le processus sous-jacent, ainsi que, idéalement, l'empêcher. Pour déterminer la structure des efflorescences du relief de Torretti, Gerhard Eggert de l'Institut des sciences de la conservation de l'Académie nationale des arts et du design, Stuttgart, fait appel à Robert Dinnebier, chef du groupe de diffraction des rayons X à l'Institut Max Planck pour la recherche sur l'état solide à Stuttgart. C'est l'un des rares groupes au monde à se spécialiser dans l'élucidation structurelle complexe, même dans des échantillons qui ne sont disponibles que sous forme de poudre et non sous forme de cristal unique.

Des efflorescences blanches d'acétate de calcium hémihydraté ont été trouvées sur un fragment de berger du relief de Giuseppe Torretti. Crédit :Laboratoire de recherche Rathgen, Staatliche Museen zu Berlin – Fondation du patrimoine culturel prussien
Les caractéristiques structurelles aident à prévenir les dommages dus à la corrosion
Le projet financé par la DFG « À la recherche de structure » a également réussi à déterminer cette structure, révélant que les ions calcium s'organisent le long de chaînes en forme de spirale - en d'autres termes, ils forment des hélices. Les ions acétate, d'autre part, s'asseoir entre les ions calcium et agir comme des ponts. Tout à fait, trois de ces cordes de calcium s'enroulent les unes autour des autres de la même manière que les trois brins d'une tresse.
Le collagène forme également une triple hélice
Les structures en hélice de ce type ne sont pas rares dans la nature vivante. ADN, la molécule porteuse de matériel génétique, prend la forme d'une double hélice, c'est-à-dire un double brin enroulé en spirale. Selon Dinnebier, cependant, la structure qui vient d'être identifiée présente une similitude frappante avec les protéines de collagène en particulier, tels que ceux trouvés dans les tissus conjonctifs de notre corps. "Les chaînes d'acides aminés du collagène forment également une triple hélice, " explique le cristallographe.
Cependant, les chercheurs de Max Planck à Stuttgart n'ont pas pu utiliser des échantillons provenant des efflorescences sur le relief du berger de Torretti pour leur analyse structurelle. "La technique de diffraction des rayons X correspondante nécessite des quantités que vous ne pouvez pas obtenir à partir d'une œuvre d'art de ce genre, " explique Sebastian Bette du groupe de travail Dinnebier. Les chercheurs ont donc dû synthétiser leur propre acétate de calcium hémihydraté, ce qu'ils ont fait en laissant une solution d'acétate de calcium dans un pot en terre cuite couvert à faible humidité atmosphérique pendant six mois. Pendant ce temps, la solution a lentement traversé les pores de la paroi du pot et s'est cristallisée à l'extérieur sous forme d'acétate de calcium hémihydraté. « Nous avons ensuite pu utiliser cette poudre pour réaliser l'analyse par diffraction des rayons X, " dit Bette. Cela a révélé les positions des atomes individuels les uns par rapport aux autres - et donc la structure du composé.
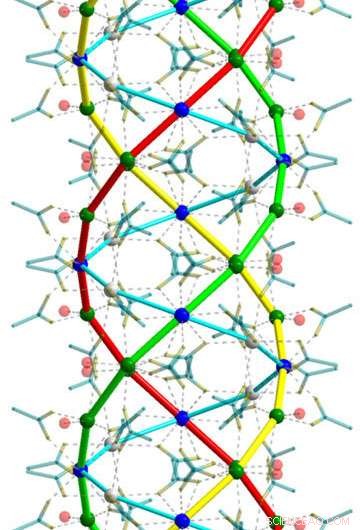
Sel avec une structure inhabituelle :comme les chercheurs de Max Planck l'ont établi, l'hémihydrate d'acétate de calcium qui compose les efflorescences de "L'adoration des bergers" de Torretti cristallise en une triple hélice, comme celui également formé par le collagène. Crédit :Sébastien Bette
Une cellule unitaire inhabituellement grande
"Il est fascinant de découvrir un motif structurel hélicoïdal dans un composé relativement simple tel que l'acétate de calcium hémihydraté, " s'enthousiasme Robert Dinnebier. En plus de 30 ans de travail sur l'élucidation structurale par diffraction des rayons X, il a vu beaucoup de structures cristallines et n'est plus facilement surpris. Mais il a été étonné de la structure en triple hélice qui a maintenant été identifiée.
Apparemment, les chercheurs ont également été surpris par la taille inhabituelle de la cellule unitaire. Les cristallographes utilisent ce terme pour désigner la plus petite unité répétitive d'une structure cristalline. Avec un volume d'un peu moins de 12, 000 ångströms cubes, une seule maille élémentaire de la substance analysée est plusieurs dizaines de fois plus grosse que les mailles élémentaires les plus courantes des sels simples et contient 64 ions calcium. "C'est un nombre incroyablement élevé pour un composé relativement simple avec seulement trois composants, à savoir le calcium, acétate et eau, " dit Bette.
D'autre part, Robert Dinnebier considère désormais la similitude structurelle avec les protéines de collagène tout à fait plausible :« En effet, l'acide aminé le plus commun dans le collagène est la glycine. » Comme le plus simple de tous les acides aminés, celui-ci est étroitement lié à l'acide acétique au niveau moléculaire et donc aussi à son sel, acétate. Si vous remplacez un atome d'hydrogène par un groupe amino dans la molécule d'acide acétique, vous obtenez de la glycine. Les chercheurs de Stuttgart considèrent maintenant qu'il est probable qu'un glycinate de calcium hélicoïdal existe également. En principe, Dinnebier trouve "fascinant" que ces "structures hélicoïdales complexes ne soient clairement pas limitées à des chaînes d'acides aminés. ils peuvent également se former ailleurs dans certaines circonstances.
Modèle possible pour les protéines avec des structures hélicoïdales
En raison de sa similitude avec le collagène, les chercheurs s'intéressent maintenant vivement à l'acétate de calcium hémihydraté en tant que substance. Sebastian Bette dit :« Dans l'évolution, le collagène a joué un rôle clé dans la transition des organismes unicellulaires aux organismes multicellulaires et donc aussi dans l'émergence des tissus. l'acétate de calcium hémihydraté ou un potentiel glycinate de calcium pourraient ouvrir de toutes nouvelles possibilités bioinorganiques. "Par exemple, nous savons déjà que la double hélice d'ADN peut être utilisée comme matrice pour faire cristalliser d'autres composés chimiques dans une structure hélicoïdale, " dit Bette. " Ce n'est pas un grand saut d'imagination d'utiliser la triple hélice démontrée comme modèle pour les protéines avec des structures hélicoïdales, par exemple."