Crédit :Angewandte Chemie
Au Japon, le poisson-globe est considéré comme un mets délicat, mais le chatouillement des papilles s'accompagne d'un chatouillement des nerfs :le fugu contient de la tétrodotoxine, une toxine nerveuse puissante. A faible dose, Les essais cliniques ont montré que la tétrodotoxine remplace les opioïdes pour soulager la douleur liée au cancer. Dans la revue Angewandte Chemie , les scientifiques ont introduit une nouvelle voie pour la synthèse totale (production complète d'un produit naturel à partir des matériaux actuels) de la tétrodotoxine.
Manger du fugu provoque d'abord un léger picotement dans la bouche, qui peut avoir un effet relaxant ou euphorique, en supposant que le cuisinier sache ce qu'il fait. Si le poisson est mal préparé, les choses peuvent mal se terminer :la tétrodotoxine bloque les canaux sodiques voltage-dépendants, et donc l'influx nerveux. Cela peut entraîner une paralysie et même des difficultés respiratoires. Dans l'UE, l'importation et la préparation de fugu comme aliment sont interdites. Au Japon et dans d'autres pays, un certain nombre de lois strictes réglementent la préparation et la consommation de produits à base de poisson-globe. Cependant, il y a des décès occasionnels.
A très faible dose, la tétrodotoxine est un analgésique et pourrait être utilisé pour traiter la douleur intense, comme dans le traitement du cancer. Les premières études cliniques sont en cours. Il est donc important de développer une méthode simple, méthode synthétique fiable pour donner accès à la tétrodotoxine et à des composés structurellement apparentés - pour la recherche et finalement une production robuste et peu coûteuse.
La tétrodotoxine a un effet unique, très complexe, structure en forme de cage (un orthoester tricyclique) ainsi qu'un composant guanidine cyclique. La guanidine est un composant important de nombreuses molécules biologiques, y compris l'arginine. La charpente de la tétrodotoxine est fortement oxydée et possède cinq groupes hydroxy (-OH) comme substituants. Un certain nombre de synthèses totales différentes de tétrodotoxine ont déjà été publiées, dont un de chercheurs dirigés par Satoshi Yokoshima à l'Université de Nagoya (Japon) en 2017. Maintenant, Yokoshima et son équipe en ont introduit un autre, nouvelle synthèse totale.
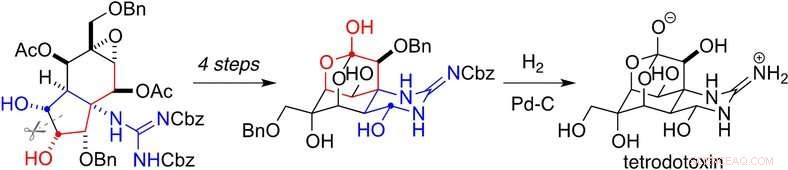
L'étape clé est une réaction de Diels-Alder entre un composé de départ connu (une énone) et un composant contenant du silicium (un siloxydiène) pour fabriquer un intermédiaire tricyclique avec le bon arrangement spatial (stérique) pour permettre une fixation appropriée des groupes hydroxy et ensuite, construction de la « cage ». La formation du composant guanidine commence par l'introduction d'un groupe amino, soit par une méthode conventionnelle en quatre étapes, soit par une séquence réactionnelle en trois étapes basée sur une conversion nouvellement développée d'un alcyne terminal en un nitrile. Finalement, les « ponts » nécessaires à la formation de la cage se construisent en plusieurs étapes. Une réaction de couplage croisé a été utilisée pour introduire un substituant carboné (groupe hydroxyméthyle) sur la cage. L'utilisation d'autres composants pour la réaction de couplage croisé pourrait conduire à la production de molécules structurellement apparentées.